서론
실험방법
기질물질 특성평가
광산배수 시료채취 및 특성평가
기질물질에 의한 광산배수의 지화학특성 변화
결과 및 토의
기질물질 특성평가
광산배수 시료채취 및 특성평가
기질물질에 의한 광산배수의 지화학적 특성평가
결론
서론
폐광산에서 배출되는 광산배수는 광종, 광상, 배출형태 등의 광산환경에 따라 다양한 오염특성을 나타낸다. 폐탄광 갱내수는 일반적으로 약산성의 pH 조건에서 Fe가 주요 오염원으로 존재하나 폐석장 침출수는 때때로 고농도의 Al과 Mn이 수반되기도 한다. 폐금속광의 경우, 갱내수 또는 광물찌꺼기 적치장 침출수는 다양한 pH 범위에서 Fe, Mn, Al뿐만 아니라 Cu, Zn, Cd, As 등이 광산배수 내 존재하기도 한다(Tabak and Govind, 2003). 광산배수에 존재하는 다양한 원소를 처리하기 위해 국내에서는 1990년대 후반부터 폐탄광 광산배수를 중심으로 자연정화공법이 적용되고 있고 전국에 약 40여기가 설치되어 운영되고 있다(MIRECO, 2016).
광산배수 정화에 적용할 수 있는 자연정화공법의 주요 단위공정은 Successive Alkalinity Producing System(SAPS), 산화‧침전조, 소택지로 구성되고 수질특성에 따라 배열 순서를 달리하여 적용 가능하다. 이중 SAPS는 산성광산배수 처리를 위한 필수적인 단위공정으로 알칼리를 공급하여 광산배수 내 산도(acidity)를 제거하는 역할을 한다. SAPS는 하단의 석회석 층과 상단의 유기 기질물질 층으로 구분된 구조로 이루어져 있고, 석회석 층 하단에는 유공관이 설치되어 있다. 광산배수는 하향류로 유동하면서 하부 유공관을 통해 배출되고, 배출관의 수두차를 이용하여 수위를 조절한다(Demchak et al., 2001; PIRAMID Consortium, 2003).
일반적으로 SAPS에서 유기 기질물질 층의 역할은 호기성 미생물을 활성화하여 용존산소를 제거하고 환원환경을 조성하여 Fe의 산화를 방지한다. 이는 하부 석회석 표면에 피복현상을 방지하여 지속적으로 알칼리 공급이 가능하도록 한다. 또한 유기 기질물질은 미생물에 의해 분해되면서 반응식 (1)과 같이 알칼리도를 생성하고, 환원조건, 탄소원, 황산염 등이 적절히 조성된 환경에서는 황산염환원균(Sulfate Reducing Bacteria; SRB)에 의한 황산염 환원반응과 동시에 2가 중금속이 식 (2)와 같이 황화물로 침전한다(Zagury et al., 2006; Neculita et al., 2007; Benedetto et al., 2005). 한편 Fe는 환원된 황과 반응하여 식 (3)과 같이 iron monosulfide가 형성되기도 한다(Ha et al., 2006; Ko et al., 2016). 이외 광산배수의 오염원소는 유기 기질물질 내에서 흡착 또는 탄산염, 수산화물로서의 침전을 포함한 다양한 제거기제(mechanism)가 발생한다(Chen et al., 2000; Song et al., 2001).
2CH2O + SO42- → H2S + 2HCO3- (1)
(CH2O : organic substrate)
M2+ + H2S + HCO3- → MS + 2H2O + 2CO2 (2)
(M2+ : divalent metals, e.g., Fe2+, Mn2+, Zn2+, Ni2+, Cu2+, Cd2+, Pb2+)
Fe2+ + H2S + S0 → FeS2 + 2H+ (3)
SAPS의 주요 기능이 광산배수의 무기산도(mineral acidity) 제거를 위한 지속적인 알칼리도 공급이므로, 광산배수가 석회석 층에 유입되기 전 유기 기질물질 층의 역할이 중요하다. 이는 유기 기질물질 층에서 무기산도의 저감과 환원환경 조성 등의 완충작용에 따라 석회석 층의 알칼리공급에 미치는 영향이 크기 때문이다. 특히 광산배수는 광종 및 배출형태에 따라 무기산도, 오염원소의 화학종, 산화환원전위 등의 지구화학적 특성이 다르기 때문에 유기 기질물질이 광산배수의 특성변화에 미치는 영향에 대한 평가가 요구된다. 따라서 본 연구는 유기 기질물질을 다양한 수질특성을 보이는 광산배수에 적용하여 지구화학적 특성변화를 평가하고, SAPS의 정화효율에 미치는 영향을 파악하고자 하였다.
실험방법
기질물질 특성평가
SAPS에서 주로 사용되는 유기 기질물질은 양송이 버섯재배 후 발생하는 폐상퇴비로 충청남도 부여군에 위치한 농장에서 획득하여 사용하였다. 폐상퇴비의 주요 구성물질은 볏집, 계분, 요소비료, 석고, 배양토, 석회 등으로 일반적으로 양송이버섯의 배양이 종료된 후 20일 내외의 폐상퇴비를 SAPS의 기질물질로 활용하고 있다. 실험에 사용된 유기 기질물질은 SAPS에서 이용하는 동일한 폐상퇴비를 사용하였다. 폐상퇴비는 상온에서 건조 후, 원소분석기(Elemental Alayzer; Flash EA 1112series, CE Instruments)를 이용하여 C와 N의 원소함량을 측정하였다. 폐상퇴비가 광산배수와 반응하는 동안 용출 가능한 용존 유기탄소(Dissolved Organic Carbon; DOC)를 측정하기 위해 폐상퇴비 20 g을 200 mL의 탈이온수(deionized water)에 2시간 동안 실온에서 200 rpm으로 진탕 후 0.45 µm로 여과하여 total organic carbon (TOC) 분석기(multi N/C 3100, analytikjena)로 분석하였다(Clesceri et al., 1998).
광산배수 시료채취 및 특성평가
실험에 사용된 광산배수는 광종(석탄광, 금속광) 및 배출형태(갱내수, 침출수)로 구분하고, 서로 다른 수질특성을 보이는 광산현장을 조사하여 5곳의 광산배수를 채취하였다. 폐금속광 광산배수는 경상북도 봉화군에 위치한 DD광산과 대구광역시에 위치한 DS광산에서 채취하였다. DD광산은 광물찌꺼기 적치장 침출수이고 DS광산은 갱도와 인접한 침출수이다. 폐탄광 광산배수는 경상북도 봉화군에 위치한 IW탄광, 강원도 정선군에 위치한 HJ탄광 및 SM탄광에서 채취하였다. 이중 IW광산과 HJ탄광의 배출형태는 갱내수이고, SM탄광은 갱내수와 폐석 침출수가 혼재되어 있다. 채취된 광산배수는 수질변화를 최소화하기 위해 냉동 보관하고, 실험 전 해동하여 수질분석을 수행하였다.
광산배수의 수질분석을 위해 pH, 온도, 용존산소, 전기전도도, 산화환원전위를 휴대용 측정기(Orion 3star, Thermo)를 이용하여 측정하였고, Fe2+, Fe, SS 농도는 각각 phenanthroline method(Clesceri et al., 1998), FerroVerⓇ Method 8008, photometric method(Krawczyk and Gonglewski, 1959)에 따라 색도계(Colorimeter, DR-890, HACH)로 측정하였다. 용존 양이온 분석용 시료는 0.45 µm 여과지로 여과한 후 50 mL 시료병에 채수하고 질산을 첨가하여 pH 2이하로 보존하였으며, 음이온 분석용 시료는 0.45 µm 여과지로 여과하여 산처리 없이 분석 전까지 4°C에서 냉장보관 하였다. 양이온은 ICP-OES(720-ES, Agilent)로 분석하였고, 음이온은 Metrohm사의 이온크로마토그래피(Metrohm 850)로 분석하였다.
기질물질에 의한 광산배수의 지화학특성 변화
광산배수 수질특성에 따른 기질물질의 반응특성을 관찰하기 위해 Table 1과 같이 회분식 실험을 구성하였다. 기질물질은 체걸음으로 2 mm 이하의 입도를 취하여 각각 100 g을 정량하였고, 각각의 광산배수는 400 mL를 정량하여 고압멸균기(autoclave, 121°C에서 15분)로 멸균한 serum bottle 500 mL에 반응시켰다. 비교시료(control)로 광산배수 대신 멸균 증류수를 동일조건의 유기 기질물질과 반응시켰다. 각각의 회분식 실험은 SAPS 유기물질 층의 조건과 유사한 혐기환경을 조성하기 위해 반응기에 30분간 질소(N2 100%) 가스를 주입하고, 30°C로 설정된 배양기에서 26일 동안 반응시켰다. 분석을 위해 주기적으로 50 mL의 시료를 채취하였고, 이후 15분간 질소가스를 주입하였다. 시료채취로 손실된 양은 동일한 광산배수로 보상하였고, 신뢰도를 확보하기 위해 각각의 조성으로 중복실험(duplicate)하였다. 회분식 실험 중 주기적으로 채취한 50 mL 시료 중 25 mL는 pH, ORP, 전기전도도를 휴대용 측정기(Star series, Thermo)를 이용하여 측정하였고, 일부는 황산염 분석을 위해 0.45 µm로 여과하고 휴대용 비색계(DR-890, Hach)를 이용하여 US EPA method 8051(David et al., 2007)에 따라 분석하였다. 시료 10 mL는 0.45 µm로 여과하여 농질산(HNO3)으로 산처리 한 후 ICP-OES로 양이온 원소를 분석하였다. 음이온 분석을 위해 10 mL의 시료를 0.45 µm 여과지로 여과하여 산처리 없이 Metrohm사의 이온크로마토그래피(Metrohm 850)로 분석하였다. 또한 5 mL 시료는 농인산(H3PO4)으로 산처리 한 후 총 유기탄소를 TOC 분석기(multi N/C 3100, analytikjena)로 분석하였다.
Table 1. Composition of the batch experiments
결과 및 토의
기질물질 특성평가
회분식 실험에 사용한 폐상퇴비의 물리화학적 특성을 분석하였다. 원소분석 결과 폐상퇴비 내 C와 N의 비는 10 내외이고 pH와 수분함량은 각각 7.6과 49.3%로 분석되었다(Table 2). 폐상퇴비의 C/N 비가 10 내외일 경우 생물학적 분해(biological degradation)가 용이하고 미생물이 쉽게 유기탄소를 취할 수 있는 것으로 알려져 있기 때문에(Be´chard, 1994), 기질물질을 선정하는데 주요 지표로 사용된다. 기존 연구에서 분석된 XRF 분석 결과, 폐상퇴비의 SiO2 함량과 loss on ignition (LOI)는 다른 기질물질(예를 들면, 볏집, 우분, 톱밥, 참나무 폐목 등)에 비해 높은 수치를 나타냈다(MIRECO, 2010). 이는 버섯재배를 위한 배양토 등 토양기원의 무기물이 포함되어 있기 때문이다.
Table 2. Physicochemical properties of organic substrate
광산배수 시료채취 및 특성평가
실험에 사용된 광산배수의 수질을 분석하였고 분석결과는 Table 3과 같다. DS광산, IW탄광, SM탄광의 광산배수는 pH 3.2 이하의 강산성으로 ORP가 300 mV 이상이고, 산도는 350 CaCO3 mg/L 이상을 나타냈다. 반면 DD광산과 HJ의 광산배수는 pH 6 이상으로 ORP가 상대적으로 낮고, 산도는 50 CaCO3 mg/L 이하를 분석되었다.
폐금속광인 DD광산과 DS광산의 광산배수는 다양한 오염원소를 보이는데, 광물찌꺼기 적치장 침출수인 DD광산은 Fe, As, Mn이, 갱내 침출수인 DS광산은 Fe, Al, Cu, Zn, Mn으로 오염된 특성을 보였다(Table 3). 폐탄광 갱내수인 HJ탄광과 IW탄광, 갱내수와 폐석 침출수가 혼재된 SM탄광의 광산배수는 산도에서 차이를 보이고, 오염원소로 Fe가 공통적으로 포함되어 있으나 HJ탄광은 상대적으로 낮은 농도의 Al과 Mn이 존재하였다. 또한 용존된 총 Fe 중 Fe2+가 차지하는 비율은 DD광산과 HJ탄광에서 70% 이상으로 Fe2+의 비율이 높았고, DS광산, IW탄광 및 SM탄광은 그 비율이 30% 이하로 Fe2+가 차지하는 비율이 상대적으로 낮았다. 또한 실험에 사용한 광산배수는 무기산도가 높을수록 Ca, Mg, SO42-의 함량이 높게 나타났다.
Table 3. Chemical properties of each mine drainage
기질물질에 의한 광산배수의 지화학적 특성평가
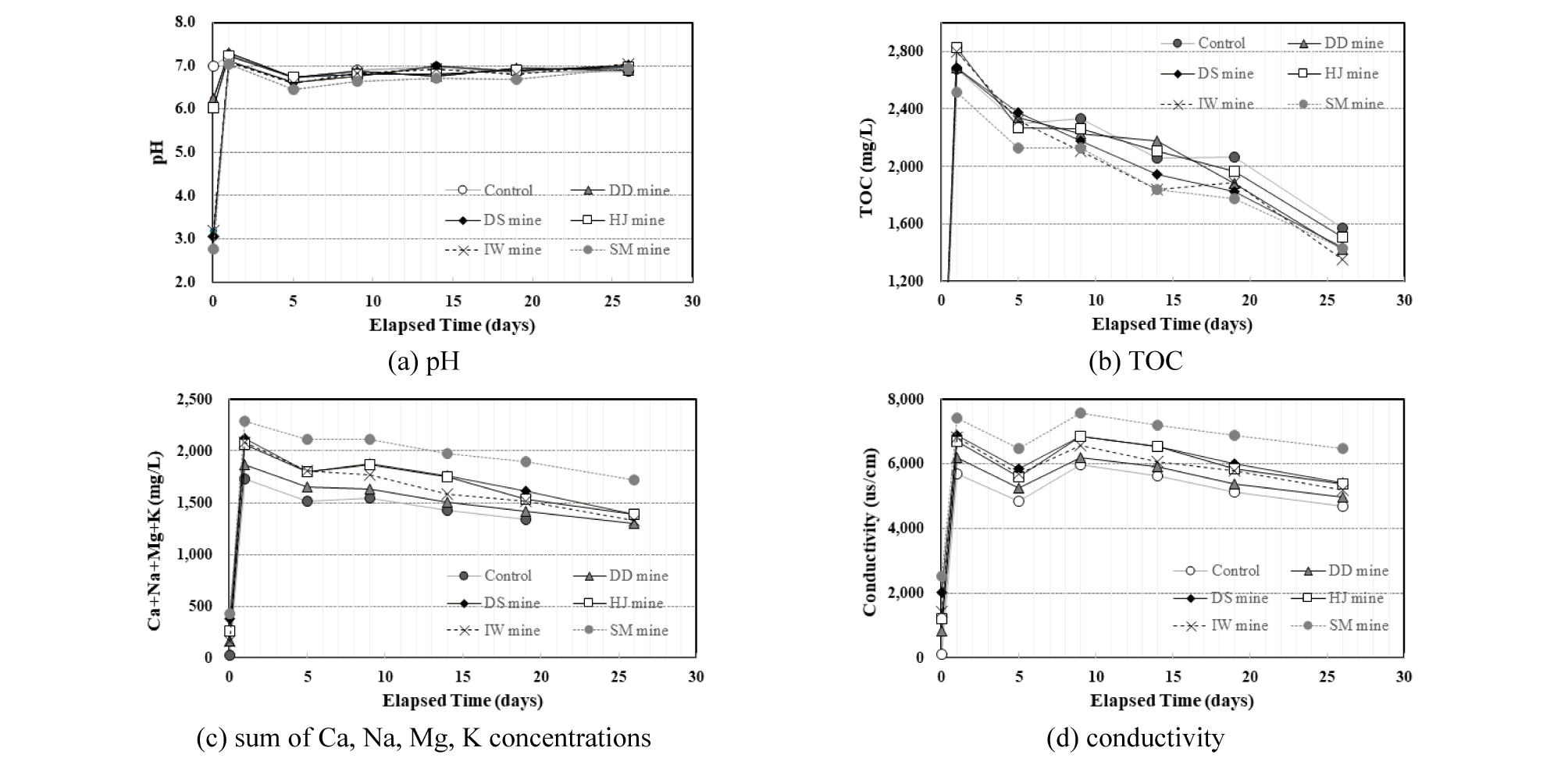
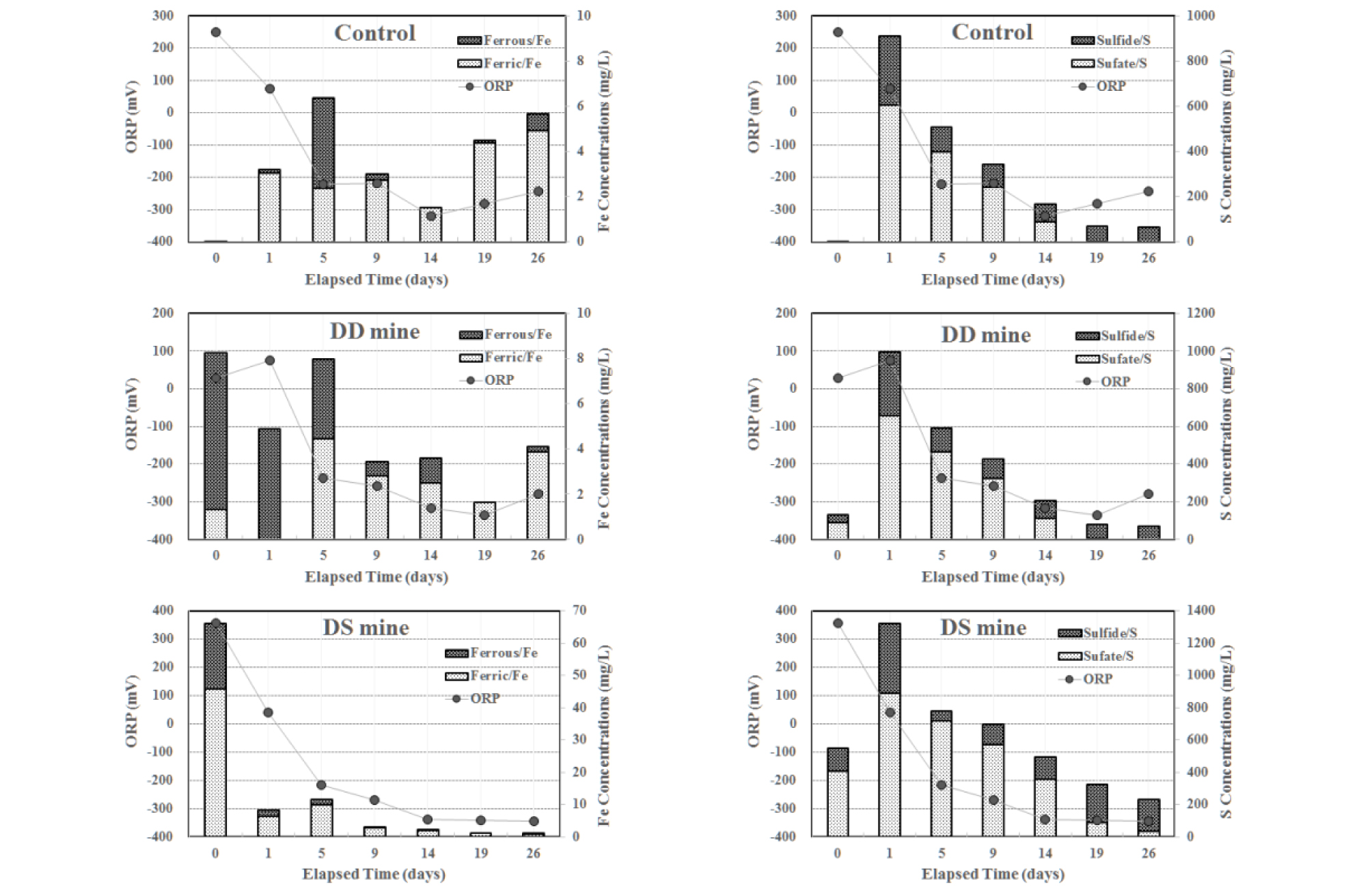
폐상퇴비가 광산배수의 지화학적 특성변화에 미치는 영향을 확인하기 위해 회분식 실험을 수행하였다. 반응 1일이 경과하자 모든 광산배수의 pH가 7.04~7.26의 범위를 나타내었고, 실험이 진행되는 동안 비교시료를 포함한 모든 광산배수의 pH가 6.8~7.2 범위를 유지하였다(Fig. 1a). 광산배수별 모든 실험조건에서 TOC는 1일 경과 후 2,500 mg/L 이상 증가하여 초기 값인 771.5 mg/L보다 높은 함량을 보였으나 시간이 경과하면서 서서히 감소하여 광산배수별로 1,300~1,500 mg/L의 농도 범위를 나타냈다(Fig. 1b). 폐상퇴비와 반응한 광산배수의 주요 양이온 원소(Ca, Mg, Na, K)는 TOC의 변화와 유사한 경향을 보였다(Fig. 1c). 전기전도도 역시 1일 경과 후 크게 증가하여 6,000~7,400 µs/cm의 범위를 보였으나 시간이 경과하면서 전기전도도는 낮아졌다. 이는 폐상퇴비에서 용출되는 주요 양이온 원소와 유기물 함량이 반영된 것으로 보인다. 광산배수가 아닌 멸균된 탈이온수를 사용한 비교시료에서도 pH, 전기전도도, TOC, 주요 양이온 농도의 변화 양상이 유사한 것으로 볼 때 폐상퇴비에서 용출되는 유기물과 무기물은 광산배수 수질변화에 영향을 미치는 것으로 판단된다(Fig. 1d). SAPS에서 폐상퇴비의 가장 중요한 역할은 Fe3+가 Fe2+로 환원되거나 Fe2+가 환원된 상태로 유지되는 것과 환원환경에서 SRB 활성에 따른 황산염 환원작용이 발생하도록 하는 것이다. 따라서 회분식 실험을 통해 산화환원전위 변화에 따른 Fe의 화학종 변화와 황산염 환원 및 총 황함량의 변화를 분석하였다. 실험결과 폐금속광 광산배수인 DD광산과 DS광산은 상이한 산도와 오염원소를 보이나 5일 경과 후 산화환원전위가 -200 mV 이하를 나타냈고, 14일 경과 후에는 -300 mV 이하의 강력한 환원환경이 조성되었다. DD광산의 경우 초기 Fe와 황산염의 함량이 낮아 비교시료와 유사한 Fe 및 황산염의 화학종 변화의 경향을 보였다. DD광산의 광산배수는 비교시료의 폐상퇴비에서 용출되는 Fe, 황산염 함량과 유사하며, Fe의 화학종 변화가 불안정하는 경향을 보였다. 또한 산화환원전위가 낮은 환원조건에서 황산염 환원 및 총 황의 함량이 감소하였다(Fig. 2).
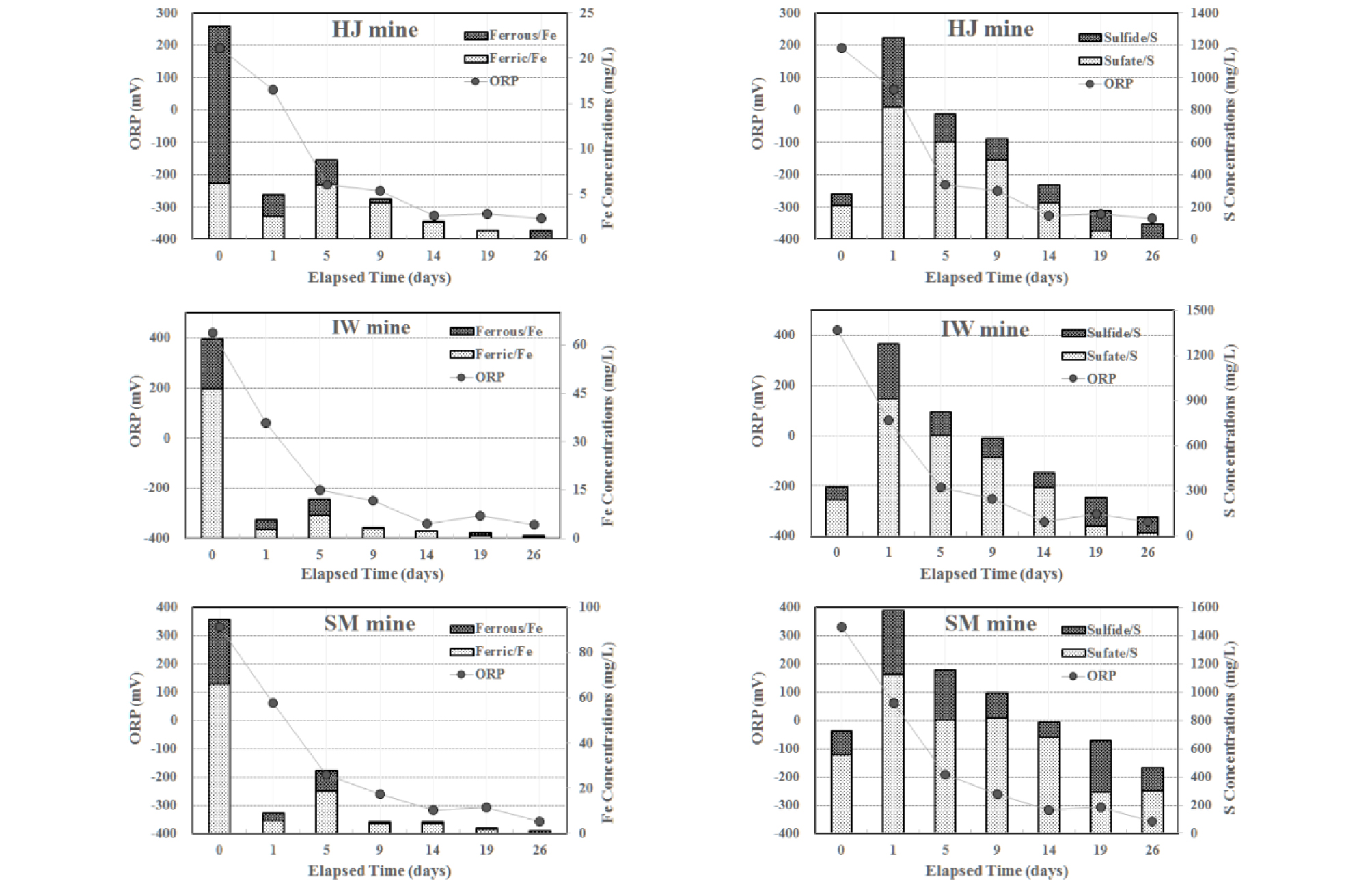
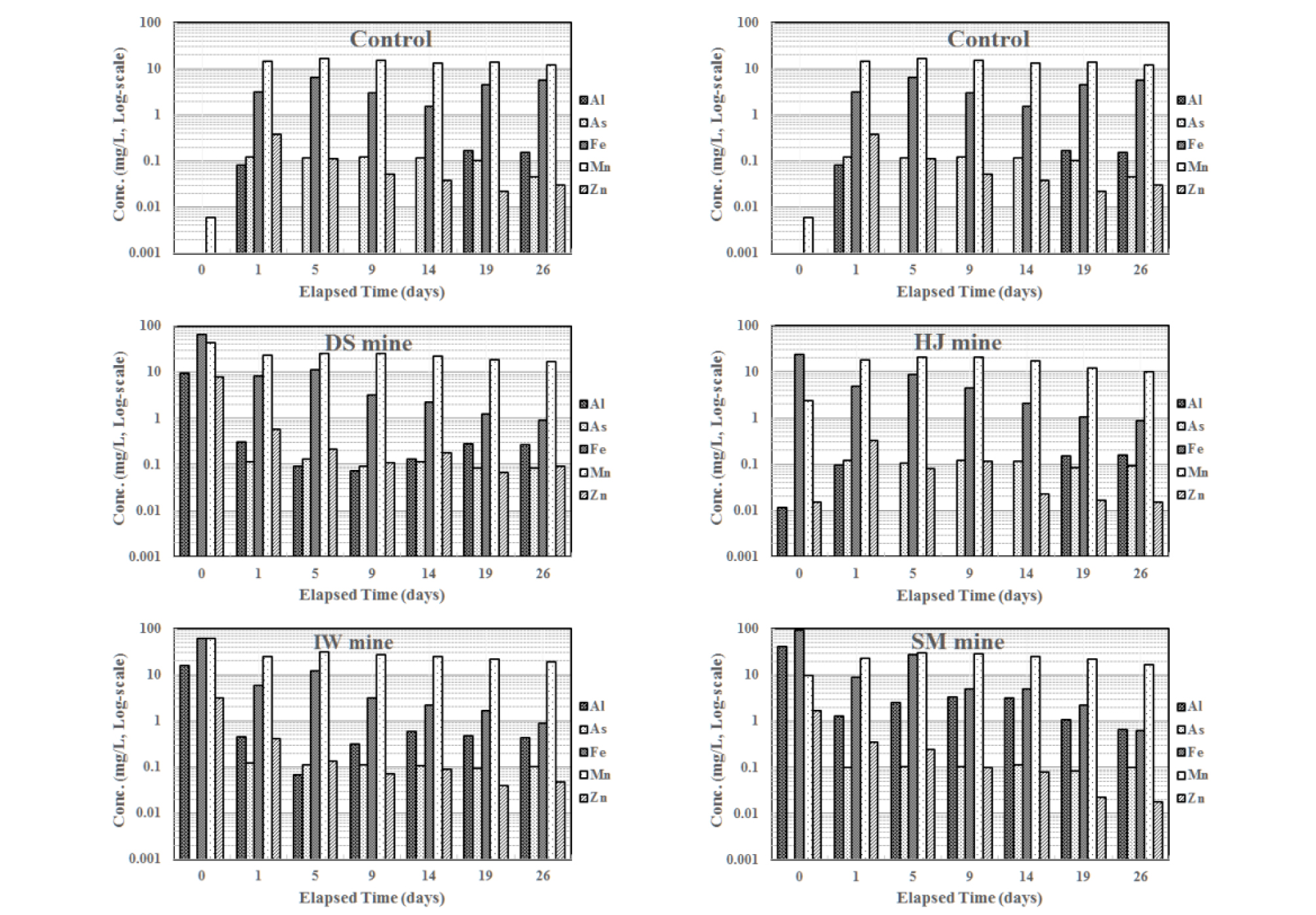
DS광산의 경우 Fe 함량이 약 65 mg/L 였으나 반응이 진행될수록 Fe가 환원되고 제거되어 1 mg/L 이하의 함량을 나타냈다. 황산염은 초기 폐상퇴비에서 2배 이상 용출되어 1일 경과 후 함량이 크게 증가하였으나 환원환경이 조성될수록 황산염 환원 및 용존된 총 황의 함량이 지속적으로 감소하였다(Fig. 2). 비교시료를 포함하여 DD광산과 DS광산은 초기 폐상퇴비에서 용출된 황산염이 19일 경과 후 대부분 환원되어 감소하고, 용존 황 중 대부분은 환원된 황(sulfide)의 형태로 존재하였다. 폐탄광 중 산도가 다른 HJ탄광, IW탄광, SM탄광의 광산배수와 유기 기질물질을 반응시켜 수질변화를 분석하였다. 광산배수별 산화환원전위를 관찰한 결과, 초기 5일 반응 후 산화환원전위는 -200 mV를 보였고, 반응이 진행될수록 지속적으로 감소하여 14일 경과 후 -300 mV 이하의 환원환경을 나타냈다. 광산배수별 초기 다른 Fe 함량에도 불구하고 9일 경과 후 모든 광산배수에서 Fe의 환원과 제거가 발생하여 5 mg/L 이하의 함량을 보였고, 19일 경과 후에는 1 mg/L 이하로 낮아졌다(Fig. 3). 초기 황산염 함량이 유사한 HJ탄광과 IW탄광의 경우 황산염 환원 및 총 황의 제거양상이 유사하였고, 다른 금속광산 시료와 유사하게 19일 경과 후 용존 황의 대부분이 환원된 황의 형태를 보였고 황산염의 함량이 상대적으로 낮게 나타났다. 반면 초기 황산염의 함량이 높고, 산도와 ORP가 높은 SM탄광의 경우 -300 mV 이하의 환원환경이 조성되더라도 용존된 황산염이 1,000 mg/L 이상 존재하고, 용존된 총 황 중 황산염의 함량이 환원된 황(sulfide)보다 약 2배 높게 나타났다(Fig. 3). 또한 SM에서는 19일의 반응시간 경과에도 초기 용존된 총 황의 60%가 용존상태로 잔류하였다. 수질특성이 다른 광산배수와 유기 기질물질과의 반응에 따른 Al, As, Fe, Mn, Zn의 함량변화를 분석하였다. 멸균된 탈이온수 400 mL와 폐상퇴비 100 g을 반응시킨 비교시료에서 1일 경과 후 용출되는 오염원소의 함량은 각각 Al 0.08 mg/L, As 0.12 mg/L, Fe 3.18 mg/L, Mn 14.46 mg/L, Zn 0.37 mg/L로, 4개의 주요 양이온(Na, K, Mg, Ca)과 As, Mn, Fe의 용출이 두드러지게 나타났다(Fig. 4). 그러나 시간이 경과함에 따라 Fe와 Mn를 제외한 오염 원소들은 상대적으로 감소하는 경향을 보이고, 특히 반응초기 1,800 mg/L까지 용출된 황산염의 함량은 19일 후 2 mg/L 이하까지 감소하였다. 비교시료에서 초기 반응용액에 부가된 용존 원소들은 유기 기질물질의 제조과정에서 첨가되는 원료물질에 의한 것으로 보이고, 특히 As는 가축이나 가금류의 분뇨에 일정농도 이상 포함되어 있는 것으로 알려져 있어 퇴비에 첨가되는 계분으로부터 기원될 가능성이 있다(Yao et al., 2009).
초기 비교시료에 용출되는 오염원소는 각각의 회분식 실험 중 광산배수에 오염원소를 부가시키는 경향을 보이나 반응 초기 pH 완충작용과 환원환경이 조성된 이후에는 비교시료와 오염원소의 함량 차이가 크지 않았다. DD광산의 경우 1일 경과 후 초기 광산배수의 As 함량은 0.42 mg/L로 다른 시료에 비해 0.3 mg/L 정도 높게 나타나지만 반응이 종료된 시점에서는 0.14 mg/L로 감소하였다. 광산배수 내 초기 Mn의 농도가 높은 DD광산, IW탄광, SM탄광은 상대적으로 반응 초기 Mn 함량이 높지만 점가 감소하는 경향을 보였다. 반면 DS광산과 IW탄광에 비교적 높은 농도로 존재하는 Zn과 공통의 오염원소인 Fe, Al은 반응초기부터 감소하였다(Fig. 4).
As와 Mn은 환원환경이 조성될수록 As3+와 Mn2+로 존재하여 지구화학적 이동도가 높고, SRB가 존재하는 황산염 환원 조건에서 때때로 황화물로 침전되기도 하지만 용해도적이 낮거나 높은 이동도로 인해 안정적인 화합물로서의 침전 및 제거가 어려운 특성이 있다. 반면 Fe, Al, Cu, Zn은 중성의 pH 조건과 황산염 환원 조건에서 금속 (수)산화물 또는 황화물로 쉽게 침전 및 제거될 가능성이 크다(Jong and Parry, 2004; Sheoran et al., 2010; Ziemkiewicz et al., 2003).
자연정화공법의 단위공정인 SAPS는 유기 기질물질로 폐상퇴비를 사용하고 있고, 초기 다량의 유기탄소와 Ca, Mg, Na, K, SO42- 등의 주요 무기원소를 용출시켜 전기전도도 및 총용존고형물(TDS)을 높이는 특징이 있다. 또한 Fe, Mn 등의 오염원소가 용출되기도 하지만 시간이 경과하면서 이러한 물질들은 소모되거나 감소하는 경향을 보이고, 유기탄소와 무기원소가 일정하게 용출되는 단계에 이르게 된다. 이는 실제 실규모의 현장이나 연속식 컬럼실험에서도 유사한 경향을 보이는 것으로 조사되었다(Park et al. 2016).
SAPS에서 유기 기질물질이 pH 완충 및 무기산도를 저감하고, 환원조건 또는 황산염 환원 환경을 조성하기 위해서는 수질특성, 체류시간, 온도 등의 조건이 충족되어야 한다. 실험결과에도 나타났듯이 무기산도가 높고 Fe3+의 비율이 높은(즉, ORP에 따른 강한 산화조건일 경우) 산성광산배수(SM탄광)에서는 환원환경이 조성되더라도 황산염 환원이 더디게 발생할 수 있다. 또한 SAPS에서 유기 기질물질 층과 석회석 층의 부피비는 약 0.3 : 1로 석회석 층에서 광산배수가 24시간 체류한다고 가정할 때 유기물 층에서는 약 5~6시간 체류하게 된다. 생물반응기에서 SRB의 활성화를 위해 혼합 기질물질에서 적정 체류시간을 2~3일로 설계하기 때문에 SAPS 유기 기질물질 층의 체류시간은 상대적으로 매우 적은 편이다. 따라서 산화환원전위가 높거나 산도 300 CaCO3 mg/L의 고산도 광산배수가 연속적으로 유입될 경우 유기 기질물질 층의 고유 기능을 유지하기 어려울 것으로 예상된다. 현재 운영 중인 자연정화시설 SAPS의 유기 기질물질 층에서 SRB에 의한 황산염 환원반응을 명확히 관찰하기 어려운 이유는 유입되는 광산배수의 높은 산도, 유기 기질물질 층에서의 짧은 체류시간, 계절에 따른 온도 및 유량 변화로 설명될 수 있다(Lens et al., 2002; Logan et al., 2005). 따라서 자연정화공법 단위공정 중 SAPS를 적용할 경우 보편적인 유기 기질물질 층의 두께(0.3~0.4 m)를 수질에 관계없이 일관되게 적용할 것이 아니라, 광산배수 수질특성을 반영한 유기물 층이 설계되어야 한다. 광산배수의 산도가 높은 경우 유기 기질물질 층의 충진 높이를 조절하여 체류시간을 높이거나, 모래입도의 석회석을 유기 기질물질과 혼합하는 등 유기 기질물질의 중화능력을 부가하는 것이 고려되어야 한다(MIRECO, 2014).
결론
자연정화공법의 단위공정 중 SAPS는 광산배수의 산도(특히, 무기산도)를 제거하기 위한 공정으로, 상기하였듯이 유기 기질물질과 석회석이 층상구조로 이루어져 있다. 일반적인 SAPS의 설계는 광산배수의 산도에 따라 석회석의 알칼리 발생량을 기준으로 그 양이 결정될 뿐, 유기 기질물질은 광산배수의 수질특성과 무관하게 0.3~0.4 m의 두께로 설계된다. 석회석 층이 관산배수의 산도제거에 결정적인 역할을 하지만, 연구결과에서도 확인하였듯이 유기 기질물질 층도 산도를 완충하고, 황산염환원균 등 산화환원전위를 조정하는 미생물을 활성화시켜 오염물질을 제거하는 중요한 역할을 한다. 현장에서 운영 중인 SAPS의 유기 기질물질 층은 산도가 300 CaCO3 mg/L 이하일 경우 상기한 두께에서도 설계연한에 근접하는 효율을 보이고 있다(MIRECO, 2016). 다만 SM탄광과 같이 산화환원전위가 높고 산도가 300 CaCO3 mg/L 이상인 산성광산배수는 통상적으로 적용되는 유기 기질물질 층의 설계가 적정하지 않을 수 있다. 유기 기질물질 층에 유입되는 광산배수에 Fe3+ 등의 함량이 높은 경우, 하부 석회석 층의 알칼리 용해를 저감하기 때문이다. 따라서 SAPS의 설계에 있어 광산배수의 지구화학적 특성을 고려하여 유기 기질물질 층의 두께를 조절하거나 알칼리 물질을 혼합하는 개선 방안을 고려해야 한다.