서 론
바나듐 원소의 지화학적 특성
바나듐을 함유하는 광물
자철석
적철석
티탄철석
금홍석
2차 광물
기타
바나듐 광상의 특징
함바나듐 티타늄 자철석 광상
함바나듐 사암 광상
함바나듐 셰일 광상
바나듐산염 광상
VTM 광상의 공정광물학적 특성
바나듐 생산이 환경에 미치는 영향
결 론
서 론
바나듐은 원자번호 23번으로 주기율표에서 티타늄과 크롬 사이에 위치하는 전이금속원소이다. 바나듐은 대부분의 금속보다 단단하고 잘 부식되지 않으며 알칼리와 산에 강한 특성을 갖고 있어 철과 비철 합금의 원료로 사용된다. 또한 세라믹, 유리, 안료를 제조하는 공정에서 촉매제로 사용되는 등 쓰임새가 많은 금속이다(Kelley et al., 2005). 최근에는 화재나 폭발 위험이 없는 에너지 저장장치로서 리튬이온 배터리를 대체할 차세대 배터리로 바나듐 흐름전지(vanadium redox-flow batteries)가 주목받고 있다. 이와 관련하여 앞으로 바나듐의 수요가 더욱 확대될 것으로 예상되어 바나듐을 안정적으로 확보하기 위한 기술 개발에 관심이 모아지고 있다(Kim, 2019; Kim and Jeon, 2019).
지각에서 바나듐의 분포는 바나듐의 지화학적 특성과 밀접하게 관련된다. 지구상에 존재하는 원소는 지화학적 결합을 선호하는 특성에 따라 다음의 네 가지로 분류된다(Goldschmidt, 1937). 즉 니켈이나 코발트와 같이 철과 결합하는 친철원소(siderophile elements), 아연이나 비소와 같이 황화물을 이루는 친동원소(chalcophile elements), 질소와 같이 기체 상태로 존재하는 친기원소(atmophile elements), 희토류 원소나 스트론튬처럼 규산염 광물에 농축되는 친석원소(lithophile elements)이다. 바나듐은 친석원소이고 주로 규산염 광물의 성분으로 함유되어 있다(Huang et al., 2015). 마그마에 용존된 바나듐은 지각의 심부로부터 지표로 이동하고 풍화와 속성작용을 거치며 화성암과 퇴적암을 구성하는 광물의 성분이 된다.
바나듐은 미량이지만 어디에나 있다고 할 정도로, 지각은 물론 강, 바다, 토양, 대기 등 지구 곳곳에 존재한다. 자원으로서의 바나듐은 지각이나 지표에 위치하는 광상으로부터 얻을 수 있는데 석탄이나 석유에도 상당량 함유되어 있다(Huang et al., 2015). V3+와 V4+ 이온이 유기물과 강한 금속-유기물 복합체를 형성하기 때문이다. 광물에 존재하는 바나듐은 대부분 그 함량이 0.1%보다 적은 미량(trace)이지만 IMA(International Mineralogical Association)에서 인정한 함바나듐 광물의 수는 모두 268개나 된다. V2O5 함량이 15~40%에 이르는 바나듐산염 광석이 고갈된 이후 현재 함티타늄 자철석광은 바나듐의 주요 공급원이 되었다. 함티타늄 자철석광에서 함바나듐 광물의 종류는 크게 자철석-적철석, 자철석-티탄철석 또는 적철석-금홍석의 3가지 광물 조합으로 나타난다. 바나듐 함량이 높은 것으로 알려진 국내 함티타늄 자철석광은 자철석-티탄철석 조합이다. 자철석-티탄철석에서는 자철석 기질(matrix) 내에 티탄철석이 밴드 혹은 선상의 용리조직(exsolution texture)으로 나타나는 경우가 흔하다. 자철석-티탄철석이 수반되는 함티타늄 자철석광에서 바나듐은 일반적으로 자철석에 더 농축되어 있다(Schuiling and Feenstra, 1980).
함티타늄 자철석광의 자철석 정광에서 바나듐의 품위를 향상시키기 위해서는 자철석의 단체분리가 가능한 입도가 되도록 원광을 분쇄한 후 약한 자력을 이용하는 자력선별법을 활용한다(Lv and Bai, 2019). 함티타늄 자철석에서 맥석 광물(티타철석, 규산염 광물)이 자철석 내에 마이크로 또는 나노미터 크기의 입자로 분포하는 경우 자력선별 정광의 품위를 높이는 일은 매우 어렵다(Lv and Bai, 2019). 맥석 광물의 입자 크기가 수 µm~38 µm로 미립인 경우 물리적 선별법으로 제거하기는 어려우며, 이런 이유로 고품위 자력선별 정광이라 할지라도 Al, Mg, Si과 같은 불순물 원소의 함량이 높을 수 있다(Lv and Bai, 2019).
국내에서는 옥천과 연천 지역에 바나듐을 함유하는 자철석 광상이 분포되어 있다(Kim and Jeon, 2019). 연천 지역은 티탄철석을 함유한 자철광체가 염기성암인 반려암질 암체 내에 발달되어 있고 주로 자철석에 바나듐이 부존되어 있다(Kim et al., 1994). 본 논문에서는 바나듐 광물과 광상의 전반적인 특징을 살펴보고 특히 연천 지역 함티타늄 자철광과 같은 바나듐 광상에서 나타나는 광석 광물에 대해 고찰하고자 하였다. 선광 및 제련 공정에서 바나듐의 지화학적 특성과 함바나듐 광물의 광물화학적 특성을 어떻게 고려해야 하는지를 공정광물학적 입장에서 기술하고자 하였다.
바나듐 원소의 지화학적 특성
지각에서 바나듐 원소의 평균 함량은 138 ppm(Rudnick and Gao, 2005)으로 이는 아연, 니켈과 유사한 농도이다(Reimann and Caritat, 1998). 상부 지각에서의 바나듐 함량은 이보다 낮은 약 7 ppm으로 알려져 있다(Rudnick and Gao, 2005). 한편 지각 내 바나듐 원소의 함량은 암석의 종류에 따라서 큰 차이를 나타낸다. 초염기성 화성암에서 바나듐의 함량은 약 40~50 ppm, 화강암과 같은 규장질 암석에서는 약 60 ppm, 현무암 또는 염기성 화성암에서는 약 250 ppm이다(Mielke, 1979). 즉 규장질과 초염기성 암석에서보다는 염기성 암석에서 바나듐의 함량이 높게 나타난다. 실리카의 함량이 매우 낮고 90% 이상이 염기성 광물로 이루어진 초염기성 암석보다는 바나듐을 함유하는 규산염 광물과 염기성 광물이 다양하게 포함된 염기성 암석에서 바나듐의 함량이 높은 것이다.
바나듐은 해수, 토양, 빗물, 지각, 맨틀 등에 존재하며 거의 모든 지화학적 과정에 관여하기 때문에 지구의 내부와 지표에서 일어나는 여러 현상과 관련이 있다(Huang et al., 2015). 이렇게 다양한 지화학적 환경에 존재하는 바나듐은 산화-환원 환경변화에 민감하기 때문에 산소 분압(oxygen fugacity)을 지시하는 추적자로 사용된다(Lee et al., 2013). 한 계의 산소 분압은 지구 시스템에서의 산화 환원전위를 결정하는 근본적인 열역학적 변수이다.
+3, +4, +5가의 바나듐은 조암광물의 격자에 존재하는 Fe3+ 또는 Al3+, Ti4+, P5+를 치환한다(Liu et al., 2018). V3+의 이온 반경은 64 pm로 Fe3+의 69 pm(high spin), Al3+의 68 pm과 비슷하기 때문에 많은 조암광물의 8면체 자리 양이온을 쉽게 치환할 수 있다(Liu et al., 2018). V5+는 수소, 알칼리, 알칼리토금속 및 +2가 전이금속과 결합해 화합물을 만드는 경향이 있다(Liu et al., 2018). 황과 인을 포함하는 화합물에서는 +4가의 산화상태를 가지며 퇴적암에 함유된 황산염 또는 인산염 광물의 성분으로 존재한다. 바나듐은 풍화과정을 겪으면서 원래 존재하던 광물로부터 풍화 산물, 즉 녹니석, 일라이트 또는 카올린 광물과 같은 점토광물로 재분배된다(Habteselassie et al., 1996).
앞에서 밝혔듯이 바나듐은 유기물과 복합체를 잘 만들기 때문에 유기물이 풍부한 퇴적물에 농집되는 경향이 있다. 셰일에서 바나듐의 평균 함량은 130~205 ppm(Kelley et al., 2005)이지만 탄질 또는 흑색 셰일의 경우 16,000 ppm (Breit and Wanty, 1991)까지 함유된 경우도 있다. 석유나 타르 샌드, 석탄 등에서도 바나듐 함량이 높게 나타난다. 탄질 셰일에 함유된 바나듐은 해수에 용해된 바나듐산염이 바나딜(vanadyl) 이온이나 H2S에 의해 환원된 후 퇴적물 입자에 흡착되어 침전, 퇴적된 것이다(Breit and Wanty, 1991). 이후 바나듐-유기물 화합물은 속성작용을 거치며 대부분 점토광물이나 가수분해가 잘되지 않는 불용성의 유기물질(refractory organic matter)의 성분으로 존재하게 된다(Breit and Wanty, 1991).
광물에 함유된 바나듐은 대부분 +3가이기 때문에 잘 용해되지 않아서 열수에 녹아 이동되는 양이 극히 적다(Kelley et al., 2005). 결과적으로 광상의 한 종류인 열수광상에서는 바나듐의 함량이 낮아서 경제성을 기대하기 어렵다. 풍화과정을 거쳐 점토광물로 이동된 바나듐의 산화상태는 +3가이거나 +4가인데, 이 역시 잘 용해되지 않는다(Kelley et al., 2005). 따라서 침식과 화학적 풍화가 심한 환경에서 생성되는 보크사이트와 라테라이트에서 바나듐이 상당히 농축될 수 있는 것이다(Kelley et al., 2005).
바나듐을 함유하는 광물
바나듐은 흔히 광물의 미량 성분으로 함유되어 있지만 함바나듐 광물의 수는 200개가 넘을 정도로 많은 편이다(Liu et al., 2018). 이는 바나듐이 4가지의 안정된 산화상태(+2가, +3가, +4가, +5가)를 가질 수 있어 광물격자 내에서 다양한 이온(Fe3+, Al3+, Ti4+, P5+ )을 치환할 수 있기 때문이다(Liu et al., 2018). 또한 Eh 및 pH의 변화에 따라 바나듐의 용해도와 바나듐이 다른 원소와 결합하는 방식이 다양하기 때문에(Taylor and van Staden, 1994) 미량 원소임에도 불구하고 많은 광물에 함유될 수 있다. 즉 광물학적으로 볼 때 바나듐은 광물 내에서의 함랑은 낮지만 상당히 흔한 원소라고 할 수 있다.
산화광물과 규산염광물에 함유된 바나듐은 +2가부터 +5가까지의 산화상태로 존재한다(Shearer et al., 2006). 음이온으로 VO43-나 V2O74- 이온을 함유한 바나듐산염 광물에서 바나듐의 산화상태는 +5가이다. 바나듐산염 광물로는 모트라마이트(mottramite, PbCu(VO4)(OH)), 데스크로이자이트(descloizite, PbZn(VO4)(OH)), 바나디나이트(vanadinite, Pb5(VO4)3Cl) 등이 있지만 자연에서 매우 드물고 남아프리카 지역에 분포되었었지만 현재는 고갈된 것으로 알려져 있다(Huang et al., 2015). 광물에서 바나듐이 가장 흔하게 치환하는 원소는 철과 알루미늄이다(Huang et al., 2015). 바나듐을 함유하는 광물은 광물의 분류 상 산화광물, 수산화광물, 규산염 광물, 그리고 황화광물에 해당하는데(Table 1) 바나듐이 철과 마그네슘, 티타늄을 치환하기 때문에 함바나듐 광물은 규소 함량이 높은 규장질 암석보다는 고철질 암석에서 더 흔하다. 따라서 철과 티타늄으로만 구성된 함티타늄 자철석에는 다른 광물보다 상대적으로 바나듐이 농축되어 있다(Table 2). 티탄철석이나 자철석뿐만 아니라 맥석광물인 휘석, 석류석, 첨정석 등에서도 바나듐이 존재할 수 있다(Table 3). 이는 바나듐이 이들 광물의 성분인 Fe, Al, Cr 등을 치환하기 때문이다. 한편 바나듐은 우라늄과 화학적 친화도(chemical affinity)가 높기 때문에 함바나듐 광물에 우라늄이 동반되는 경우가 있다. 쿠리에나이트(curienite), 모트라마이트(mottramite) 등이 이에 해당된다(Table 1).
Table 1.
Selected vanadium-bearing minerals with ideal stoichiometric formula (Kelley et al., 2005)
| *VTM deposits | Shale-hosted V deposits | ||
| Coulsonite | (Fe,V)3O4 | Illite-smectite | K0.8(Al2.8Mg0.5Fe0.4V0.3) |
| Hematite | Fe2O3 | (Si7.2Al0.8))20(OH)4 | |
| Ilmenite | FeTiO3 | Metahewettite | CaV6O16H2O |
| Magnetite | Fe3O4 | Patronite | V4+(S22-)2 |
| Perovskite | CaTiO3 | ||
| Rutile | TiO2 | ||
| §SSV deposits | Vanadate deposits | ||
| Carnotite | K2(UO2)2(VO8)・1-3H2O | Brachebuschite | Pb2(Mn,Fe)(VO4)2・H2O |
| Coffinite | U(SiO4)1-x(OH)4x | Calciovolborthite | CaCuVO4(OH) |
| Corvusite | (Na,Ca,K)V8O2・4H2O | Chervetite | Pb2V2O7 |
| Doloresite | H8V6O16 | Curienite | Pb(UO2)2(VO4)2・5H2O |
| Hewettite | CaV65+O16・9H2O | Descloizite | PbZn(VO4)(OH) |
| Montroseite | (V3+,Fe3+V4+)O(OH) | Francevillite | (Ba,Pb)(UO2)2(VO4)2・5H2O |
| Paramontroseite | VO2 | Heyite | Pb5Fe2(VO4)2O4 |
| Pascoite | Ca3(V10O28)・17H2O | Mottramite | PbCu(VO4)(OH) |
| Roscoelite | K(V3+,Al,Mg)[(Si,Al)4O10](OH)2 | Mounanaite | PbFe2(VO4)2(OH) |
| Tyuyamunite | Ca(UO2)2V2O8・5-8H2O | Pyrobelonite | PbMnVO4(OH) |
| Uraninite | UO2 (with Pb,Th,V,Zr) | Sengierite | Cu(UO2)2(VO4)2・8or10H2O |
| Vanadium clays | V-bearing hydrous mica | Turanite | Cu5(VO4)2(OH)4 |
| Vanadian chlorite | V-bearing chlorite | Vanadinite | Pb5(VO4)3Cl |
| Volborthite | Cu3V2O7(OH)2・2H2O | Volborthite | Cu3(VO4)2・3H2O |
Table 2.
Selected vanadium-bearing minerals in VTM deposits(Anthony et al., 2003)
Table 3.
Main gangue minerals in VTM deposits(Krivolutskaya and Bryanchaninova, 2011; Moon, 1996)
지표면 또는 지표 가까이에서 풍화작용을 받아 분해, 이동된 후 퇴적되어 속성과정을 거쳐 새롭게 생성된 광물을 2차 광물이라고 한다. 바나듐은 운모, 스멕타이트, 일라이트, 카올리나이트, 녹니석과 같은 2차 광물 격자 내의 양이온을 치환하여 이들 광물의 성분으로 존재한다. 이 외에 철-망간 가수산화물에 부존되거나 유기물과 강하게 결합하여 원유와 석탄, 탄질 셰일에도 농축될 수 있다(Clark, 1993).
바나듐이 다양한 산화상태를 갖는 만큼 광물 구조 내에서 여러 종류의 배위다면체를 형성하는 것으로 알려져 있다. 즉 음이온에 의해 4배위, 5배위, 8배위되는 화학결합이 가능하다(Huang et al., 2015). 광물 내에서 바나듐의 정확한 산화상태는 X-선 광전자 분광법(X-ray photoelectron spectroscopy, XPS), XANES(X-ray absorption near edge spectroscopy), 분광광도법(Spectrophotometry) 등으로 측정하여 결정할 수 있다.
자철석
자철석은 등축정계에 속하고 흔히 정팔면체나 정십이면체의 자형을 이룬다(Klein and Dutrow, 2007). 자형을 갖추고 있지 않을 때는 괴상이나 세립질로 나타난다. 모스 경도계 6의 굳기를 가지며 비중은 5.18이다(Klein and Dutrow, 2007). 이론적인 화학구조식은 Fe3O4인데 철을 함유하는 모든 광물에서 유일하게 자철석에만 Fe2+와 Fe3+가 동시에 존재한다. 자철석은 역첨정석(inverse spinel) 구조를 갖고 있기 때문에 결정구조식은 Fe3+(Fe2+, Fe3+)2O4로도 표현된다. 즉 Fe3+ 이온의 절반은 사면체 양이온 자리를, 나머지 반과 Fe2+ 이온은 팔면체 양이온 자리를 차지한다(Fig. 1, Klein and Dutrow, 2007). 자철석에 존재하는 불순물로는 팔면체 자리의 Fe2+ 이온을 치환하는 마그네슘과 망간(Mn2+), Fe3+를 치환하는 알루미늄, 크롬, 망간(Mn3+), 티타늄, 바나듐 이온이 있다(Table 2; Klein and Dutrow, 2007). 자철석에 존재하는 바나듐은 대개 사면체 자리의 Fe3+를 치환하는 V3+이지만 팔면체 자리를 V3+와 V4+가 채우기도 한다(Balan et al., 2006).

Fig. 1
Crystal structure of magnetite (Dvoryankina and Pinsker, 1962). Half of Fe3+ ions in magnetite occupy tetrahedral cation sites (Fetetra), and the other half and Fe2+ ions occupy octahedral cation sites (Feoct). Red balls present oxygens. VESTA 3 was used for visualizing the crystal structure of magnetite (Momma and Izumi, 2011).
자철석은 600°C 이상의 온도에서 울보스피넬(ulvöspinel, Fe2TiO4)과 완전 고용체를 이룬다고 알려져 있다(Fig. 2; Klein and Dutrow, 2007). 울보스피넬은 Ti4+가 Fe3+를 치환할 때 전기적 중성을 이루기 위해 격자 내에 Fe2+가 증가된 결정구조를 갖는다. 자철석과 울보스피넬 사이의 화학조성을 보이는 광물을 티타늄 자철석(titanomagnetite)이라고 하고 결정구조식으로는 (Fe3-xTixO4)으로 나타내지만 티타늄 자철석은 광물분류에 의한 정식 광물명은 아니다.
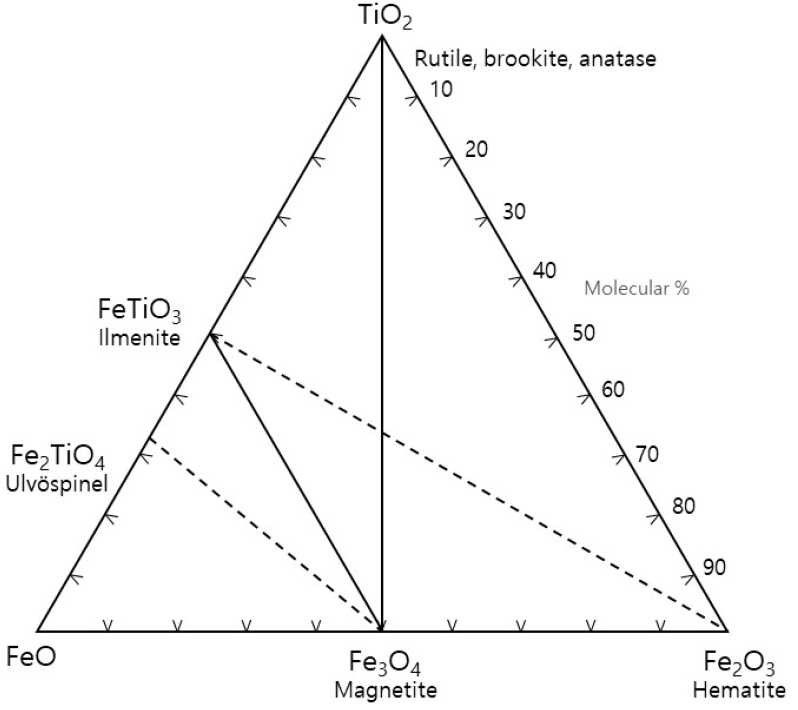
Fig. 2
Solid solution series and their extent among oxides in the system TiO2-FeO-Fe2O3 (Klein and Dutrow, 2007). Dashed lines indicate complete solid solution between end members.
티타늄을 함유하는 자철석은 마그마가 식으며 결정화가 일어나는 과정에서 티탄철석과 용리 조직을 이루는 경우가 흔하다(Fig. 3). 용리는 고온에서 균질한 고용체를 이루던 물질이 계 내에 물질의 첨가나 제거를 수반하지 않고 두 개 이상의 서로 다른 결정질 물질로 분리되는 현상을 말한다(Moon and Choi, 2001). 이러한 용리조직은 자철석 정광의 품위를 어느 수준 이상으로 올리기 어려운 원인이 되는데 얇은 선상의 용리엽(exsolution lamellae)이 나노미터 두께로 존재할 수도 있기 때문이다. 풍화받은 함티타늄 자철석의 경우 미립의 2차 광물이 자철석과 복잡한 조직을 이루고 있어서 자철석 정광의 품위를 향상시키기는 쉽지 않다(Xu et al., 2017).
적철석
철의 광석인 적철석의 이상적인 결정구조식은 Fe2O3이며 철은 +3가로만 존재한다. 적철석의 결정구조는 티탄철석, 강옥(corundum)의 결정구조와 동일하다. 적철석의 모스경도계 굳기는 5.5-6.5이고 비중은 5.26으로 자철석보다 다소 무겁다(Klein and Dutrow, 2007). 육방정계에 속하며 적철석의 자형은 판상이며 패각상 또는 괴상의 외형으로도 나타난다(Klein and Dutrow, 2007). 적철석은 고온에서 티탄철석과 완전 고용체를 이룬다(Fig. 2; Anthony et al., 2003). 적철석에서 바나듐의 함량이 증가하면 격자상수 중에서도 α각과 c의 변화가 상대적으로 커진다(Chernikov et al., 2005). 적철석에서 Fe3+ 이온의 자리는 자철석에서 Fe3+ 이온이 차지할 수 있는 자리의 1.5배나 많지만(Schuiling and Feenstra, 1980) 적철석과 자철석이 존재할 때 예외 없이 바나듐은 자철석에 더 농축된다고 알려져 있다(Schuiling and Feenstra, 1980). 적철석은 자철석에 비해 불순물 원소의 종류가 적은데 불순물로는 망간이 가장 흔하다(Table 2).
티탄철석
티탄철석은 화성암과 변성암에서 흔한 부구성 광물(accessory mineral)이다. 티탄철석의 결정구조식은 FeTiO3이 아닌 (Fe, Mg, Mn)TiO3이 더 적합하다고 할 정도로 Mg과 Mn은 매우 흔한 불순물 원소이다(Klein and Dutrow, 2007). 티탄철석은 가이키에라이트(geikielite, MgTiO3), 파이로패나이트(pyrophanite, MnTiO3)와 고용체를 형성하기 때문에 티탄철석에서 Mg와 Mn의 함량은 다양하다(Klein and Dutrow, 2007). 티탄철석에는 Mg, Mn 이외에 Si, Al, V, Cr 등이 불순물로 함유될 수 있는데 Mg와 Mn을 제외하면 함량이 매우 낮은 편이다(Table 2). Mg와 Mn은 주로 Fe2+ 이온을, V3+ 또는 V4+ 이온은 Ti4+ 이온을 치환한다(Mehdilo et al., 2015). 적철석과 마찬가지로 티탄철석의 결정구조는 강옥과 동일하게 Fe-O, Ti-O 팔면체가 c 축에 수직인 방향으로 서로 번갈아 위치한다. 이러한 연결성으로 인해 자형은 두꺼운 판상이나 능면체로 나타나지만 과립이나 괴상으로도 나타난다.
티탄철석은 고철질 화성암에서는 흔히 자철석과 공정(intergrowth) 관계이거나 적철석과 완전 고용체를 이룬다. 티탄철석은 흔히 자철석이나 적철석 내에 다양한 두께의 용리엽으로 나타난다(Klein and Dutrow, 2007). 용리엽의 두께는 암석의 냉각속도와 관련되는데 냉각이 빠르게 진행되었다면 용리엽의 두께는 얇게 나타난다. Fig. 3은 연천지역 함티타늄 자철석 입자의 후방산란전자 영상으로 저배율에서는 용리엽이 구분되지 않지만(Fig. 3(a)) 배율을 올리면 어두운 선으로 나타나는 용리엽이 구분되고(Fig. 3(b)) 자철석 입자 내부에 철과 티타늄의 분포로도 티탄철석의 존재를 확인할 수 있다.
금홍석
금홍석의 결정구조식은 TiO2로 다구조형인 브루카이트(brookite), 아나타제(anatase) 중에서 가장 흔한 광물이다. 고온, 고압의 변성암과 화성암에서 흔히 나타나는 부구성 광물이다. 철과 니오븀, 탄탈륨, 바나듐을 불순물로 함유한다(Table 2). 금홍석은 육방최밀격자 구조로 티타늄이 팔면체 자리의 절반을 차지하고 있다(Klein and Dutrow, 2007). 티타늄 팔면체가 c축 방향으로 체인을 형성하고 팔면체의 꼭지점을 공유하여 교차결합하기 때문에 c축 방향을 따라 긴 프리즘 또는 침상의 결정으로 산출되는 경우가 흔하다(Klein and Dutrow, 2007). Liu et al.(2014)은 마그마와 금홍석 사이의 바나듐 분배 관계 연구를 통해 바나듐이 금홍석에 불순물로 포함되는 경우 V4+>V3+>V5+의 순서로 선호된다고 추론하였다. 이온반경과 전하 측면에서도 V4+는 Ti4+와 가장 가깝고 Ti4+과 V3+의 이온 반경 차이는 3.5 pm, Ti4+과 V5+의 이온 반경 차이는 6.5 pm으로 가장 크다(Blundy and Wood, 2003).
2차 광물
풍화, 속성작용에 의해 생성된 2차 퇴적광물에는 다양한 함량의 바나듐을 함유하는 광물이 있다(Huang et al., 2015). 예로서 운모, 스멕타이트, 일라이트, 카올린과 같은 점토광물, 철-망간 함수 산화물을 들 수 있다(Huang et al., 2015). 탄질 셰일에서 바나듐이 탄질물과 점토광물, 쇄설성 입자에 얼만큼의 농도로 분포되어 있는지는 연속추출법을 이용하여 간접적으로 추론할 수 있다(Zhang et al., 2015).
기타
광물은 아니지만 정유 공정의 부산물로부터 바나듐을 얻을 수 있으며 오일 셰일, 석탄, 타르샌드 등도 바나듐의 공급원으로 알려져 있다. 또한 석유화학 공정에서 배출되는 폐촉매에서 회수될 수도 있지만 그 양은 극히 일부에 지나지 않는다(Taylor et al., 2006).
바나듐 광상의 특징
바나듐은 광물의 주원소가 아닌 미량원소로 존재하기 때문에 바나듐 광상이라는 용어는 바나듐이 주성분인 광물이 농축된 곳을 의미하지 않는다. 현재 바나듐은 다른 금속을 회수하는 공정에서 나오는 부산물로부터 회수, 생산되기 때문이다. 예를 들어 함티탄늄 자철석은 철의 광석이며 제강 공정 중 배출되는 선철(pig iron)에는 바나듐이 함유되어 있어 바나듐을 회수할 수 있으므로 이를 바나듐 광상이라고 지칭하는 것이다. 우라늄 생산 공정의 부산물로부터 바나듐이 생산되는 경우도 이에 해당된다(Moskalyk and Alfantazi, 2003). 한편 바나듐 광상으로 분류되는 함바나듐 사암과 탄질 셰일은 바나듐을 함유한 광물을 포함하고는 있지만 바나듐을 회수하기에는 환경적, 경제적 부담이 있어 광상이라고 보기에는 부족한 면이 있다.
바나듐을 회수할 수 있는 광상으로 함바나듐 티타늄 자철석(vanadiferous titanomagnetite, VTM), 함바나듐 사암(sandstone-hosted vanadium, SSV), 함바나듐 셰일(shale- hosted vanadium), 그리고 바나듐산염(vanadate) 광상을 들 수 있다(Table 1; Kelley et al., 2005). VTM 광상은 현재 세계적으로 바나듐을 생산하는 대표적인 바나듐 공급원이라 할 수 있으며 대규모의 상업적인 생산이 이루어지고 있다. VTM 광상에서 바나듐을 함유하는 광물은 주로 자철석으로 알려져 있으나 이 외에 티탄철석, 적철석이나 페로브스카이트, 금혹석 등도 VTM 광상에서 바나듐을 함유할 수 있는 광물로 알려져 있다(Table 2; Fischer, 1975).
함바나듐 티타늄 자철석 광상
VTM 광상은 세계적으로 고르게 분포되어 있으며 전 세계 바나듐 수요의 80-85%가 VTM 광상과 제강 슬래그로부터 생산된다(Kelley et al., 2005; Schulz et al., 2018). 대표적인 VTM 광상으로는 남아프리카공화국의 Bushveld Complex와 중국의 Sichuan Province, 호주의 Windimurra complex, 캐나다의 Lac Doré Complex 등이 있다. 광체는 괴상 또는 광염상(disseminated)을 이루고 있는데 괴상 광체의 경우 80% 이상의 함티타늄 자철석 외에 다양한 함량의 단사휘석, 감람석, 사장석으로 구성된다(Zhou et al., 2005; Rohrmann, 1985; Eales and Cawthorn, 1996). 광염상 광체의 경우 약 50%의 자철석, 20%의 단사휘석, 20%의 사장석, 10%의 티탄철석과 소량의 감람석으로 구성된다(Zhou et al., 2005; Rohrmann, 1985; Eales and Cawthorn, 1996).
현재까지 알려져 있는 대규모의 VTM 광상에서 바나듐을 함유하는 광석광물의 종류와 지구조적 특징은 서로 매우 유사한 것이 특징이다(Kelley et al., 2005). 이러한 광상들에서 광체는 수평 방향으로 잘 연장되어 있고 두꺼운 층상의 형태를 보이는데 렌즈상으로 나타나기도 하고 복잡한 관입 양상을 보이기도 한다. VTM 광상은 주로 철질~고철질 화성암에 배태되는데 모암으로는 사장암(anorthosite)과 반려암(gabbro)이 가장 흔하다.
VTM 광상에서 바나듐은 대개 자철석(Fe2+Fe3+2O4)-울보스피넬(ulvöspinel, TiFe2+2O4) 고용체에 농축되어 있는데 V3+ 이온이 자철석의 Fe3+를 치환하기 때문이다(Table 1). VTM 광상에서 자철석에 흔히 수반되는 광물은 티탄철석, 적철석, 금홍석, 페로브스카이트(perovskite)이다(Table 2). 이들 광물들은 용리나 미립의 공정 또는 고용체로 나타난다. 바나듐을 함유하는 화성암은 크롬, 구리, 니켈 또는 백금족 금속을 함유하는 경우가 많다(Cawthorn et al., 2002).
함바나듐 사암 광상
우라늄이 배태된 사암은 전 세계적으로 분포하는데, 바나듐은 우라늄과 함께 농축되어 있는 것으로 알려져 있다(Dahlkamp, 2010). 미국의 경우 특히 콜로라도 고원지역 함우라늄 SSV 광상에서 바나듐이 생산되고 있다(Kelley et al., 2005). SSV 광상에서 바나듐의 품위는 흔히 V2O5 1% 이상으로 알려져 있는데 바나듐:우라늄의 비율은 지역에 따라 다양하다. 바나듐과 우라늄이 농축된 부분은 대개 검게 보이고 코피나이트(coffinite), 몬트로사이트(montroseite), 우라니나이트(uraninite), 함바나듐 규산염 광물이 분포된다(Table 1).
SSV 광상에서 발견되는 함바나듐 점토광물은 주로 일라이트와 녹니석인데 바나듐은 녹니석의 팔면체 배위 양이온인 알루미늄을 치환하는 것으로 알려져 있다(Meunier, 1994). 과거에는 일라이트를 운모류의 하나로 간주하였으나 엄밀히 말해 일라이트는 점토광물학계에서 만든 분류체계에는 잘 맞지 않는 점토광물이다. 일라이트는 X-선회절 분석에서 운모류와 마찬가지로 약 10Å의 저면간격을 나타내지만 사면체자리에서 알루미늄의 치환이 운모에서보다 적고 백운모와 비교하면 층간 양이온인 칼륨의 양도 적다(Moon, 1996). 함바나듐 일라이트와 함바나듐 백운모는 층전하와 팔면체 자리를 차지하는 바나듐 함량에서도 차이를 나타내는 것으로 알려져 있다(Meunier, 1994). 함바나듐 일라이트는 로스코에라이트(roscoelite)라고도 불리는데 문헌에 따라서는 함바나듐 운모류를 지칭하는 광물명으로도 사용된다.
함바나듐 셰일 광상
바나듐이 농축된 탄질 셰일은 바나듐 이외에도 은, 바륨, 코발트, 구리, 몰리브데늄, 우라늄, 아연 등 다양한 금속을 함유하는 경우가 흔하다(Kelley et al., 2005). 함바나듐 셰일은 해수에 녹아있던 바나듐이 식물성 플랑크톤의 잔해, 점토 또는 진흙과 함께 퇴적되어 오랜 기간의 물리화학적 작용을 통해 단단한 암석으로 생성된 것이다. 따라서 셰일 내 유기물의 함량이 5% 이상으로 높은데다 황철석과 같은 황화광물을 포함하기도 한다(Kelley et al., 2005).
바나듐은 주로 유기물과 자생(authigenic) 점토광물로 유입되기 때문에 탄질 셰일에서 바나듐(V4+)의 함량은 유기물의 함량과 비례하는 경향을 보인다(Breit and Wanty, 1991). 로스코에라이트와 스멕타이트, 일라이트/스멕타이트 혼합층상광물, 일라이트, 백운모 구조에 존재하는 바나듐은 +3가인데 V3+은 팔면체 자리의 양이온, 즉 Al, Fe, Mg 등을 치환한다고 알려져 있다(Gaines et al., 1997; Zhang et al., 1987; Meunier, 1994). 이는 탄질 셰일이 환원환경에서 생성되기 때문이다. 미국 인디아나주 메카쿼리 셰일(Mecca Quarry Shale)에 함유된 일라이트/스멕타이트 혼합층상광물의 경우 바나듐 함량은 1.65 wt%로, 이 값은 유기물에서의 바나듐 함량보다 훨씬 높아 바나듐이 광물에 더욱 농축된 양상을 보인다(Peacor et al., 2000).
함바나듐 셰일 광상은 바나듐의 잠재적 공급원으로 간주되긴 하지만 대체로 품위가 낮고 규모가 작아서 실제로 상업적인 규모로 개발되고 있는 곳은 거의 없다. 메카쿼리 셰일의 경우에도 바나듐의 함량은 매우 높지만 함바나듐 지층의 두께가 수 십 cm로 매우 얇아서 경제적인 가치는 없다. 앞에서 언급하였듯이 이 유형의 광상에는 다양한 중금속이 수반되는데 호주나 캐나다, 스웨덴 등에서는 니켈이나 몰리브데늄, 우라늄 등이 농축되어 있다고 알려진 광상이 있으며 실제로 중국에서는 바나듐이 아닌, 몰리브데늄과 니켈을 회수하기 위한 소규모 채굴이 있었던 것으로 알려져 있다(Kelley et al., 2005).
SSV 광상과 마찬가지로 탄질 셰일에 바나듐이 부존되는 경우는 바나듐을 함유하는 점토광물의 종류가 다양한 만큼, 바나듐이 어느 광물에 어떤 형태로 존재하는지를 정확히 이해해야 한다. 바나듐을 회수하기 위한 산 침출 공정을 사용할 경우 황화광물은 산을 소모하기 때문에 선광 공정에서는 광석광물의 품위를 높이고 황화광물의 함량을 낮추기 위한 전략을 수립해야 한다(Zhao et al., 2013). 국내에서도 이 유형의 광상에서 바나듐을 회수하기 위한 기초 연구가 수행된 바 있다(Park and Hong, 1992).
바나듐산염 광상
대부분의 바나듐산염 광물은 구리, 철, 아연 또는 납을 함유하고 있는데 이는 바나듐산염 광물이 건조한 기후 지역의 심부 산화대에 배태되는 비귀금속(base metal) 광상의 산화대에서 발견되기 때문이다(Fischer, 1975). 즉 바나듐산염 광상은 지표 가까이에 생성된 천부광상에서 풍화작용과 관련된 저온의 광화용액 등에 의해 2차적으로 생성된다(Kelley et al., 2005). 따라서 바나듐산염 광상은 셰일이나 고철질암과 같은 주변의 모암으로부터 유래된 바나듐이 농축된 것으로 보고 있다. 이러한 바나듐산염 광상은 매우 드물게 발견되고 아프리카에서는 구리-납-아연 바나듐광이 1940년대까지 가행되었던 기록이 남아있다.
VTM 광상의 공정광물학적 특성
앞에서 밝혔다시피 VTM 광상은 주로 철, 마그네슘 함량이 높은 광물로 이루어진 철질-고철질 화성암 즉, 반려암이나 사장암에 배태된다. 이런 화성암은 심부 기원이기 때문에 암층(sills)이나 병반(laccolith)처럼 두껍고 옆으로 넓게 퍼진 층상의 평평한 형태를 갖고 있다(Kelley et al., 2005). 광석 광물은 0.1~10 m 두께의 화성암 층을 관입하지 않고 평행한 층상을 이루고 있고, 곳에 따라서는 수 십m의 두께로 나타나기도 한다(Kelley et al., 2005).
VTM 광상에서 대부분의 바나듐은 자철석-울보스피넬 고용체에 농집되어 있다(Fischer, 1975). 흔하진 않지만 바나듐 함량이 높은 스피넬 광물인 쿨소나이트(coulsonite)가 자철석 내 용리조직을 보이는 경우도 있다(Balsley, 1943). 자철석에 수반되는 가장 흔한 광물은 티탄철석, 적철석, 금홍석, 페로브스카이트로 알려져 있는데 풍화를 겪으면 산화되어 바나듐 마그헤마이트(vanadomaghemite)와 적철석으로 나타나기도 한다(Rohrmann, 1985).
VTM 광상 중에서도 괴상의 Fe-Ti 산화광물에 어떻게 바나듐이 농집되는지는 명확하지 않다. 단지 맨틀 암석의 부분 용융과 이 마그마에서 일어나는 광범위한 결정분화 작용이 바나듐 농집 초기에 중요했을 것으로 추론하고 있다(Kelley et al., 1985). 바나듐이 농집된 화성암에서는 흔히 Cr, Cu, Ni과 백금족 원소가 동반된다(Naldrett, 2010; Zientek, 2012).
서호주 윈디뮤라 복합체(Windimurra complex)는 고온 건조한 환경에서 풍화가 상당히 진행된 VTM 광체로, 바나듐의 이동 가능성과 풍화 작용이 선광공정에 미치는 영향이 평가되었다(Habteselassie et al., 1996). 흥미롭게도 바나듐을 함유한 자철석 광체에서 바나듐의 함량은 감소하지 않았다(Habteselassie et al., 1996). 바나듐은 광체에서 빠져나가지 않고 풍화과정 동안 생성된 녹니석이나 카올린 광물같은 2차 광물로 이동되었으나 이들 점토광물은 입도가 작기때문에 선광공정 동안 유실될 수 있다(Habteselassie et al., 1996). 이 예에서 볼 수 있듯이 VTM 광체가 풍화작용을 받은 경우에는 2차 광물에서의 바나듐의 함량까지 평가할 필요가 있다.
VTM 광상에서 바나듐의 품위는 대체로 높지 않지만 그린랜드의 시나석(Sinarsuk) 광상의 경우 자철석 내 바나듐 함량이 각각 1.93~2.68 wt% V2O5, 티탄철석에서 0.32~ 0.59 wt%로 매우 높았다(Grammatikopoulos et al., 2002). 그러나 대부분의 VTM 광체에서는 바나듐의 함량이 낮고 용리 구조가 흔하기 때문에 선광 공정에서 광석 입자를 미립으로 분쇄한다. 그럼에도 불구하고 티탄철석 용리엽은 전자현미경에서 구분될 수 있을 정도 나노미터 두께로 나타날 수 있기 때문에 광석 광물의 조직학적 특징을 확인해야 한다(Fig. 3). VTM 광석의 선광 공정은 기본적으로 분쇄와 자력선별로 구성되어 있다(Guo et al., 2020). 자력선별의 비자성 산물은 부유선별이나 정전선별을 거쳐 티탄철석 정광으로 생산된다(Lv and Bai, 2019).
자력선별 정광에서 자철석, 즉 바나듐의 품위를 올리기 위해 정선 단계를 추가하거나 청소선을 실시하여 철 광석입자의 유실을 최소화할 수 있다(Lv and Bai, 2019). 자철석 정광에서 불순물인 Al, Si, Mg, Ca 등의 함량을 최소화하는 것이 정광의 품위를 높일 뿐만 아니라 티탄철석을 함유하는 슬래그에서 TiO2의 함량을 높여 티타늄의 회수율을 개선할 수 있는 방법이다(Lv and Bai, 2019). 이를 위해 맥석의 광물 성분을 정확하게 정성 및 정량 분석할 필요가 있다. VTM 광상에서 산출되는 주요 맥석광물들은 대부분 다양한 광물단종을 포함하는 광물군으로 구성되어 있다(Table 3). 맥석광물에 대한 정확한 정성, 정량분석을 통해 자력선별 정광에 포함된 불순물 원소가 어떤 광물에서 유래되는지, 조직학적으로 자철석이 어떤 맥석광물에 수반되는지, 자철석의 단체분리도는 우수한지를 판별할 수 있다.
바나듐 생산이 환경에 미치는 영향
바나듐은 지구 어디에서나 발견되지만, 광업 등 산업 활동은 특히 바나듐의 대기 중 농도를 증가시킨 결과를 가져왔고 따라서 대기 중 바나듐의 농도가 토양에서보다 더 높다(Mandiwana and Panichev, 2004). 즉 채광 활동과 선광, 석탄과 석유같은 화석연료의 연소는 대기 중 바나듐의 대기 중 농도를 증가시키는 주요 원인이다(Kelley et al., 2005). 실제로 중국에서는 제련, 채광, 농업, 도심지역 순으로 바나듐의 발생량이 높은 것으로 보고되었다(Teng et al., 2011).
광산폐기물에도 바나듐이 함유되어 있는데 보크사이트, 우라늄 광상, VTM 광상뿐만 아니라 흑색 셰일이나 구리-납-아연 바나듐산염 광산의 광산폐기물이 이에 해당된다(Kelley et al., 2005). 바나듐이 함유된 이들 광산폐기물의 광물학적 특성은 각 광산의 광석 및 금속을 생산하는 공정에 좌우된다. 예를 들어 VTM 광상인 중국 판지후아(Panzhihua) 광산에서 배출되는 광물찌꺼기에는 티탄철석이 15-18% 함유되어 있다(Dahe, 2004). 흑색 셰일 광상인 미국의 기벨리니(Gibellini) 광산은 인회석, 방해석, 점토, 황철석, 황동석로 이루어져 있지만 바나듐은 주로 유기물에 농축되어 있어서(Desborough et al., 1979) VTM 광상과는 다른 특성을 보인다. 이러한 다양한 형태의 광물찌꺼기 또는 광산폐기물로부터 바나듐을 회수할 수 있는데 실제로 바나듐의 공급원으로 점차 중요해지고 있다(Kelley et al., 2015). 광물찌꺼기 등 광산폐기물은 이미 채광되어 지표에 위치하고 있기 때문에 채광 비용을 절약할 수 있는 잇점이 있다. 그러나 광산폐기물에서는 바나듐의 함량이 대부분 매우 낮기 때문에 바나듐 회수는 기술적으로나 경제적으로 쉽지 않은 편이다.
일반적으로 채광이 종료된 폐광은 잠재적인 환경 오염원이 될 수 있다. 다른 금속광상과 마찬가지로 VTM과 함바나듐 흑색 셰일 광상에 황철석과 같은 황화광물이 맥석으로 존재하는 경우 산성광산배수가 발생될 수 있다. 광물찌꺼기에 함유된 황화광물에 의한 산성배수는 광물찌꺼기의 광물학적 특성에 따라 적절한 처분방법으로 중화시키거나 저감시킬 수 있다(Lee, 2019). 폐광산의 환경 영향 측면에서 보면 VTM 광상은 일반적으로 규모가 크기 때문에 광산폐기물의 양도 막대하다는 특징을 갖는다(Kelley et al., 2005). 또한 VTM 광상의 모암은 철질 또는 고철질암이기 때문에 미립의 광산찌꺼기에는 철, 마그네슘, 티타늄 등의 다양한 금속이 포함될 수 있다. 이러한 금속들을 경제적으로 추출하고 최종 찌꺼기를 건축재나 유리, 세라믹 원료로 활용하는 연구(Bryan et al., 2006; Ahmadi et al., 2015; Lottermoser, 2011; Falagán et al., 2017)가 수행되어 환경 영향을 줄이려는 노력이 계속되고 있음을 알 수 있다.
한편 바나듐은 인간과 동물에게 독성을 나타내는데 수은, 납, 비소와 동일한 수준의 잠재적 독성원소로 간주된다(Moskalyk and Alfantazi, 2003). 바나듐과 철의 합금인 바나듐철(FeV, ferrovanadium)이나 강철의 생산 공정에서 발생되는 V2O5에 지속적으로 노출되는 작업자는 메스꺼움, 설사, 위경련, 적혈구의 감소 및 고혈압 증상을 겪을 수 있고 암에 걸릴 수도 있다고 추정되고 있다(Kelley et al., 2005). 이 때문에 V2O5의 농도에 대한 제한기준이 수립되었는데, 8시간 근로 기준의 작업장에서 V2O5 먼지는 0.05 mg/m3 이하, V2O5 흄은 0.1 mg/m3 이하의 농도로 유지되어야 한다(Occupational Safety and Health Administration, 2013b). 호흡을 통해 하루에 10-20 mg 이상의 바나듐을 흡입하면 독성이 나타나는 것으로 알려져 있다(Anke, 2004).
결 론
바나듐은 지각을 구성하는 미량 원소이며 지각 내 농도는 아연, 니켈과 유사한 수준이다. 바나듐은 +2가부터 +5가까지 다양한 산화상태를 갖기 때문에 광물 격자 내에서 전하와 이온 반경이 유사한 원소를 치환한다. 바나듐은 주로 지각에서 매우 흔한 원소인 Fe3+, Al3+ Ti4+를 치환하기 때문에 200개가 넘는 함바나듐 광물이 알려져 있다. 함바나듐 티타늄 자철석광상인 VTM 광상은 현재 가장 중요한 바나듐의 공급원으로 전 세계적으로 고르게 분포되어 있다. VTM 광상에서 바나듐(V3+)은 자철석-울보스피넬 고용체의 Fe3+를 치환하는 방식으로 주로 자철석에 함유되어 있다. 함티타늄 자철석에는 티탄철석이 용리엽이나 미립의 공정으로 존재하기 때문에 자력 정광에서 티탄철석을 어느 수준 이하로 제거하는 것은 불가능하다. 자력 정광을 정선하여 정광의 품위를 높일 수 있으며, 청소선을 통해 철 또는 바나듐 광석의 유실을 막을 수 있다. 정광의 품위를 저해하는 불순물 원소의 함량을 낮추기 위해서는 정확한 광물학적 특성분석, 즉 정성분석과 정량분석, 단체분리도 분석 및 수반광물 분석이 이루어져야 한다.





