서 론
실 험
출발원료
다공성 세라믹 비드 지지체 제조
메조포러스 실리카 합성
표면 코팅
특성 평가
결과 및 고찰
광미 세라믹 비드의 기공 특성
메조포러스 실리카의 기공 특성
표면 코팅 특성
결 론
서 론
광산개발의 부산물 광미(Mine tailing)는 토양오염 대책기준을 초과하는 높은 중금속 함량, 선광과정에서 사용된 독성 시약 잔류로 인하여 주변 수계 및 토양 오염의 원인이 되고 있다. 이러한 광미의 무해화법으로는 주변 수질 및 토양에 접촉하는 것을 차단하는 매립공법과 중금속 용출을 억제하는 고형화공법 등이 적용되고 있다(Lee et al., 2008; Jung et al., 2006; Yim et al., 2009). 또한, 무해화된 광미를 사용하여 건설자재 또는 지오폴리머와 같은 신소재 등으로 활용하는 연구도 진행되고 있다(Han et al., 2010).
다공성 세라믹은 높은 기공율과 기공간의 연결성이 특징이다(Huerta et al., 2007). 그리고 구형의 비드는 하중과 진동을 견딜 수 있는 우수한 내구성과 함께 물질전달의 효율 및 사용의 용이성을 증가시킬 수 있다(Schaefer and Raymond, 1983). 그러나 수십-수백 µm의 기공크기로 흡착제 및 촉매담체로 응용하기에는 적합하지 않으므로 나노미터 기공물질을 표면에 연결할 필요가 있다(Huerta et al., 2007).
메조포러스 물질(mesoporous materials)은 균일한 크기의 기공이 규칙적으로 배열되어 있을 뿐 아니라, 높은 비표면적을 가지고 흡착제, 촉매 지지체, 약물전달 지지체, 센서 그리고 나노전극물질 등에 사용되고 있다(Liu et al, 2000; Kang et al., 2004; Vinu et al., 2004; Deere et al., 2003). 또한 사용하고자 하는 용도에 따라 기공 구조 및 크기 그리고 표면 개질이 용이하기 때문에 매우 각광받고 있다. 따라서 다공성 세라믹 표면에 메조포러스 물질을 코팅하는 선행연구가 진행되어 왔다. Granato et al.(2010)은 메조포러스 실리카 MCM-41을 세라믹 폼에 코팅하여 메조기공과 매크로기공을 갖는 소재를 합성하였다. 그러나 MCM-41은 기공 벽 두께가 얇고, 수열안정성이 낮기 때문에 수계에서 적용이 어려운 단점이 있다(Cassiers et al., 2002). 반면 SBA-15는 메조포러스 물질 중 수열안정성이 높다고 알려져 있다(Ooi et al., 2004; Zhang et al., 2005). 본 연구에서는 광미를 출발원료로 하여 수 mm 크기의 다공성 세라믹 비드 지지체를 제조하고, 광미추출이온을 전구체로 하여 메조포러스 실리카 SBA-15를 합성하였다. 함침법을 통해 SBA-15를 다공성 세라믹 비드 표면에 코팅하였으며 비표면적 측정을 통해 코팅된 비드의 특성을 평가하였다.
실 험
출발원료
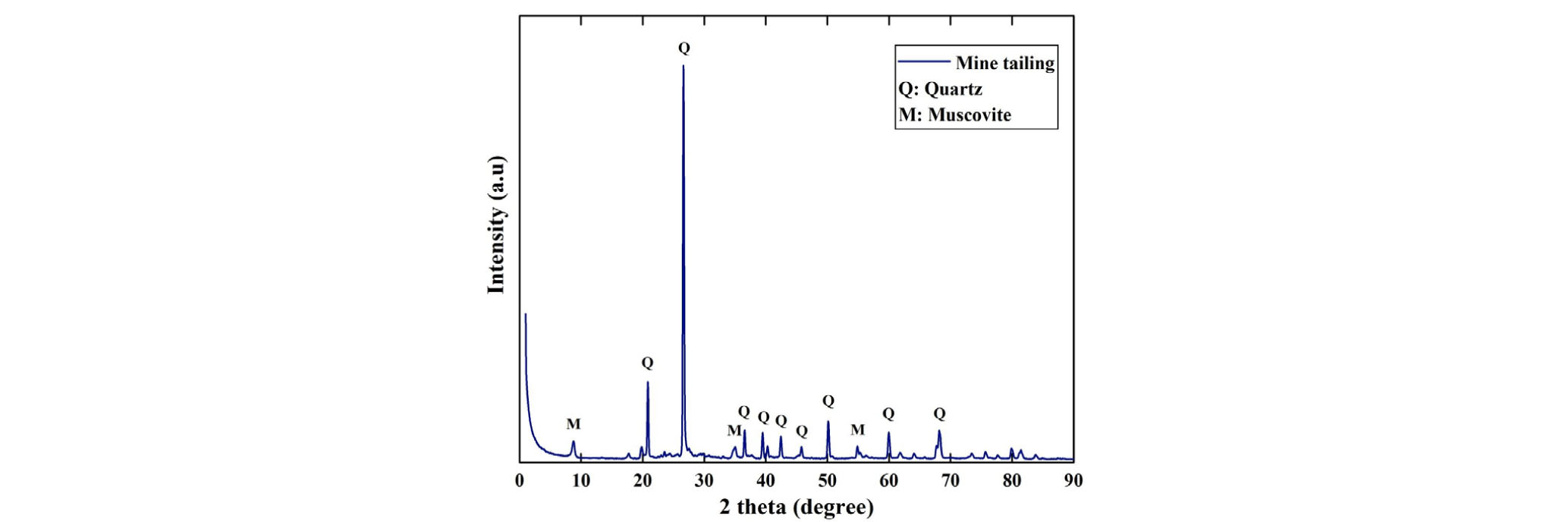
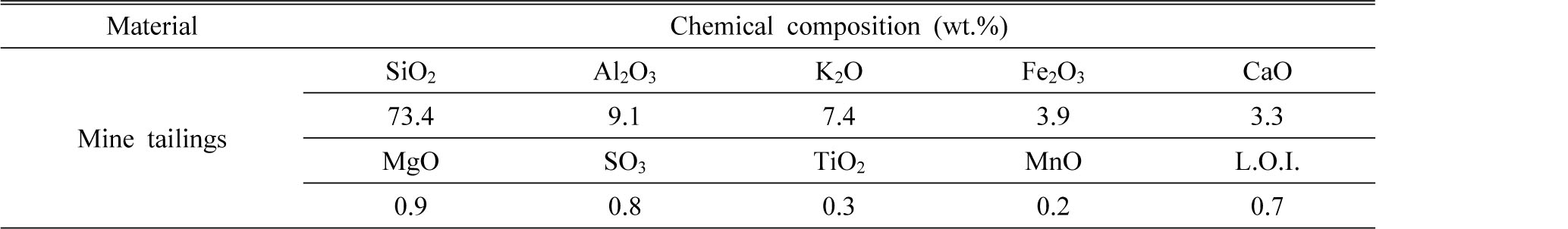
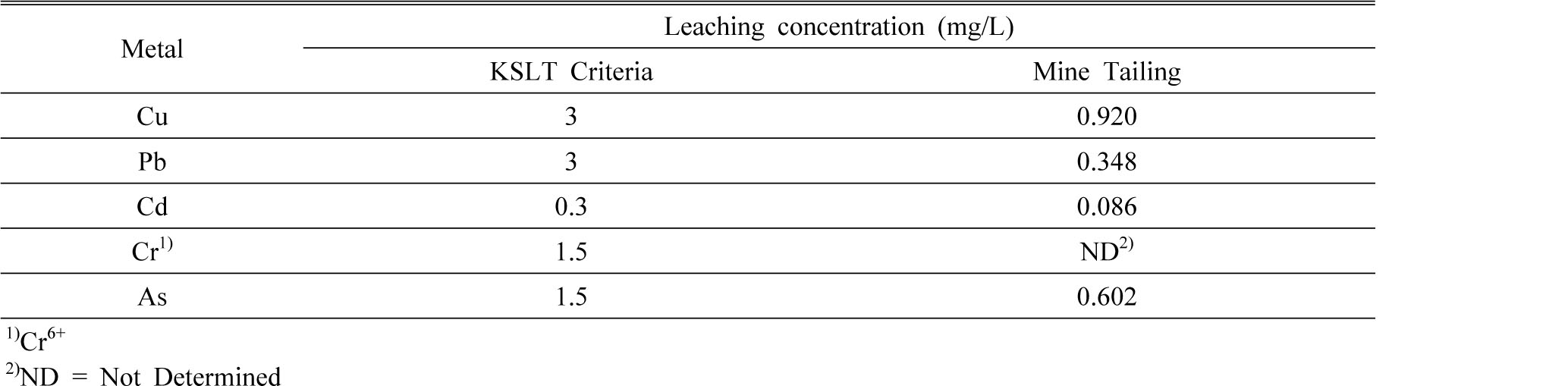
본 연구에서 사용한 광미는 전라남도 금은광산 선광장 부산물이다. 광미는 XRD 분석 결과 대부분 석영(SiO2), 백운모(K(OH)2Al3Si3O10)의 결정구조를 갖는 것으로 나타났다(Fig. 1). 또한 XRF 분석 결과, SiO2는 73.4%, Al2O3는 9.1% 등으로 나타났다(Table 1). 광미의 중금속용출시험결과, 측정한 전 항목에서 폐기물관리법 시행규칙에 규제되어 있는 중금속 기준치 이하로 검출되어 사용이 가능한 것으로 판단하였다(Table 2).
Table 2. Leaching concentration (mg/L) of heavy metal from the mine tailing tested by Korean Standard Leaching Test (KSLT) |
|
다공성 세라믹 비드 지지체 제조
교반 밀을 사용하여 광미를 d50기준 4.7µm의 입도로 분쇄하였다. 분쇄된 광미는 50 vol.%로 증류수에 넣어 세라믹 슬러리를 제조하였다. 세라믹 비드 성형 방법으로는 겔케스팅 및 액 중 조립법을 이용하였다. 겔케스팅은 고분자 중합반응을 통해 세라믹 입자의 네트워크를 형성시킨다(Mao, 2008). 액 중 조립법은 파라핀유에 슬러리를 주입하여 표면장력에 의해 구형으로 만들어진다. 액 중 조립법에 의해 제조된 성형체는 1075°C에서 소성과정을 거친 후 직경 약 3 mm 크기의 다공성 세라믹 비드(Mine tailing bead, TB)가 된다(Lee et al., 2003; Seo et al., 2013).
메조포러스 실리카 합성
메조포러스 실리카는 열수(hydrothermal) 조건에서 솔젤 과정(sol-gel process)을 통해 합성하였다(Zhao et al., 2012). 2M HCl과 증류수를 혼합한 용액에 비이온성 계면활성제인 Pluronic P123(M.W. 5800, EO20PO70EO20, Aldrich, USA)을 넣고 35°C에서 교반시켰다. 그리고 충분히 교반된 혼합물에 실리카 원으로서, 실리카 전구체인 tetraethyl orthosilicate(TEOS, Aldrich, USA)와 광미를 sodium hydroxide(Duksan, Korea)으로부터 얻은 추출액을 넣어 90°C에서 교반시켰다(Han et al., 2011; Jeon et al., 2012; Kim et al., 2015). 이때, TEOS로 합성된 메조포러스 실리카는 SBA-15-T, 광미로 합성된 것은 SBA-15-MT로 표기하였다. 교반된 혼합물은 정치와 필터링 및 건조 과정을 거친 후 계면활성제 제거를 위해 하소(Calcination) 또는 에탄올 추출(Extraction)을 시행하였다. 하소는 가장 일반적인 템플릿 제거 방법이며 계면활성제가 대부분 제거되는 장점이 있지만 수축 현상으로 인해 기공 크기가 작아지고 표면 하이드록시기가 소멸하는 단점이 있다. 반면, 추출은 계면활성제가 완전히 제거되기 어렵지만 하소에 비해 큰 기공을 얻을 수 있고 더 많은 표면 하이드록시기가 유지되는 장점이 있다(Zhao et al., 2012). 합성조건에 따라 이하 SBA-15-T-Cal은 전구체를 TEOS로 합성하고 하소한 시료이고, SBA-15-T-Ext는 TEOS로 합성 후 에탄올 추출한 것이다. SBA-15-MT-Cal과 SBA-15-MT-Ext은 광미로부터 합성 후 각각 하소법과 에탄올 추출법을 사용한 시료들이다.
표면 코팅
함침법(dip coating)을 이용하여 다공성 세라믹 비드 표면에 SBA-15를 코팅하였다. 이때 다공성 세라믹 비드는 0.5M NaOH에 20분간 수세하여 표면 활성을 제공하였다. 표면 활성은 가수분해성 금속 이온에 반응성을 주는 것으로 용액의 pH 또는 양이온의 전하밀도 및 온도를 올림으로써 표면에 하이드록시기를 제공할 수 있다(Livage, 1988). SBA-15는 증류수에 2 wt.% 넣고 20분간 초음파 처리하여 콜로이드 현탁액을 제조하였다. SBA-15 현탁액에 표면 활성이 이루어진 비드를 함침시키고 회전감압 증류기를 사용하여 수열 처리(90°C, 20 min) 한 뒤 여과 및 건조하였다.
특성 평가
광미의 주요 구성광물은 XRD(DMAXRINT 2000, Rigaku, Japan)를 통하여 분석하였고 화학분석은 XRF(PW2404, Philips, Netherlands)를 통해 확인하였다. 분쇄한 광미의 입도 크기 분포는 레이저 회절 입도분석기(LA-950V2, HORIBA, Japan)를 이용하여 측정하였다. 다공성 세라믹 비드의 기공 크기 분포는 광학현미경(Digital microscope system, Leica DVM2500, Leica VZ80, Germany)으로 촬영하고 화상해석 프로그램(LAS Macro Editor, Leica, Germany)을 통해 분석하였다. 합성한 SBA-15의 기공 크기와 등온흡탈착 곡선은 질소흡착기(ASAP 2020, Micromeritics, USA)를 이용하였으며, 미세구조는 TEM(JEM-2010, JEOL, Japan)을 통해 확인하였다. 또한 적외선 분광광도계 (FT-IR 4100, Jasco, Japan)를 통해 SBA-15의 표면 하이드록시기를 정성적으로 분석하였다. SBA-15가 코팅된 다공성 세라믹 비드의 기공 단면은 SEM(Nova Nano SEM, FEI, USA)을 통해 확인하였다.
결과 및 고찰
광미 세라믹 비드의 기공 특성
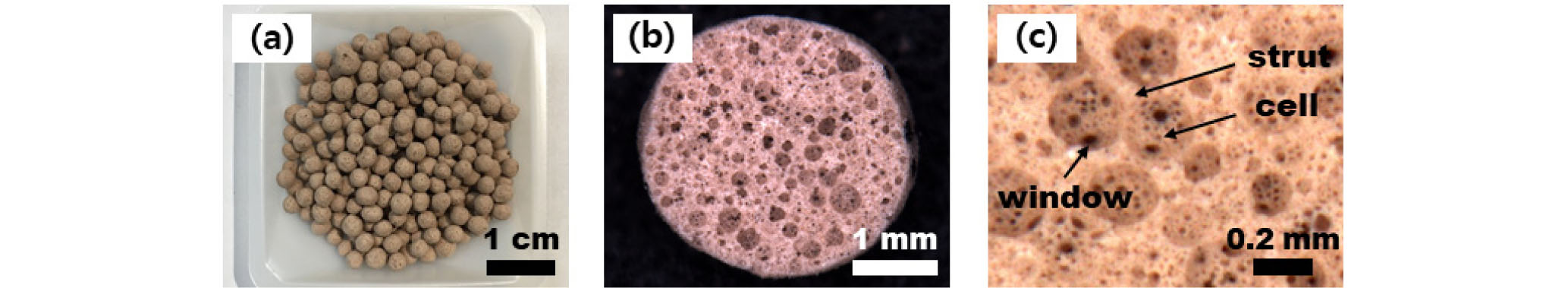
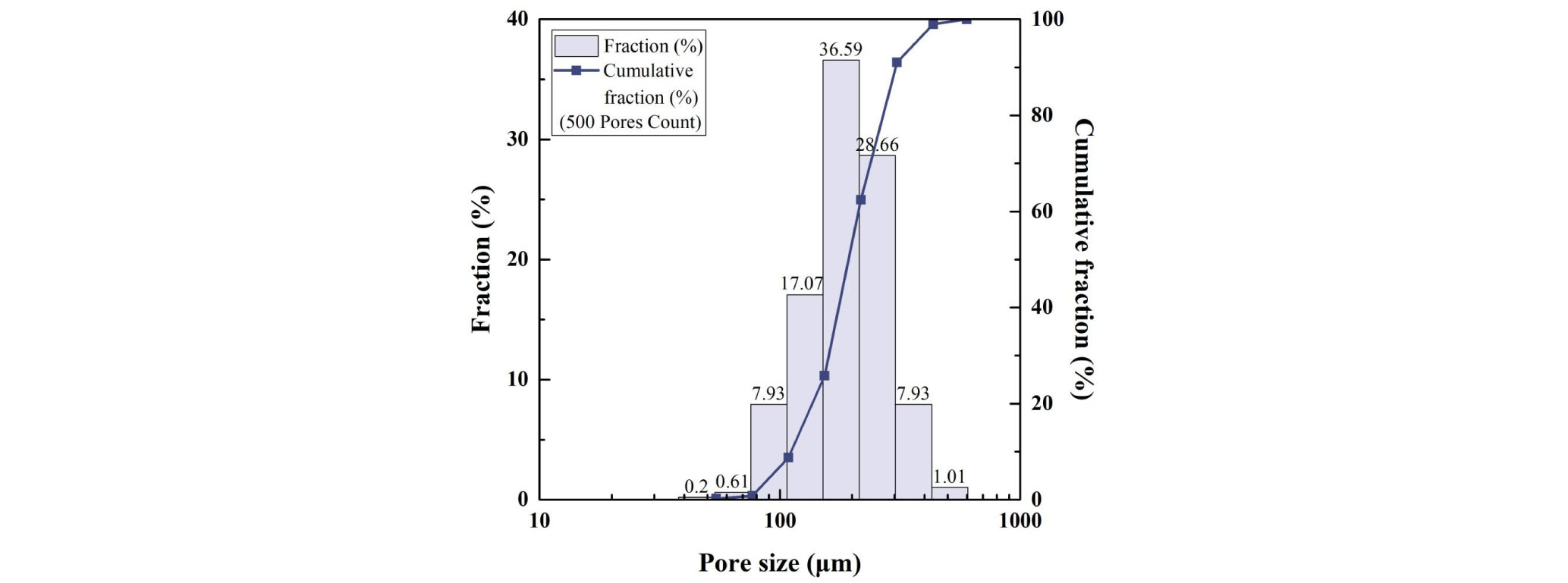
Fig. 2(a)는 제조된 다공성 세라믹 비드(Mine tailing bead, TB)의 외관을 나타낸 것이며, (b)는 광학현미경(Leica)으로 촬영한 TB의 단면이다. 단면을 확대한 사진 (c)에서 기공(cell)과 골격(strut)을 관찰할 수 있었고, 근접한 기공과 기공 사이에 연속적인 채널이 발견됨에 따라 window의 존재를 확인하였다. 이를 통해 TB support는 기공과 기공이 연결되어 있는 열린 기공을 갖는 3D-network 구조임을 확인하였다(Liang et al., 2012). 즉, 내부 기공들이 연결되어 형성된 window를 통해 열린 기공을 형성하기 때문에 유체흐름에 대한 투과특성이 클 것으로 생각되었다. 그리고 화상해석 프로그램을 사용하여 500개의 기공(cell)을 임의로 선택해 기공 크기를 측정하였다(Park et al., 2005). Fig. 3에 TB의 기공 크기 분포를 나타내었으며 기공 크기는 d50 기준 160 µm, 기공율은 83%로 나타났다.
메조포러스 실리카의 기공 특성
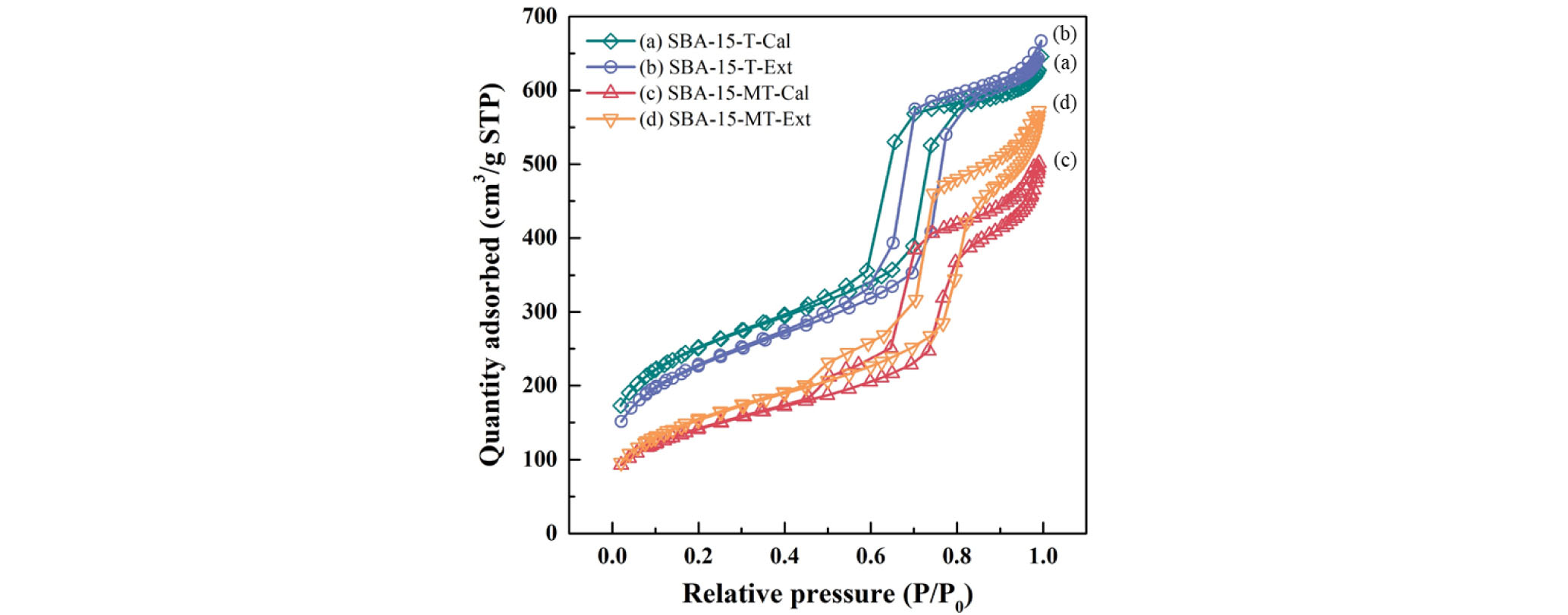
SBA-15 시료들의 질소 흡탈착등온곡선은 Fig. 4와 같다. 합성된 네 종류의 시료는 모두 IUPAC 분류에 의해 IV 형태의 전형적인 메조포러스 물질로 확인되었다. 그리고 히스테리시스 곡선 분류에 따라 H1인 실린더형의 기공으로 존재하는 것으로 나타났다(Han et al., 2011). Fig. 5는 SBA-15-T-Cal과 SBA-15-MT-Cal의 TEM 사진이다. 사진으로부터 규칙적으로 기공이 배열된 전형적인 메조포러스 실리카의 hexagonal한 기공구조를 확인할 수 있었다.
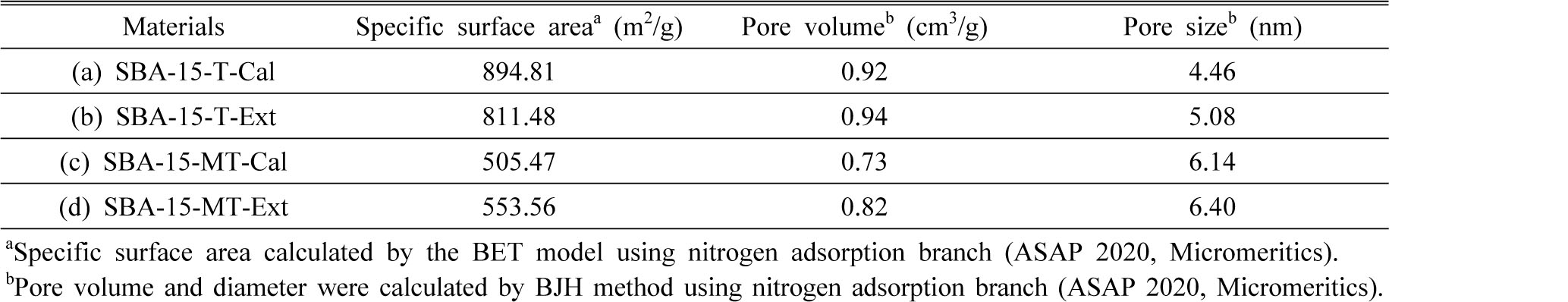
Table 3에 SBA-15 시료들의 비표면적 및 기공 부피, 기공크기를 나타내었다. SBA-15-T의 비표면적은 약 811~894 m2/g으로 SBA-15-MT보다 약 1.7배 높게 나타났다. 이는 SBA-15-MT의 경우 실리케이트 추출 용액 내 불순물로 인하여 SBA-15의 자기조립 현상이 방해되었기 때문으로 생각된다. SBA-15-T의 경우 하소했을 때 추출에 비해 비표면적이 높고, SBA-15-MT의 경우 하소로 인한 기공 막힘이 많았으며 에탄올 추출 효과가 크게 나타났다. 기공 크기는 BJH 이론을 통해 계산되었으며 이는 메조 기공(2~50 nm)과 매크로 기공(>50 nm)만을 대상으로 한다. 일반적으로 비표면적이 높을수록 작은 기공 크기에서의 흡착량이 많아 비표면적과 기공크기는 서로 반비례하나 SBA-15-MT의 경우 비례하였다. 그 이유는 SBA-15-MT는 SBA-15-T와 다르게 두 구간(3 nm와 6~8 nm)에서 비슷한 수준의 기공 크기 피크가 나타났고 SBA-15-MT-Ext의 경우 두 번째 구간에서의 흡착량이 SBA-15-MT-Cal보다 높았기 때문이다. 또한 기공 크기는 (a)와 (c)보다 (b)와 (d)에서 크게 도출되었는데 이는 하소 시 수축 현상으로 기공이 작아지기 때문이다(Zhao et al., 2012).
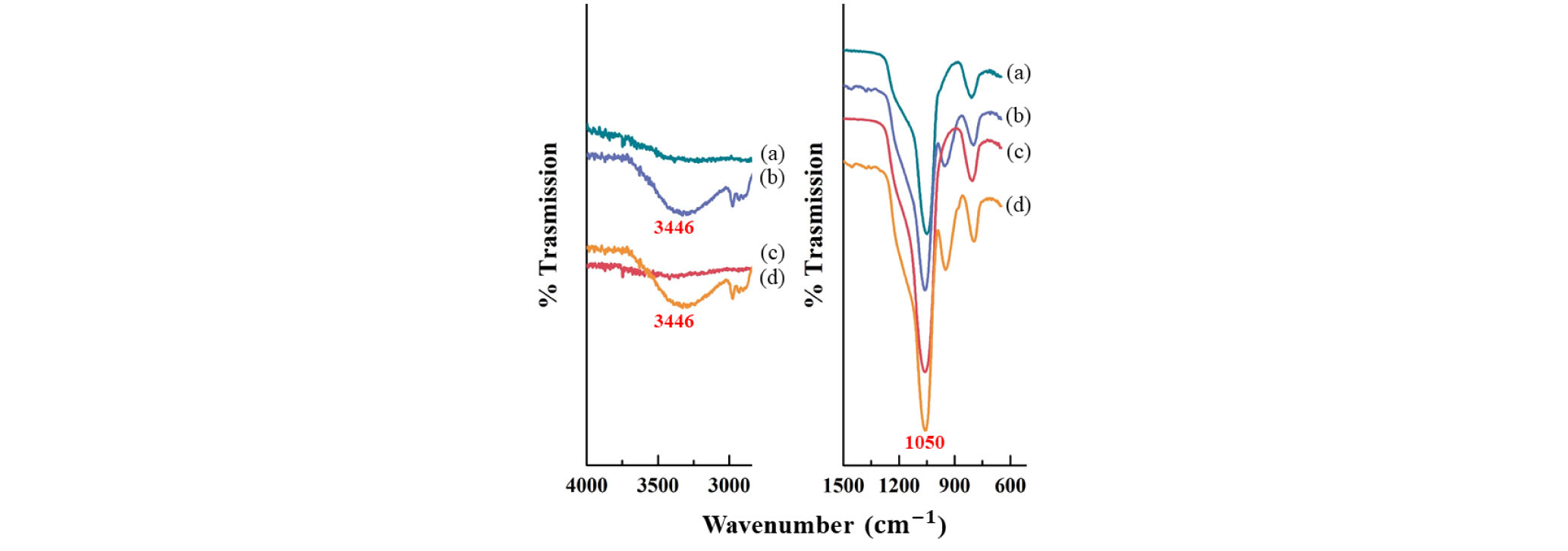
Fig. 6은 SBA-15 시료를 각각 하소와 추출하였을 때 표면 실란올(silanol)을 확인하고 비교하기 위한 FT-IR 스펙트럼이다. 3346 cm-1에서의 피크는 Si-OH 분자구조의 진동에 해당한다(Lai et al., 2012). 하소한 SBA-15는 표면수 및 결정수가 열분해되어 하이드록시기의 밀도가 낮고, 에탄올 추출한 SBA-15는 하소보다 상대적으로 높은 하이드록시기 밀도를 보였다. SBA-15 표면의 Si-OH는 광미 비드 표면의 Si-OH와 반응하여 물 분자를 내보내며 Si-O-Si 결합을 만들기 때문에 표면 하이드록시기의 존재는 중요하다. Fig. 7(a), (b), (c), (d) 모두 1,050 cm-1에서 가장 큰 피크를 보였다. 800~1,050 cm-1에서의 피크는 Si-O-Si 분자구조의 진동이며 실리카 물질에서 흔히 나타난다(Kim et al., 2015).
표면 코팅 특성
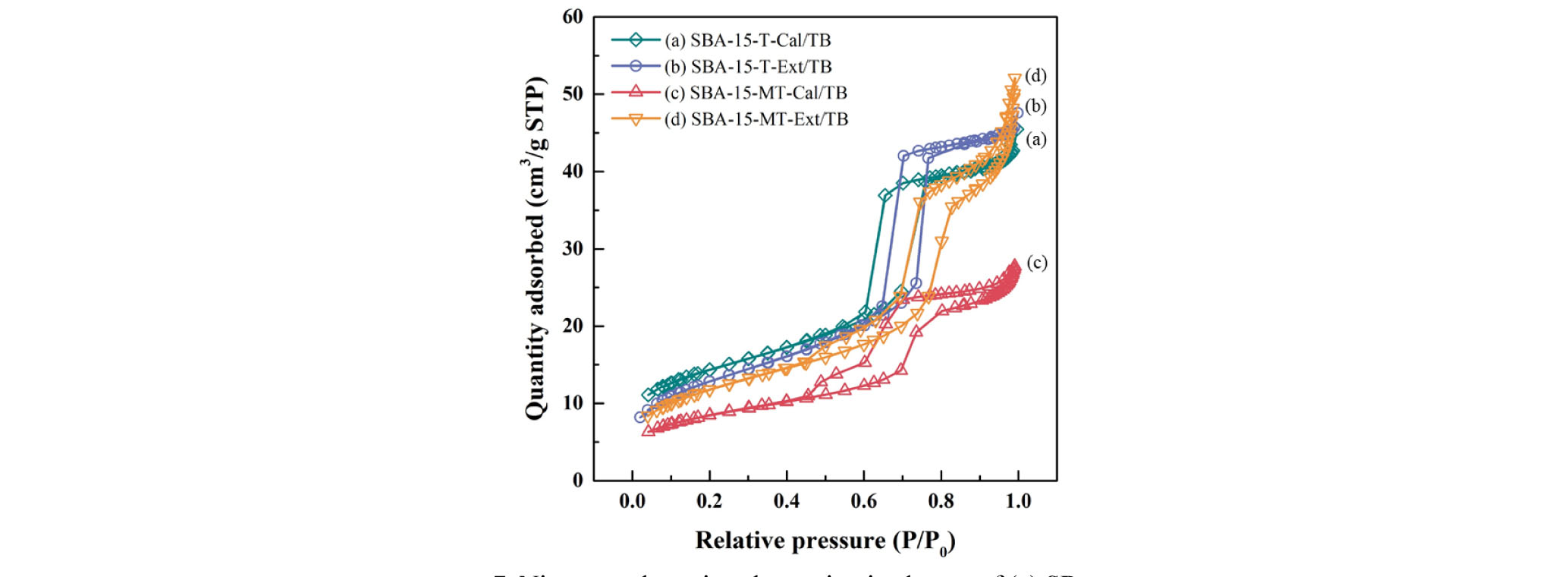
Fig. 7은 SBA-15가 코팅된 TB의 질소 흡탈착등온곡선이다. 등온곡선은 메조기공에서 모세관 응축에 의해 질소흡착량이 상대압(P/P0) 0.5-0.7부터 높게 나타났으며 이는 Fig. 4에서 보인 질소흡착량 결과와 동일했다. 즉, 비드 표면에 코팅된 SBA-15의 존재를 확인할 수 있었다.
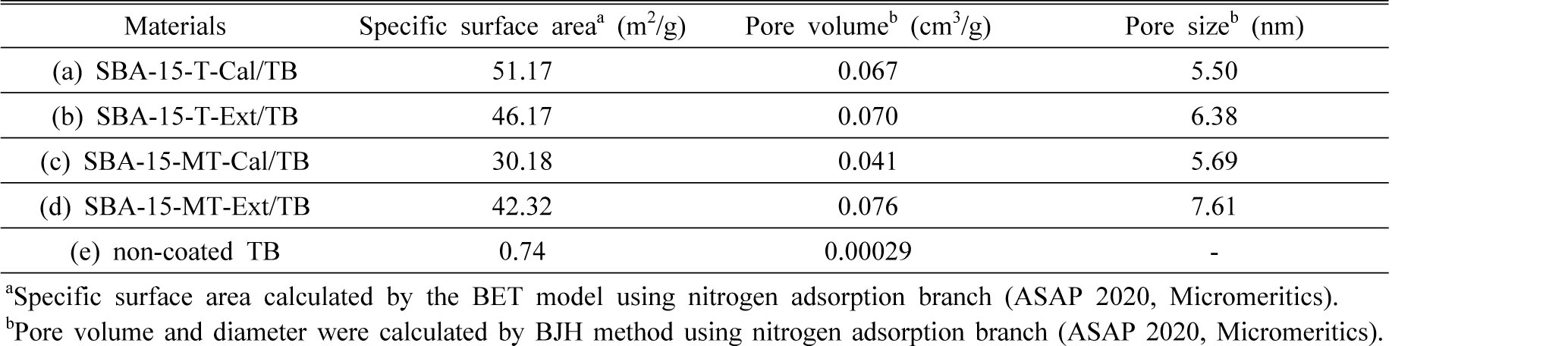
Table 4는 SBA-15가 코팅된 TB의 질소흡착기 분석 결과이다. Tables 3과 4를 비교하면, 코팅된 비드의 비표면적 크기순으로 (a), (b), (d), (c) 순으로 높게 나타났다. Table 3의 SBA-15-T의 비표면적은 (a)가 (b)보다 약 9.3% 높았으며 TB 표면에 코팅한 이후의 비표면적은 Table 4(a)가 (b)보다 약 9.7% 정도 높게 나타났다. 즉, 코팅물질 SBA-15-T의 비표면적 차이에 비해 코팅된 TB의 비표면적은 큰 차이가 없었고 이는 SBA-15-T-Ext의 높은 하이드록시기 밀도가 코팅을 용이하게 해준 것으로 사료된다. 또한 Table 3의 SBA-15-MT의 비표면적은 (d)가 (c)보다 약 8.7% 높았으며 이를 TB표면에 코팅 후, Table 4의 (d)가 (c)보다 29% 더 높게 나타났다. 즉, 추출법을 이용한 SBA-15-MT-Ext의 코팅 후 비표면적 상승률이 더욱 크게 나타났다. 따라서 Fig. 6을 통해 확인한 추출한 SBA-15 시료의 높은 하이드록시기 밀도가 TB에의 코팅에 영향을 끼친 것으로 사료된다. 결과적으로 비표면적이 0.74 m2/g으로 낮았던 다공성 세라믹 비드는 SBA-15가 표면에 코팅됨에 따라 비표면적이 52 m2/g까지 증가하였다. 선행 연구 결과를 살펴보면, Granato et al.(2010)이 제작한 MCM-41이 최적으로 코팅된 세라믹 폼 M120-3과 M80-4의 비표면적은 각각 42 m2/g와 17 m2/g이다. 또한 Huerta et al.(2007)이 제작한 나노물질 UVM-7이 1회 코팅된 세라믹 폼의 비표면적은 44 m2/g이며 코팅 횟수에 따라 비표면적이 상승하였다. 본 연구에서 제작한 SBA-15/TB는 선행 연구 소재(Granato et al., 2010; Huerta et al., 2007)보다 높은 비표면적을 보였다. 또한 코팅 횟수를 늘릴수록 비표면적은 더욱 상승할 것으로 예상된다. 더욱이 본 연구에서 제작한 구형의 세라믹 폼은 기존 직육면체의 세라믹 폼보다 표면적이 넓기 때문에 유체 내 반응효율을 높일 수 있고 그에 따른 응용 분야가 다양하다는 장점이 있다.
Table 4의 기공크기의 경우, Table 3에 나타난 SBA-15의 기공크기보다 대부분 크게 나타났는데 이는 측정된 기공의 균일성이 떨어졌기 때문이다. 즉, 질소흡착기를 이용하여 수 나노 및 수백 마이크로미터의 Bimodal한 기공물질의 기공크기를 평가하는 것은 적합하지 않음을 확인하였다.
SBA-15가 코팅된 TB의 기공 단면은 SEM 사진을 통해 확인하였다. Fig. 8(a)는 TB의 단면 사진이며, (b)는 SBA-15가 코팅된 TB 사진이다. 사진 (b)로부터 window가 막히지 않은 상태로 TB 표면에 코팅된 SBA-15를 확인할 수 있었다.
결 론
광미를 활용하여 나노기공구조를 갖는 다공성 세라믹 물질을 제조한 결과 도출한 결론은 다음과 같았다.
1. 다공성 세라믹 비드는 기공과 기공이 연결되어 열린 기공을 가진 3D-network 구조였다. 기공 크기는 화상해석 프로그램을 통해 측정한 결과, d50기준 160 µm였다.
2. TEOS를 전구체로 하여 합성한 SBA-15는 광미로부터 추출된 실리케이트 이온을 전구체로 했을 때보다 약 1.7배 높은 비표면적을 나타냈다. 또한 SBA-15는 하소한 경우보다 에탄올 추출법을 통해 템플릿을 제거했을 때 상대적으로 높은 하이드록시기 밀도를 보였다.
3. 함침법을 이용해 TB의 기공 표면을 SBA-15로 코팅한 결과, 코팅물질인 SBA-15의 비표면적과 표면 하이드록시기 밀도가 높을수록 코팅된 비드의 비표면적이 높았다. 코팅 후 비드의 비표면적은 최대 52 m2/g 수준으로 선행 연구 소재보다 높게 나타났다.