서론
인쇄회로기판(printed circuit boards, PCBs)은 대다수 전자제품의 필수 부품이며, 해당 제조공정에서 회로인쇄를 위해 사용된 구리 중 불필요한 구리를 제거하기 위해 에칭공정(ethcing process)이 적용된다(Adakkalam et al., 2002; Keskitalo et al., 2007). 에칭공정으로부터 발생한 폐에칭액은 상당한 양의 구리(10-15%)를 포함하고 있기 때문에(Kim et al., 2002), 에칭액 중 구리성분을 회수하기 위한 다양한 연구가 다음과 같이 진행되었다. Yang과 Kocherginsky (2006)는 폐에칭액으로부터 실관형 지지액막(hollow fiber supported liquid membrane)을 이용한 구리회수거동을 조사하였으며, Kim et al.(2002)는 폐애칭액으로부터 형상조절형 산화동 제조를 보고하였다. Keskitalo et al.(2007)는 산성 염화구리에칭액(acidic cupric chloride etchant)의 재생에 관한 특허들을 정리하여 보고하였다. 이 보고에서 특허들은 전기화학적 재생, 세멘테이션, 용매추출, 염기성 염화구리 제조, 그리고 산화동 침전으로 분류되었다.
한편, 산화동은 가장 오래된 선박 방오제의 하나로서 선박 바닥면의 해양계 생물들의 부착을 방지하며, 방오제 사용에 의해 선박운영 중 에너지 비용이 30% 정도 절감한다고 알려져 있다(Lossin and Westhoff, 1997). 또한 산화제1동(cuprous oxide, Cu2O)은 붉은색 계통의 염료로 사용되며 이 또한 살생물제(biocide)로서 사용되어 왔다(Lossin and Westhoff, 1997). 최근 산화제1동이 2.2 eV의 밴드갭(band gap)을 갖고 있어 광촉매로서의 사용이 주목되고 있다(Zhang et al., 2008). 이러한 산화제1동의 제조방법으로는 열수 환원(hydrothermal reduction) (Zhang et al., 2008), 전착(electrodeposition) (Huang et al., 2002), 열이완(thermal relaxation) (Deki et al., 1998), 음향화학적 방법(sonochemical methods) (Kumar et al., 2001), 진공증착(vacuum evaporation) (Yanagimoto et al., 2001), 그리고 금속염의 액중 환원(Ram and Mitra, 2001)이 제안되어 왔다.
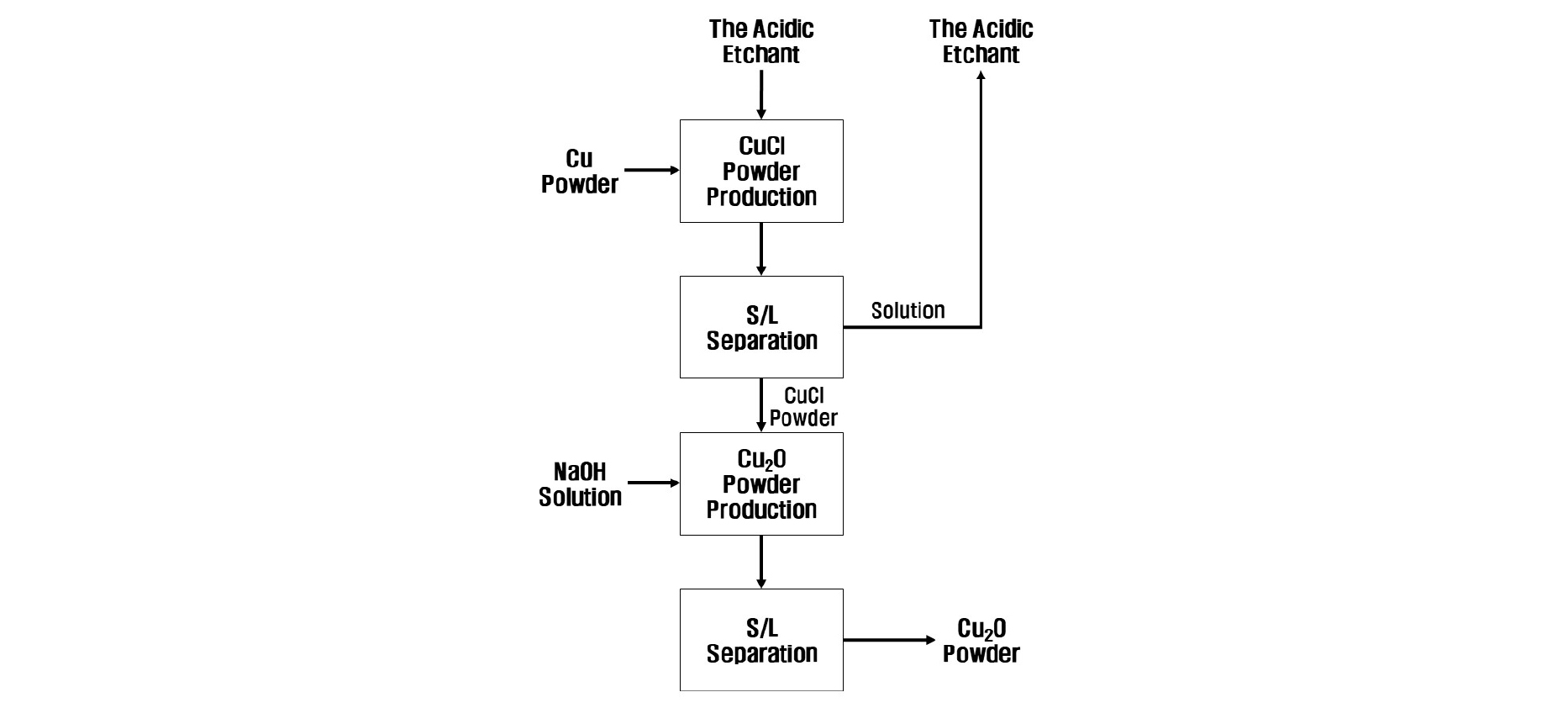
다만 현재까지 고농도 구리를 함유하고 있는 폐에칭액으로부터 산화제1동을 제조하는 연구는 많이 보고되지 않아, 본 논문에서는 Fig. 1과 같은 공정을 통해 에칭액으로부터 산화제1동을 회수하고자 하였다. 이 공정은 크게 두가지 세부공정으로 구성되어 있는데, 우선 폐에칭액에 구리 분말을 투입해 구리 성분을 철과 주석 등의 불순물로부터 분리하여 염화구리(CuCl)로 침전시키는 공정, 그리고 회수된 염화구리분말을 수산화나트륨 수용액과 반응시켜 산화제1동을 제조하는 공정으로 구성된다. 모든 공정은 상온에 가까운 30oC에서 진행된다.
본 연구는 Fig. 1에 기술된 공정의 가능성을 평가하기 위해 진행되었으며, 에칭액과 구리분말을 이용한 염화구리 제조과정에서의 ORP(Oxidation-Reduction Potential) 변화를 관찰하고, 산화제1동 형성에 미치는 pH의 영향을 관찰하기 위해 수산화나트륨 농도를 조절하여 산화제1동 제조실험을 진행하였다.
실험방법
실험재료
본 연구에서 사용된 폐에칭액은 국내의 PCB 제조사로부터 확보하였으며 폐에칭액의 주요 성분과 pH를 Table 1에 나타내었다. 폐에칭액 중 구리농도는 156 kg m-3으로 매우 높으며, 철과 주석의 농도는 각각 1,100 g m-3과 7.3 g m-3이고, 염산함량은 9.5%이었다. 에칭액의 pH는 –0.83으로 강산성이었다.
본 연구에서 구리분말(Aldrich, USA)은 순도가 99%이며, 크기가 75 µm이하인 것을 사용하였다. NaOH용액은 시약급의 NaOH(JUNSEI, Japan)를 초순수에 용해시켜 제조하였다.
염화구리 제조방법
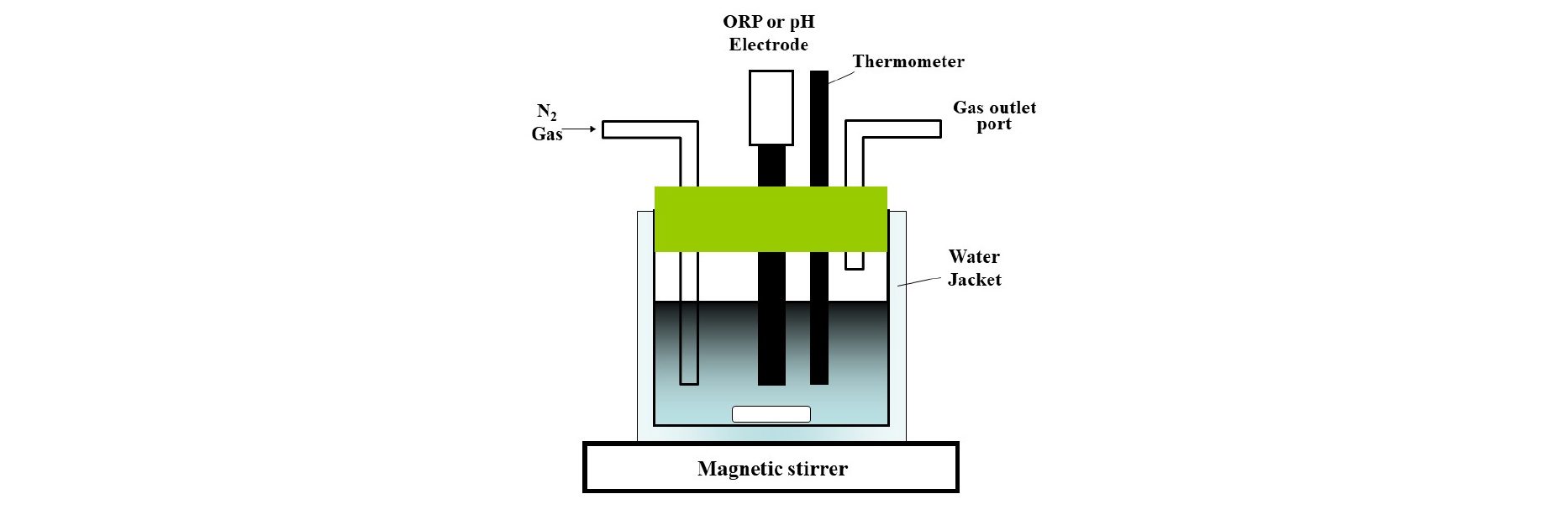
Fig. 2에 본 연구에서 사용된 실험장치의 모식도를 나타내었다. 반응기에 50 cm3의 에칭액을 주입하고 온도를 30oC로 증가시킨 후 유지하였다. 용존산소의 영향을 최소화하기 위하여 실험 전 한시간전 부터 반응기에 질소를 주입하고, 7.8 g의 구리분말을 용액에 투입하였다. 반응기는 실리콘 마개로 밀봉되었으며, 실리콘 마개에는 OPR 전극(saturated with Ag/AgCl), 온도계, 질소가스 주입과 배기를 위한 유리관들이 각각 장착되었다. 실험이 진행되는 동안 자석교반에 의해 500 rpm으로 교반되었다.
산화제1동 제조방법
염화구리 제조실험에서 사용된 반응기와 동일한 반응기에 ORP 전극 대신 pH 전극을 삽입하여 산화제1동 제조실험을 진행하였다. 50 cm3의 초순수를 반응기에 넣고 상기의 염화구리 실험에서 얻어진 염화구리분말 4 g을 초순수에 넣었다. NaOH의 농도를 0.3, 0.7, 0.8, and 1.6 kmol m-3로 조절한, 50 cm3 NaOH 용액을 염화구리분말 수용액에 첨가하여 실험을 진행하였다. 질소가스를 모든 용액에 혼합 전 주입하였고, 온도와 교반속도는 각각 30oC와 500 rpm으로 고정하였다. 제조과정 중 용존산소의 영향을 최소화하기 위해 질소가스를 지속적으로 주입하였다.
분석방법
염화구리와 산화제1동 제조 실험 중 ORP와 pH는 정해진 시간에 각각 ORP와 pH 전극을 이용하여 측정되었다. 각 실험이 종료된 후 용액은 멤브레인 필터(0.45 µm)를 이용하여 여과한 후 70oC에서 12시간 건조하였다. 건조된 시료는 Ru-200B X-ray diffractometer(Rigaku, Japan)를 이용하여 XRD 패턴을 조사하였으며, Cu Kα 타겟을 이용하여 40 kV과 30 mA의 조건에서 CuCl 분말은 5~65 degree/2θ 범위에서, Cu2O 분말은 5~75 degree/2θ의 범위에서 8 deg/min의 스캔속도로 조사하였다.
산용해 후 JY-38 plus(Laptam Co., Australia) inductively coupled plasma atomic emission spectroscope(ICP-AES)를 이용하여 구리함량을 측정하였다. 분말 중 염소함량은 proton induced X-ray emission(PIXE) 방법으로 분석하였으며, X-ray 검출기로는 NEC 5SDH-2 tandem VDG accelerator and Si(Li) X-ray detector를 이용하였다. 열중량 분석은 질소분위기에서 2960 SDT V3.0F(TA instruments, USA)를 이용하여 분당 10oC의 승온조건에서 실시하였다.
실험결과 및 고찰
구리를 불순물로부터 분리하기 위해 용매추출(Aminian and Bazin, 2000; Cupertino et al., 1999)이나 황화 침전(precipitation using H2S) (Hammack and Dijkman, 1999)이 연구되어 왔다. 이 연구에서는 철과 주석을 함유하고 있는 폐에칭액으로부터 구리를 회수하기 위해 구리분말을 투입하여 선택적인 구리침전이 시도되었다. 이 반응은 식 (1)과 같이 나타낼 수 있다(Herreros et al., 2005).
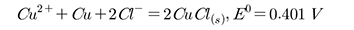 (1)
(1)
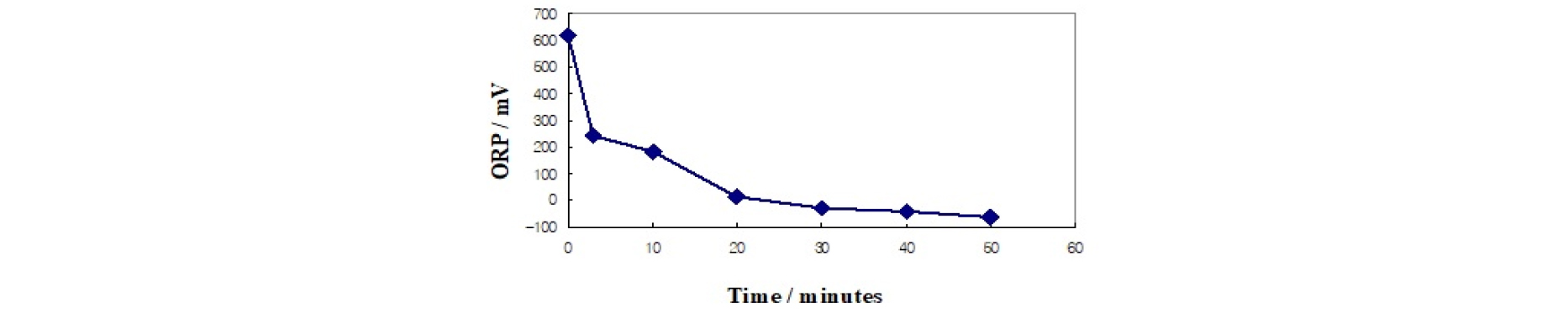
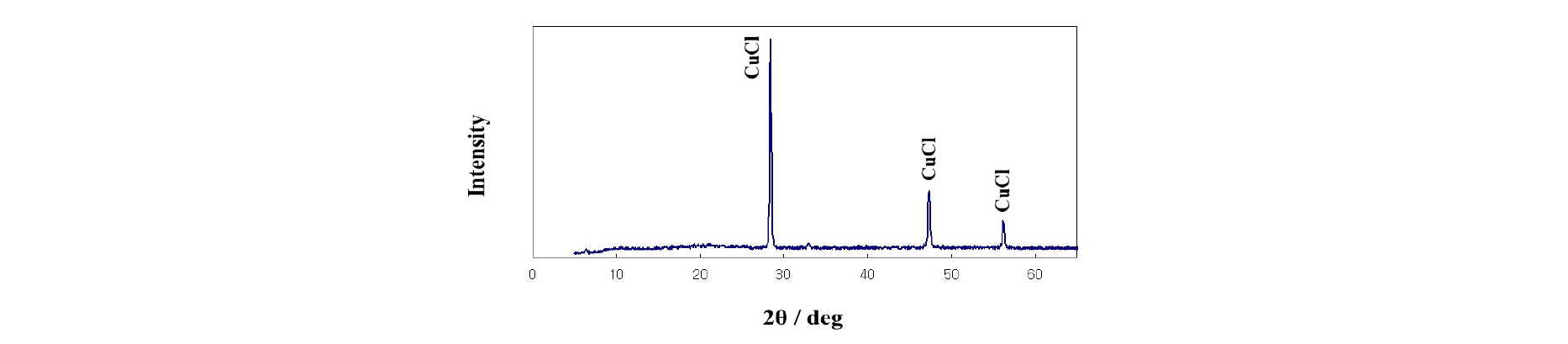
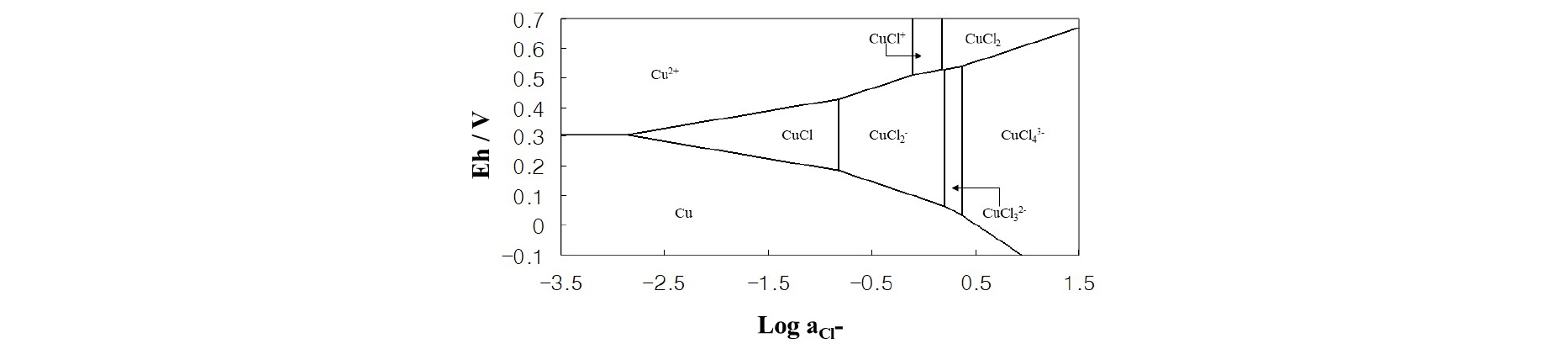
폐에칭액에 구리분말을 투입한 후 ORP의 변화를 Fig. 3에 나타내었다. 반응이 진행됨에 따라 ORP는 –72.1 mV까지 감소하였는데, 이는 구리 2가이온이 감소하고 구리 1가 이온종이 증가함에 따른 것으로 생각된다. Fig. 4는 회수된 분말의 XRD 패턴을 나타내었으며, 이 결과는 염화구리의 피크(JSPDS 6-0344)와 일치한다. 염화구리(CuCl)의 용해도는 매우 낮기 때문에(KSP=1.72 × 10-7) (Lin et al., 1991), 구리분말 투입에 의해 염화구리 분말이 형성되며 구리성분을 회수할 수 있다. 구리의 침전에도 불구하고 구리 농도는 반응 후 17.5 kg m-3가 남아있는데, 이는 Fig. 5에 나타낸 바와 같이 염소이온농도가 높을 경우 용액 내에는 CuCl2-, CuCl32-과 CuCl43-의 구리 1가 이온종이 형성되기 때문이다(Lin et al., 1991). 여기서 잔존하는 구리이온은 Fig. 1에 나타낸 바와 같이 재활용 공정으로 재투입된다.
염화구리 분말 중 구리함량은 63.9%였고, 철과 주석 성분은 검출되지 않았다. 이 결과는 철과 주석 등의 불순물로부터 성공적으로 구리성분만을 분리한 것으로 평가할 수 있다. 일반적으로 산화제1동 분말 중 산화철(Fe2O3) 함량은 0.02 wt%로 제한된다.
상기에서 회수된 염화구리 분말을 수산화나트륨 수용액에 투입했을 때 분말의 색이 붉게 변하는 것이 관찰되었으며, 이 반응은 다음의 반응식으로 나타낼 수 있다(Hyvarinen and Hamalainen, 2005).
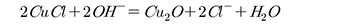 (2)
(2)
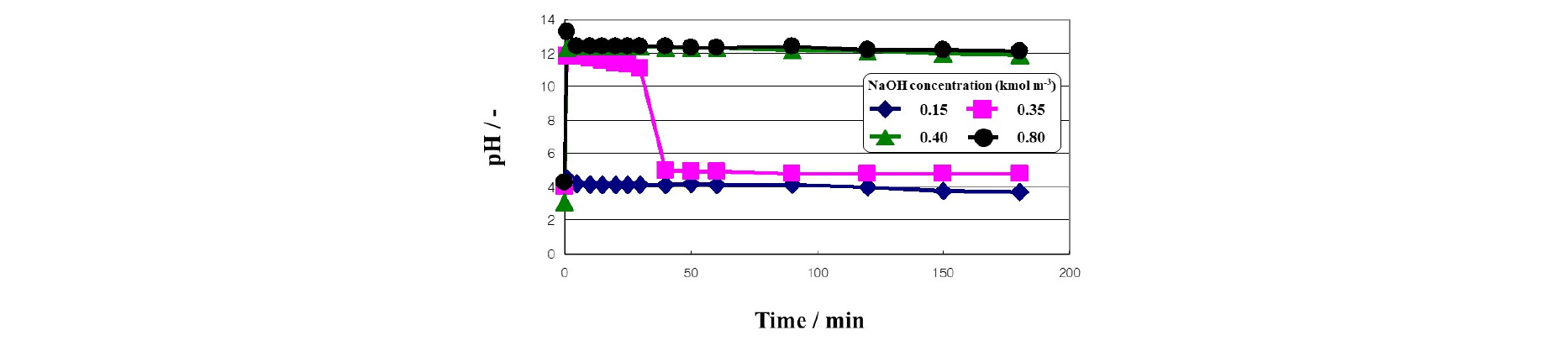
Fig. 6에 NaOH 초기농도에 따른 pH의 경시변화를 나타내었다. 용액의 pH는 NaOH의 초기농도가 각각 0.15, 0.4, 그리고 0.8 kmol m-3일 때 3.7, 11.9, and 12.1에서 유지되었고, NaOH 농도가 0.35 kmol m-3일 때 pH는 40분 후 급격히 감소하여 pH 4.8에서 일정하게 유지되었다. 식 (2)의 평형상수는 다음과 같이 나타낼 수 있다.
 (3)
(3)
Table 2의 데이터를 이용할 때 평형상수는 10-12.1로 계산되었다. 이 계산에서 활동도 계수는 1로 가정되었다. 물의 해리상수는 다음과 같다.
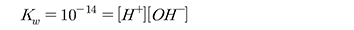 (4)
(4)
식 (4)를 식 (3)에 대입한 후 정리하면 식 (5)와 같이 나타낼 수 있다.
 (5)
(5)
이를 pH의 식으로 정리하면 식 (6)과 같다.
 (6)
(6)
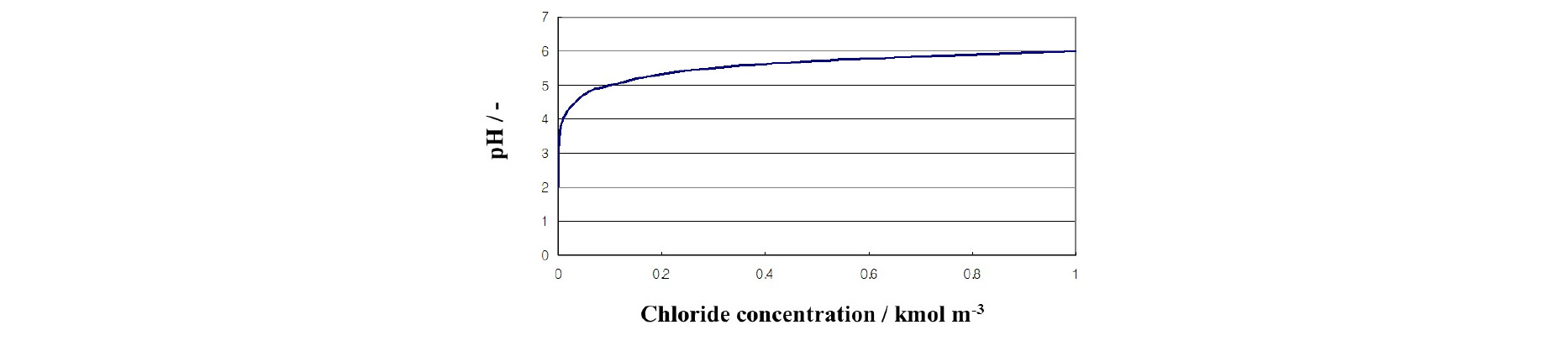
평형 pH와 염소이온 농도의 관계를 Fig. 7에 나타내었다. 이 연구에서 용액 중 CuCl의 양은 0.4 kg m-3이며, 이를 농도로 표현하여 계산하면, 평형 pH는 5.4로 계산되어 Fig. 6의 결과인 pH 4.8에 근접하는 것을 알 수 있다. 여기서 발생한 오차는 활동도 계수가 1로 가정된 것과 용액 중 구리이온이 잔존한 것이 원인일 수 있다고 생각된다. NaOH 농도가 0.35 kmol m-3일 때 구리잔존농도는 394.5 g m-3이고, NaOH 농도가 0.4와 0.8 kmol m-3일 때 구리는 검출되지 않았다.
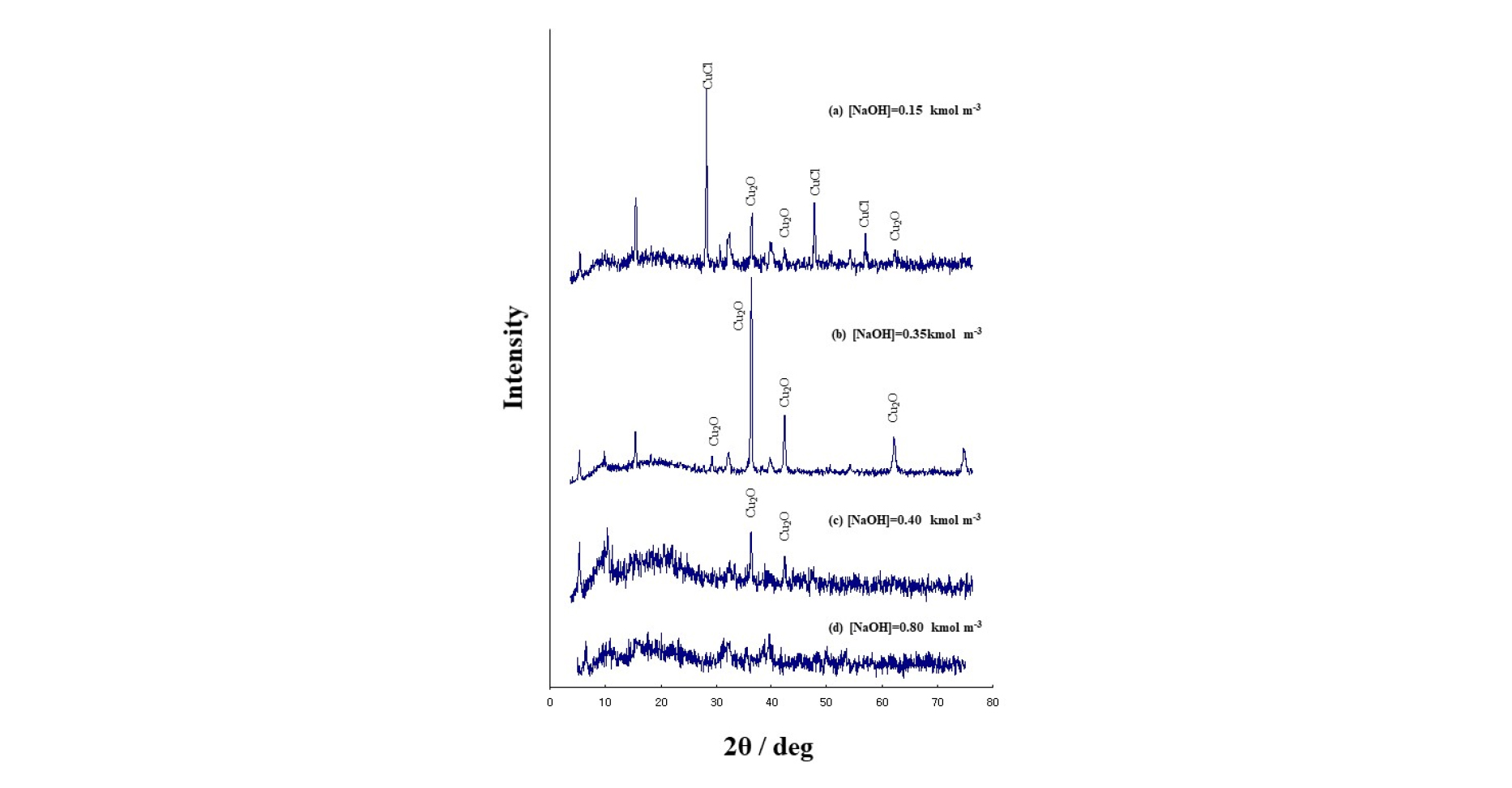
NaOH의 농도가 0.15, 0.35, 0.4, 0.8 kmol m-3일 때 회수된 분말의 XRD 패턴을 Fig. 8에 나타내었다. NaOH의 농도가 0.15 kmol m-3일 때(Fig. 8(a)), 산화제1동과 염화구리의 피크가 동시에 관찰되었으나 0.35 kmol m-3일 때 산화제1동의 피크(JSPDS 05-0677)만이 관찰되었다. NaOH의 농도가 0.4와 0.8 kmol m-3일 때 부분적으로 산화제1동의 피크가 관찰되었으나 피크가 약하거나 사라져 비정질이 형성된 것으로 생각되었다. 따라서 이 결과는 평형 pH에 근접한 용액의 pH에서 산화제1동이 형성될 수 있는 것을 나타낸다.
산화제1동 분말 중 염소의 함량을 PIXE를 이용하여 분석하였다. NaOH의 농도가 0.15 kmol m-3일 때, 분말 중 11.2%의 염소가 존재하는 것으로 분석되었으나 다른 NaOH 농도를 사용한 결과 염소는 검출한계 이하로 나타났다. 이 결과는 0.35 kmol m-3의 NaOH를 반응시킬 경우, 염화구리 분말이 산화제1동 분말로 성공적으로 전환된 것을 나타낸다.
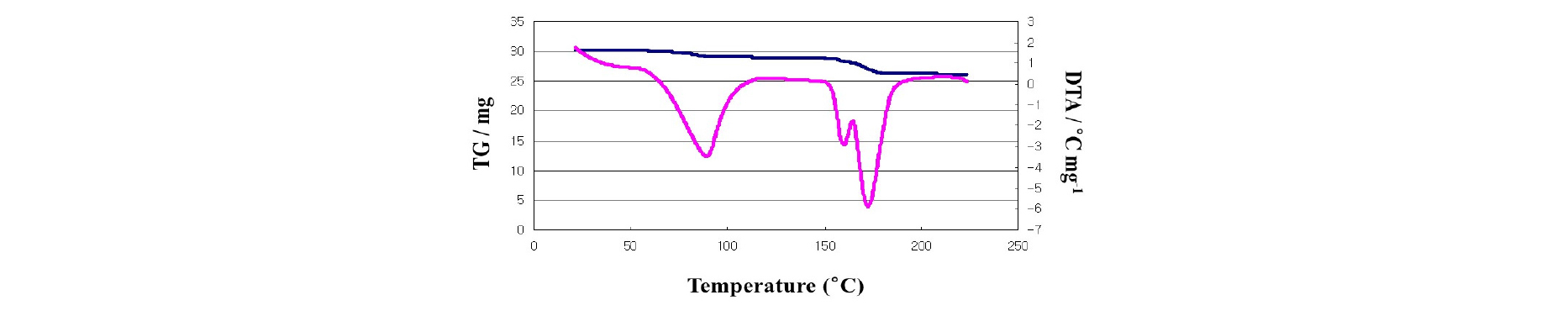
0.35 kmol m-3 NaOH 조건에서 회수된 산화제1동 분말을 용해하여 구리의 함량을 분석한 결과 77.1%이였으며 순수한 산화제1동 분말은 구리 함량이 88.8%이 되어야 한다. 산화제1동 분말의 열중량분석을 30oC에서 220oC로 변화시켜 수분의 거동을 관찰하였고 Fig. 9에 결과를 나타내었다. 두 흡열반응이 이 온도범위에서 나타났으며, 이것은 분말의 표면과 결정내에서의 수분이 증발하여 발생한 것을 알 수 있다. 이 증발된 수분의 양은 13%였고, 수분 증발량을 고려해 재계산을 수행한 구리의 함량은 88.6%로 시약급 산화제1동의 구리함량 88.8%에 근접한 것을 알 수 있었다.
결론
폐에칭액으로부터 구리를 산화제1동으로 회수하기 위한 재활용공정을 적용하였다. 우선, 구리성분은 폐에칭액에 구리분말을 투입하는 방식으로 염화구리분말로서 다른 불순물 금속이온으로부터 분리되어 회수되었다. 염화구리분말 중 구리함량은 63.9%로 나타났다. 다음 이 염화구리분말을 사용하여 수산화나트륨 용액과 반응시켜 산화제1동 분말을 제조하였다. NaOH의 농도가 0.35 kmol m-3일 때 생성된 산물의 XRD 결과는 산화제1동의 피크와 일치하는 것으로 나타났으며, 반응 후 수용액의 pH는 계산된 평형 pH 5.4에 근접한 것으로 판단되었다. 제조된 산화제1동 분말은 구리가 77.1%이고 수분이 13%인 것으로 분석되었다. 이 결과는 폐에칭액으로부터 산화제1동이 성공적으로 제조된 것을 나타내었다.