서 론
국내의 폐광산에는 그 주변으로 광물찌꺼기 및 폐(광)석이 잔재하고 있고, 대부분이 농경지와 인접한 곳에 존재한다. 따라서 광산 주변 토양과 농산물의 비소(As) 및 수은(Hg)오염 가능성은 비교적 높다(Kwon et al., 2020). 기존의 연구에서도 토양과 엽채류의 평균 수은 함량이 평야 지역보다 폐광산 지역이 높은 것으로 확인된 바 있다(Kim et al., 2002).
일반적으로 비소는 철산화물과 강한 친화력이 있어 비소오염 토양 내 높은 비율의 비소가 철산화물에 결합하여 존재하는 것으로 알려져 있다(Smedley and Kinniburgh, 2002). 국내에서는 비소 및 중금속 오염 토양을 정화하는 방법으로 입도분리(physical separation)와 화학적 추출(chemical extraction)을 통해 비소 및 중금속을 제거하는 토양세척법을 주로 적용하여 정화 사업을 수행하고 있다(Lee et al., 2009; Lee et al., 2020; Han, 2021). 아울러 수은을 함유한 대표적인 광물은 진사(Cinnabar, HgS)이지만 국내에서는 거의 존재하지 않는 것으로 알려져 있다. 그러므로 국내의 광산 주변에서 발견되는 수은 오염은 과거 아말감법에 의한 선광과정과 밀접한 관련이 있을 것이다(Jung et al., 2009). 국외의 연구자들도 아말감으로 금(Au)을 추출하기 위해 원소수은을 사용하는 것에 대해서 수은과 그 화합물로 인해 환경오염이 가중될 수 있다고 언급하였다(Brito and Guimaraes, 1999; Grandjean et al., 1999).
비소 오염토양을 대상으로 한 세척연구는 Gwon et al.(2020)이 폐광산 주변 토양을 대상으로 옥살산(Oxalic acid)를 이용하여 비소를 세척 후 비소의 존재형태 및 생물학적접근성을 평가한 바 있다. Kim and Baek(2014)은 제련소와 광산주변의 비소로 오염된 토양을 대상으로 염산(HCl), 질산(HNO3), EDTA 및 옥살산의 세척효과를 비교하였다. 국내외 연구에서 옥살산을 활용한 토양 내 비소 세척이 많이 다뤄지는 것은 다른 세척액에 비해 독성이 낮으며, 킬레이트 결합을 통한 철산화물 추출 효과가 다른 무기산들에 비해 높기 때문이다. 그러나 보다 근본적인 이유는 옥살산의 경우 식물이나 채소 등을 통해 자연적으로 발생할 수 있고, 생물학적 분해가 가능한 물질로 알려져있는 환경친화적인 세척액이기 때문이다(Panias et al., 1996; Lee et al., 2007; Lee et al., 2016; Wasay et al., 1998; Jones, 1998; Kim and Baek, 2015).
수은오염토양에 대한 세척연구도 Kwon et al.(2020)이 광산주변의 수은으로 오염된 토양을 대상으로 HCl, HNO3, 요오드화칼륨(KI) 등의 세척액을 사용하여 세척공정 실험을 실시하여 요오드화칼륨으로 세척 할 시 0.01 M의 낮은 농도로도 모든 입도조건에서 우수한 화학적 세척효율을 보이는 것을 확인하였다. 한편 국외에서는 Moreno et al.(2005)와 Moreno et al.(2004)은 티오황산나트륨(Na2S2O3), 티오황산염(Thiosulfate), 요오드화물 및 HNO3, 왕수(Aqua regia), HCl, 수산화나트륨(NaOH) 및 요오드화칼륨을 이용하여 토양에서 수은을 추출하는 연구를 수행하였다. Wasay et al.(1995)은 100 mM KI + 50 mM HCl(pH 1.5)의 용액으로 토양에 함유된 수은을 약 77%가량 제거하였으나 토양 특성 변화에 주의를 기울여야 한다고 평가하였다.
일반적으로 #200 이하(≤ 0.074 mm)의 입도를 가진 토양은 세척과정에 경제성을 고려하여 물리적인 선별을 통해 슬러지로 폐기되는 것이 일반적이다(Ko et al., 2004). 하지만 점토질 토양은 입경이 미세한 입자로 넓은 표면적을 가지고 있어서 양분의 흡착·고정·방출·산도·토양반응·통기성·투수성 등 이화학성을 결정하는 중요한 요소이다(Cho et al., 2013). 따라서 이와 같은 물리적 선별에 의한 실트 및 점토질 토양의 손실은 농경지 토양으로의 복원차원에서 농작물의 생장에 악영향을 미칠 것으로 예상된다. 이러한 이유로 과거 광산활동에 따른 영향으로 인하여 비소 및 수은이 복합적으로 오염되어 있는 광산주변 농경지 토양의 경우 농경지복원 차원에서 실트 및 점토질 토양을 폐기 처리하지 않고 정화하는 과정이 필요하다.
본 연구에서는 폐금속광산 인근 오염 농경지 중 비소와 수은에 의해 복합적으로 오염된 농경지토양을 대상으로 통상적인 세척과정과는 달리 물리적 선별과정을 배제한 토양세척 공법연구의 실용가능성을 확인하고자 하였다. 또한 추후 비소 및 수은 복합오염된 농경지 토양의 순차적인 세척액 적용을 통한 물리적 선별과정이 없는 토양세척공법 연구를 위한 기초자료를 획득하는데 목적이 있다.
연구 방법
연구 지역
연구대상 광산은 충청남도 천안시에 위치한 일보광산으로 과거 갱구 1개소, 폐시설 4개소, 폐석장 1개소 및 광물찌꺼기 적치장 1개소가 존재하였으나, 현재 폐시설 1개소만 남아있는 상태이다. 광산일대는 천보, 중앙, 천안제일, 호미 및 신호미 등 다수의 광산이 개발되어 인근 토양을 오염시키는 광해요소가 산재되어 있는 실정이다(Lim et al., 2015).
본 연구의 세척실험 대상토양은 일보광산 주변의 농경지로 광산활동의 영향을 받은 수은 및 비소 복합오염 토양으로 선정하였다. 시료채취 당시 농경지는 휴경상태였으며 인근 농경지는 과수원으로 사용되고 있었다. 광산활동의 영향을 받은 농경지는 폐광석 및 광물찌꺼기의 영향을 많이 받았을 가능성이 높다. 폐광석에 포함된 비소와 광물찌꺼기에 표면에는 아말감법 선광작업에 사용된 수은 이 선광 후 잔류 및 흡착되어 있기 때문에 주변 토양에 영향을 줄 가능성이 높다.
오염도 분석
본 연구대상지의 비소 및 수은 오염확인을 위해 대상토양의 토양 pH 분석 및 오염원소에 대한 전함량 분석을 실시하였다. 토양 내 오염원소 분석은 토양오염 공정시험법인 왕수법(Aqua regia)으로 추출하여 대상지의 비소 및 수은의 농도를 분석하였다.
입도 분석
대상 토양을 입도분포 확인을 위해 ASTM(American Society of Testing Materials) 규격의 표준체를 활용한 입도분석을 실시하였다. 사용한 체눈크기는 #10(2.000 mm), #20(0.841 mm), #40(0.420 mm), #60(0.250 mm), #100(0.149 mm), #200(0.074 mm)이었다. 입도분석은 최상부로부터 증류수를 주입하는 방식인 습식입도분리를 통하여 #10 ~ #20, #20 ~ #40, #40 ~ #60, #60 ~ #100, #100 ~ #200, #200 이하의 총 6 개의 입도구간을 분리하고, 자연건조하여 수분을 제거 후 각 입도구간별 시료의 무게(g)을 측정하여 구성비(wt%)를 산정하였다. 각 입도구간별 시료와 함께 입도구간별 구성비(wt%) 산정에 따라 혼합시료를 제작하여 원토양 시료로 사용하였다.
세척 실험
복합오염토양에서 비소 세척에 높은 효율을 나타내는 옥살산과 수은 세척에 높은 효율을 보이는 요오드화칼륨 용액을 사용하여 토양세척 시험을 진행하였다. 또한 농경지 토양복원이 가능한 세척공법의 적용을 위하여 입도구간별 및 원토양(raw)에 대해서도 실험을 진행하였다(Table 1).
Table 1.
Experimental steps in soil washing method as unit processed
옥살산 용액은 옥살산 powder를 0.2 M의 농도가 되는 양을 정량하여 증류수와 충분히 혼합 후 세척액으로 사용하였다. 또한 요오드화칼륨 용액은 요오드화칼륨 powder를 0.01 M의 농도로 정량하여 증류수와 충분히 혼합시킨 후 염산(HCl)을 소량 첨가하여 pH를 1.5로 조절한 것을 세척액으로 하였다.
시료는 5 g씩 정량한 것으로 입도구간별 토양 6개 시료와 입도구간별 구성비를 고려하여 혼합한 원토양시료 1개이다. 본 연구는 물리적 선별을 거치지 않은 농경지 토양 대상의 토양세척법 적용을 위해 체질을 하지 않은 #10 이하의 토양시료에도 토양세척 실험을 진행하고자 하였다. 하지만 실험실 규모에서는 시료로 5 g의 소량을 사용하기 때문에 시료의 대표성을 확보하기 어려운 문제가 있었다. 이러한 이유로 구성비를 고려하여 입도별 토양을 인위적으로 혼합한 원토양 시료를 제조하였다. 이를 통하여 입도구간별 세척효율 및 입도분리를 하지 않은 원토양에 대한 토양세척 공법의 적용가능성을 평가하고자 하였다.
세척조건의 경우 입도구간별 시료 및 원시료가 5 g씩 적재된 코니컬 튜브에 옥살산은 고액비 1(토양) : 3(세척액)의 비율로 주입하고, 요오드화 칼륨은 고액비 1(토양) : 5(세척액)의 비율로 세척액을 주입한 후 회전식 교반기에서 20 rpm으로 60 min 동안 세척하였다. 세척과정 종료 후 원심분리를 통해 잔류토양과 세척액을 분리 및 회수하였다.
이후 회수된 잔류토양에 남아있는 세척액에 의한 비소 및 수은이 토양으로 재흡착되는 것을 방지하기 위하여 증류수를 넣고 교반 후 원심분리기로 3,000 rpm으로 15 분간 고액분리를 하는 과정을 5회 반복하여 잔류토양에 포함된 세척액을 제거하였다. 최종 처리한 시료는 상온에서 완전건조하여 분석시료로 하였다.
시료 분석
세척 전 토양과 세척공법을 적용 후 회수한 잔류토양을 대상으로 국내 토양오염공정시험법인 왕수법(Aqua regia)로 추출하여 비소 및 수은의 세척 전후의 농도를 분석하였다. 단, 세척 후 토양은 입도구간별 시료임을 감안하여 #100로 체거름을 하지 않고 왕수 용출을 실시하였다. 건조 후 #100 이하로 체질이 완료된 토양시료 0.25 g에 왕수(HNO3 : HCl = 1 : 3) 4 mL을 주입한 후, 마이크로파 분해법을 이용하여 용출하였다. 반응 후 3차 증류수 6 mL을 주입하고 0.45 µm cellulose acetate filter로 필터링하여 중금속을 분석하였다. 분해액을 취하여 여과한 후 분석용 시료로 하였다. 전처리가 완료된 시료는 ICP-OES(model 8300, Perkin Elmer inc.)를 이용하여 분석하였다.
연구 결과
오염원소 분석 결과
대상토양의 토양 pH 분석 및 왕수법(Aqua regia)로 추출하여 분석을 실시한 결과는 Table 2와 같다. pH는 8.7로 약알칼리성을 나타내고 있었으며, 비소는 1,113 mg/kg으로 매우 고농도로 오염되어 있는 것으로 확인되었다. 수은의 경우 3.65 mg/kg으로 토양오염우려기준인 4.0 mg/kg의 약 91% 수준인 것으로 나타나 과거 광산영향을 받은 농경지인 것으로 판단하고 실험대상 토양으로 사용하였다.
Table 2.
Chemical composition of control soil
| ID | pH |
As (mg/kg) |
Cd (mg/kg) |
Cu (mg/kg) |
Pb (mg/kg) |
Zn (mg/kg) |
Ni (mg/kg) |
Hg (mg/kg) |
| Control | 8.7 | 1,113.15 | N.D | 14.6 | 60.5 | 142.3 | 9.9 | 3.65 |
입도 분석 결과
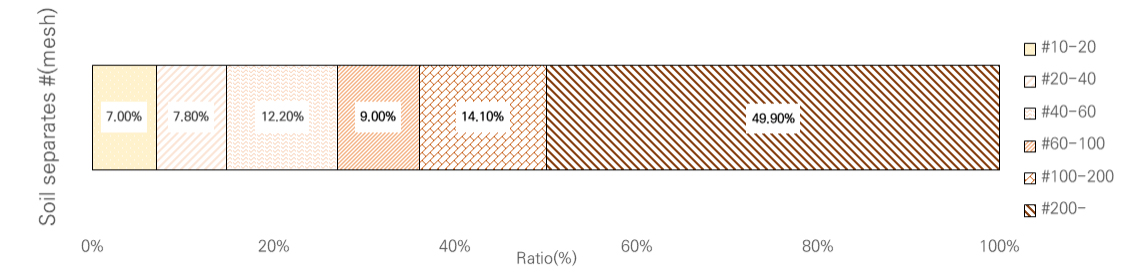
대상토양의 입도분석 결과를 6개 입도구간별 구성비(wt%)로 산정하여 Fig. 1에 도식하였다. 분석대상 토양은 #200 이하(≤0.074 mm)가 전체의 49.9%를 차지하고 있었으며, #100(0.149 mm) ~ #200(0.074 mm) 구간이 14.1%, #40(0.420 mm) ~ #60(0.250 mm) 구간이 12.2%, #60(0.250 mm) ~ #100(0.149 mm) 구간이 9.0% 등으로 구성되어 있었다.
토양세척기술을 적용함에 있어 입도에 따른 세척효율을 고려할 때 과립의 토양 입자의 세척 후, 실트 크기(≤0.074 mm) 이하의 미세토양은 물리적 분리 제거대상으로 구분하고 있다(Ko et al., 2004). 물리적 분리 및 제거는 점토와 미사 함량이 30 ~ 50% 미만인 토양에 보다 적절하고 비용 효과적인 것으로 알려졌다(Dermont et al., 2008; U.S. EPA, 1997). 하지만 본 연구에서 사용된 시료를 대상으로 통상적인 토양세척법을 적용할 시에 전체의 약 50%가 슬러지 형태로 폐기되게 된다. 이는 농경지 토양에서 식생 성장에 필요한 실트 및 점토질 토양이 대부분 손실되는 것을 의미한다. 따라서 광산주변의 비소 및 수은오염 농경지 토양에 세척기술을 적용할 때에는 입도분석을 실시하여 물리적 분리 제거의 실효성 검토가 선행되어야 하며, 실트 및 점토질 토양이 우세한 토양일 경우에는 미세입자에 높은 효율을 갖는 화학적 세척액 선정이 중요할 것이다.
세척토양 분석 결과
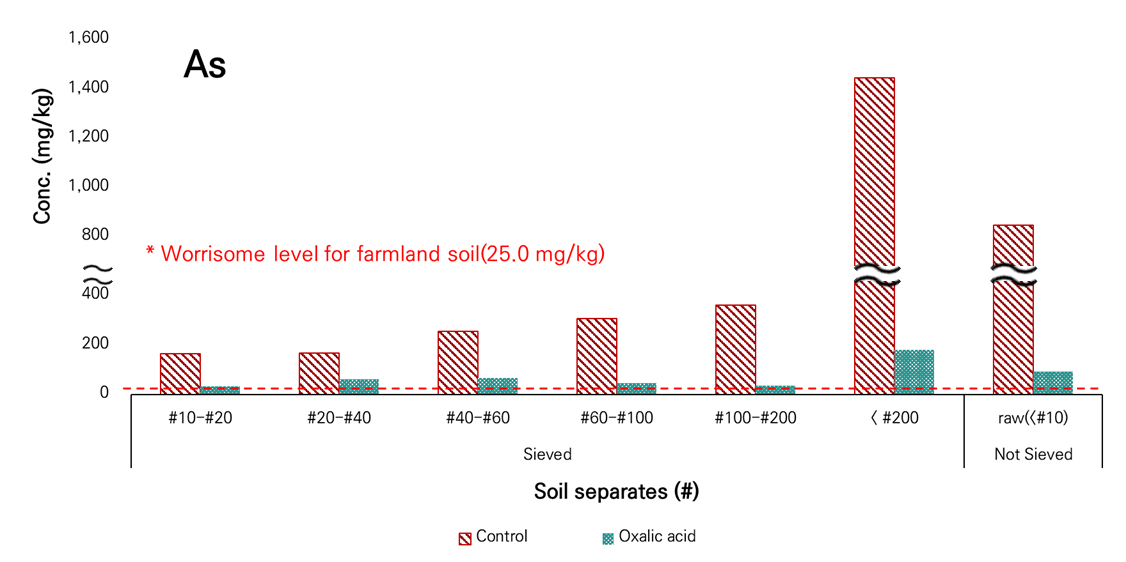
Table 3은 토양 내 비소를 대상으로 옥살산을 이용하여 입도구간별 시료 및 원토양를 대상으로 토양세척공법을 적용하고 세척 후 토양의 잔류 비소를 분석한 것이다. Fig. 2는 분석결과를 그래프로 나타내어 세척효율을 분석하였다.
Table 3.
As concentrations in the washed soil (unit: mg/kg)
| As | Control | Oxalic acid | |
| Sieved | #10‒#20 | 167.25 | 33.48 |
| #20‒#40 | 170.14 | 63.41 | |
| #40‒#60 | 257.14 | 67.42 | |
| #60‒#100 | 308.89 | 47.71 | |
| #100‒#200 | 364.14 | 36.98 | |
| < #200 | 1447.59 | 182.59 | |
| Not Sieved | raw (<#10) | 848.94 | 93.01 |
0.2 M 옥살산 용액은 비소를 목적원소로 하는 세척액으로 모든 입도구간에서 높은 제거효율을 보였다. 특히 #200 이하 및 원토양(raw) 시료에서도 각각 87%, 89%의 제거율을 보여 실트 및 점토질 토양에서도 높은 세척효율을 나타내었다. 이러한 결과는 토양세척에 유기산인 옥살산을 이용하였을 때 옥살레이트(oxalate, C2O4-)가 철(Fe)과 강한 킬레이트를 형성하고 약한 환원반응에 의해 토양 중 철산화물을 용출시키며 철과 결합되어 있는 비소를 추출했기 때문으로 해석된다. 옥살산을 이용한 토양 세척이 비결정질 철산화물에 결합되어 있는 비소의 추출에 효과적이라는 선행연구들과 유사한 결과를 나타낸 것이다(Lee et al., 2016; Kim and Baek, 2014).
하지만 본 연구결과에서 세척완료 토양의 잔류 비소 농도가 33.48 ~ 182.59 mg/kg으로 토양오염 우려기준(농경지, 25 mg/kg)을 만족하지는 못했다. 이는 세척액의 높은 세척효율에도 불구하고 연구 대상토양의 초기 비소가 167.25 ~ 1,447.59 mg/kg으로 고농도로 함유되어 있었기 때문에 투입한 세척액의 용출한계를 넘어섰던 것으로 해석된다. 따라서 추후 세척공정을 적용할 시에는 사전에 대상토양에 대한 전함량 분석을 통하여 초기농도가 높을 경우에는 세척액의 고액비를 조정하거나, 추가 세척공정을 배치하는 과정이 필요할 것으로 사료된다.
일반적으로 토양세척의 경우 #200 이하의 미세토양에서 반응성이 높은 점토광물과 산화물의 양이 증가하면서 중금속이 토양에 강하게 결합하여 존재하기 때문에 미세토양 중 중금속의 추출 효율은 감소한다. 하지만 광산토양의 경우에는 반대로 토양입경이 작아지면서 추출효율이 증가하게 되는데, 이는 광산토양 중 Arsenolite 광물 형태의 비소가 토양입경이 작아지면서 옥살산과의 반응표면적이 증가함에 기인한 것으로 연구되었다(Gwon et al., 2020). 따라서 본 연구 대상지와 같은 광산활동의 영향을 받은 농경지 토양의 경우에도 이와 유사한 경향이 있을 것으로 사료된다.
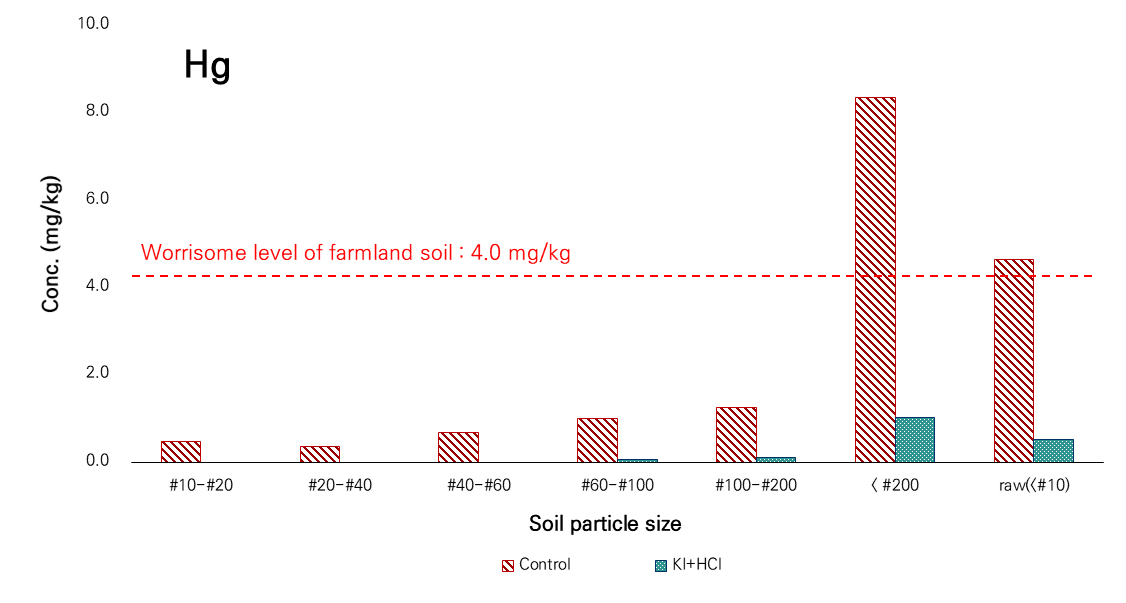
Table 4는 토양 내 수은을 대상으로 요오드화칼륨을 이용하여 입도구간별 시료 및 원토양(raw)를 대상으로 토양세척공법을 적용하고 세척 후 토양의 잔류 수은 분석한 결과이다. Fig. 3은 분석결과를 그래프로 나타내어 세척효율을 분석하였다.
Table 4.
Hg concentrations in the washed soil (unit: mg/kg)
| Hg | Control | KI+HCl | |
| Sieved | #10‒#20 | 0.47 | N.D |
| #20‒#40 | 0.36 | N.D | |
| #40‒#60 | 0.67 | N.D | |
| #60‒#100 | 0.99 | 0.07 | |
| #100‒#200 | 1.25 | 0.12 | |
| < #200 | 8.35 | 1.03 | |
| Not Sieved | raw (<#10) | 4.64 | 0.51 |
0.01 M 요오드화칼륨 용액은 수은을 목적원소로 하는 세척액으로 모든 입도구간에서 높은 제거효율을 보였다. #10 ~ #60의 입도구간에서는 수은이 100% 제거되었으며, #60 ~ #100 구간에서 93%, #100 ~ #200에서 91%의 농도저감이 확인되었다. #10 ~ #200 구간의 수은 농도는 0.36 ~ 1.25 mg/kg으로 저농도의 수은이 세척된 결과이다. 아울러 #200 이하의 토양에서는 8.35 mg/kg의 수은이 1.03 mg/kg으로 88%의 농도저감이 확인되었다. 특히, 원토양 시료에서도 4.61 mg/kg에서 0.51 mg/kg으로 89%의 높은 제거율을 나타내었다. 특히 수은이 토양오염 우려기준(농경지, 4 mg/kg)을 초과하던 #200 이하 및 원토양 시료에서 세척결과 환경기준을 만족하는 농도까지 저감되었음을 확인하였다.
이와 같은 요오드화칼륨의 세척효율은 HgI42-가 pH 2 이하에서 형성하는 것과 같이 낮은 pH에서 요오드화물 이온이 가용성 복합체를 형성하는데, 요오드화물 이온보다 HgI42-의 안정성 상수(29.8)가 높기 때문에 수은에 대한 우수한 세척 효율을 나타내는 것으로 해석된다(Wasay et al., 1995; Smith and Martell, 1976).
본 연구 결과에서 비소와 수은 오염토양을 각각의 세척액을 적용하여 토양세척 시 모든 입도에서 제거효율이 좋은 것으로 나타났다. 특히 #200 이하의 입도시료 및 물리적 선별을 하지 않은 원토양 시료에서도 높은 제거효율을 보이는 것을 확인하였다. 이는 추후 비소 및 수은오염 농경지 토양을 대상으로 토양세척공정을 적용할 때 옥살산과 요오드화칼륨을 적용한 물리적 선별을 거치지 않는 토양세척 공정연구의 가능성을 시사한다. 또한 본 연구결과는 비소 및 수은으로 복합오염된 농경지 토양에 대해서 각각의 세척액을 사용한 세척과정을 순차적으로 배치하는 방식으로 공정을 고안하는 등의 추후 연구에도 기초자료로 활용될 수 있을 것으로 사료된다. 다만, 일부 입도구간에 오염물질이 분포해 있는 경우 토양세척 공법 적용 시 경제성 측면에서 선택적인 물리적 선별은 필요할 것으로 판단된다. 본 연구대상 부지와 같은 경우 #200 이하의 입도구간에서만 수은이 환경기준을 초과하고 있는 것으로 나타났다. 따라서 물리적 선별과정을 통해 #200 이하의 토양을 대상으로만 요오드화 칼륨을 적용한 세척공법을 적용하면 대상토양의 부피를 감소시켜 경제적 효율성도 확보할 수 있을 것으로 기대된다. 이와 같은 추후 연구를 통해서 비소와 수은으로 복합 오염된 농경지토양을 대상으로 물리적 선별과정 없이도 정화 및 복원을 할 수 있을 것으로 기대된다.
결 론
본 연구는 광산주변 농경지 중 비소와 수은에 의해 복합적으로 오염된 농경지 토양 복원을 위해 통상적인 세척과정과는 달리 물리적 선별과정이 불필요한 토양세척 방안을 연구하고자 하였다.
비소 및 수은오염 농경지 토양을 대상으로 옥살산 및 요오드화칼륨을 세척액을 사용하여 각각 토양세척공법을 적용한 결과, 모든 입도구간에서 토양 내 비소 및 수은에 대해서 80% 이상의 세척효과를 보였다. 특히, #200 이하의 입도 토양과 입도구성비를 고려하여 혼합한 원토양에서도 비소와 수은 모두 87% 이상 제거되는 것을 확인하였다.
이와 같은 결과는 광산주변 비소 및 수은오염 농경지 토양을 대상으로 물리적 선별과정 없이 세척공정을 적용하더라도 높은 제거효과를 기대할 수 있다는 것을 의미한다.
다만, 본 연구지역의 수은과 같이 오염물질이 특정 입도구간에 집중적으로 분포하는 경우에는 선택적인 물리적 입도선별을 통해 토양세척 공법을 적용하여 경제성에 대한 고려할 필요가 있을 것으로 사료된다.
본 연구결과는 비소 및 수은오염 농경지 토양을 정화 및 복원하기 위하여 통상적인 세척과정과는 달리 물리적 선별과정 없는 토양세척 공법의 가능성을 확인하였다. 이는 추후 옥살산과 요오드화칼륨을 순차적으로 세척과정을 배치하는 방식의 공정에 대한 연구의 기초자료로 활용될 것이다. 또한 관련 세척공법에 대한 최적공정 적용성 연구가 수행된다면 효과적으로 폐광산 인근의 복합오염 농경지 토양을 정화 및 복원하는데 기여할 것으로 기대된다.