서 론
연구내용 및 방법
시료채취 및 분석
물리적 선별(Physical Separation)
토양세척(Soil Washing)
연속추출(Sequential Extraction)
결과 및 고찰
오염토양 실험 결과
자력 선별 제거효율 규명
부유 선별 제거효율 규명
토양세척 실험 결과
단계별 토양세척 분석 결과
결 론
서 론
토양은 생태계 유지와 인간 생활에 필수적인 자원으로 농업 생산과 환경보호에서 중요한 역할을 한다. 그러나 자연적인 요인과 인위적인 다양한 활동으로 인해 토양 오염이 점차 심화되고 있으며, 그 중에서도 비소 오염은 심각한 환경 문제로 주목받고 있다(Kwon and Hong, 2023). 비소는 암석과 광물의 분해와 침전을 통하여 토양과 물에 분산되거나(Luong et al., 2007), 광산활동, 농업활동, 목재방부재 소비 및 식품 첨가물로부터 증가된다(Aldrich et al., 2007). 비소의 이동도와 용해도는 화학적 형태와 종류에 따라 의존하며, 비소 3가는 이동도가 높아, 비소 5가 보다 독성이 높은 것으로 알려져 있다(Caruso et al., 2001). 국제암연구소(IARC)는 비소를 1급 발암 물질로 지정하고 있으며, 방광암, 신장암, 피부암 및 간암을 유발할 가능성이 있는 것으로 보고하였다(IARC, 2012; Chappell et al., 1997). 또한 장기간 노출될 경우 백혈구 감소증과 같은 혈액 질환을 유발하며, 난청 사례도 확인되는 것으로 나타났다(Tchounwou et al., 2003; Guo et al., 2007).
국내에서는 비소 및 중금속 오염토양을 정화하는 방법으로 입도분리(Physical separation)와 화학적 추출(Chemical extraction)을 통해 비소 및 중금속을 제거하는 토양세척법을 주로 적용하여 정화를 수행하고 있으며(Lee et al., 2020; Han, 2021), 그 외로 동전기공법(Park et al., 2013; Lee et al., 2009) 및 열탈착공법(Kim, 2011; KMOE, 2012) 등이 적용되었다. 비소 오염토양을 대상으로 한 세척연구로서 Im et al.(2015)과 Wang et al.(2017)은 염산과 인산을 사용하였으며, Qiu et al.(2010)은 킬레이트제인 EDTA를 이용하여 연구를 수행하였다. Beiyuan et al.(2017)은 알칼리성 용매(NaOH 및 Na2CO3)를 이용하여 비소를 세척한 후 비소의 존재형태 및 생물학적 접근성을 평가하였다. 또한 국내·외에서 옥살산을 이용한 연구가 많이 이루어지고 있으며, 이는 다른 세척액에 비해 독성이 낮고 생물학적 분해가 가능한 물질로 알려져 있는 환경 친화적인 세척액이기 때문이다(Lee et al., 2016; Wei et al., 2016).
토양세척과 관련된 주 연구는 세척제 종류(Im et al., 2015; KEITI, 2016), 혼합비율(Lin et al., 2017; Kim, 2017), 세척제 농도(Wang et al., 2017; Choi, 2006) 및 세척시간(Zhao et al., 2016; Jho et al., 2015) 등의 조건들을 고려한 것이 대부분이다. 다만 기존 연구들의 경우, 주로 세척제의 종류와 조건에 초점을 맞췄으며, 비소의 화학적 존재형태에 대한 고려는 미흡한 것으로 조사되었다. 일반적으로 비소는 철산화물과 강한 친화력이 있어 비소오염 토양 내 높은 비율의 비소가 철산화물에 결합하여 존재하는 것으로 알려져 있어(Smedley and Kinniburgh, 2002), 비소의 존재형태를 확인하는 것이 중요하다. 대표적으로 비소의 화학적 존재형태는 Wenzel et al.(2001)의 연속추출법에 따라 총 5가지로 구분되며 특히 4, 5단계의 경우 결합력이 매우 강하며, 주로 황비철석(Arsenopyrite, FeAsS)과 같은 광물의 형태로 존재하기 때문에 일반적인 토양세척만으로는 효과적으로 제거하기 어렵다(Smedley and Kinniburgh, 2002). 따라서 이러한 형태의 비소를 효과적으로 제거하기 위해서 물리적 선별 과정이 필요하다. 물리적 선별 방법은 대표적으로 자력 선별과 부유 선별이 있으며, 자력 선별은 철과 같이 자성이 강한 광물에 결합된 비소를 분리하는데 효과적이며, 부유 선별은 유비철석과 같은 소수성 형태 광물에 결합된 비소를 분리하는데 유용하다(Oberteufferm, 1974; Jeong et al., 2006).
따라서 본 연구에서는 화학적으로 강하게 결합되어 일반적인 토양세척만으로는 제거가 어려운 주로 Fraction 4(결정질 산화물)와 Fraction 5(잔류상) 형태로 존재하는 비소 오염 토양을 대상으로 다양한 세척제를 활용하여 토양세척을 통한 제거 효율을 비교, 평가하였을 뿐만 아니라, 물리적 선별(자력 선별 및 부유 선별)의 제거 효율을 함께 평가하여 이를 통해 토양 내 비소의 결합 형태별 제거 가능성을 살펴보았다.
연구내용 및 방법
시료채취 및 분석
시료채취는 비소로 오염된 경기도 소재 체육시설을 대상으로 수행하였으며, 시료는 중농도(Sample A, 60 mg/kg 내외)와 고농도(Sample B, 200 mg/kg 내외)를 대상으로 총 두 지점에서 각각 20 kg 이상을 채취하였다. 해당 연구지역은 체육시설 전체가 아닌 일부 구역에서만 높은 비소 농도를 보이고 있어 외부에서 유입된 것으로 판단되며, 정확한 유입 정황은 확인할 수 없었다. 채취한 시료는 상온에서 풍건한 후 10 mesh(<2 mm) 이상의 입자는 제거한 후 균질화 하였으며, 국내 토양오염공정시험기준에 따라 왕수분해법을 적용하여 비소의 총 함량을 분석하였다. 왕수분해법은 100 mesh(<0.15 mm)로 체질한 건조시료 3.0 g을 잰 후, 질산(7.0 mL)과 염산(21 mL)을 넣은 후 heating block에서 70°C을 유지하면서 1시간 동안 용출한 용액(KMOE, 2022)을 원자흡수분광광도계(Varian, 호주)를 활용하여 분석하였다.
물리적 선별(Physical Separation)
자력 선별 실험은 10,000 및 14,000 가우스(Gauss) 영구자석을 사용하여 1회 진행하였다. 입도범위 2–0.075 mm의 중농도와 고농도 시료(각 2개씩 총 4개)를 고액비 1 : 5로 혼합한 후, 습식상태에서 영구자석으로 30×35 cm 면적의 트레이에서 총 20회 왕복하여 선별하였다.
부유 선별 실험은 부유 효율 감소와 미립자의 동반부유를 막기 위해 0.5–0.075 mm 입도 범위의 시료를 대상으로 1회 실험하였으며(Wills and Finch, 2016), 공기 유량 조절기가 부착된 Sub-A형 부선기(KHD Humboldt Wedag AG)를 사용하여 실시하였다. 오염 토양 슬러리를 부선 Cell에 넣고 동일 실험 조건에서 포수제의 종류를 Potassium Amyl Xanthate(P.A.X)와 Potassium Ethyl Xanthate(P.E.X)로 하고 투입량(100 g/t, 200 g/t)을 다르게 하여 실험을 진행하였다.
토양세척(Soil Washing)
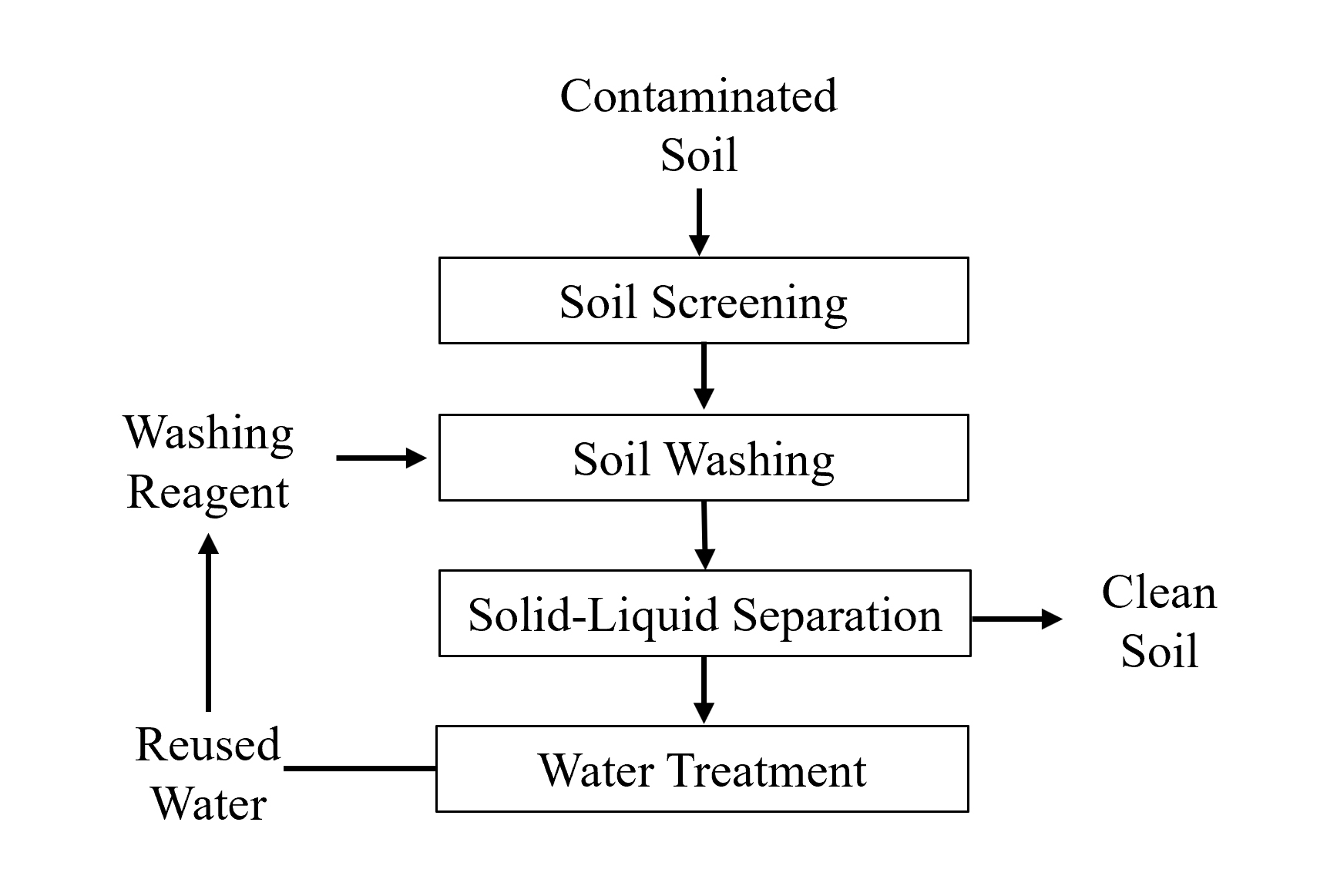
토양세척 실험은 2–0.075 mm와 2–0.15 mm의 입도 범위로 나누어 각 입도별 세척 효율을 평가하였고, 세척액으로 옥살산(Oxalic acid, C2H2O4), 옥살산 + 디씨오나이트(Dithionite, Na2S2O4) 혼합 용액, 아스코빅산(Ascorbic acid, C6H8O6), 인산(Phosphoric acid, H3PO4), 황산(Sulfuric acid, H2SO4) 및 증류수(Deionized water) 등 총 6가지 세척액을 사용하였으며, 증류수를 제외한 모든 세척액은 각각 0.2 M과 0.5 M의 농도로 제조하여 세척제의 종류 및 농도에 따른 제거율 변화를 평가하였다. 실험은 1회 진행하였으며, 토양세척공정의 기본적인 흐름도를 Fig. 1에 정리하였다. 토양과 세척액의 고액비는 1 : 5로 적용하여 교반속도 150 rpm에서 24 시간 동안 세척하여 진행하였다. 또한, 토양세척 실험에서 연속추출 3단계와 4단계에서 가장 높은 제거율을 보인 옥살산과 디씨오나이트 혼합 용액과 잔류상 형태 비소에서 가장 높은 제거율을 보인 아스코빅산을 단계별로 적용하여 그 효율을 평가하였다(Table 1).
Table 1.
Overview of the physical and chemical separation methods applied in this study
연속추출(Sequential Extraction)
토양 내 비소의 존재형태를 평가하기 위하여 Wenzel et al.(2001)의 연속추출법을 적용하여 분석하였다. 이에 따른 분획특성을 단계별로 정리하면 이온교환형태(Fraction 1), 강하게 흡착된 형태(Fraction 2), 비결정질 산화물과 결합된 형태(Fraction 3), 결정질 산화물과 결합된 형태(Fraction 4) 및 잔류상 형태(Fraction 5)로 구분되며 추출 방법은 Table 2에 정리하였다.
Table 2.
Procedure of the sequential extraction method for arsenic in soils (Wenzel et al., 2001)
| Fraction | Extractable phase | Chemical extractions | Reference |
| I | Non-specifically bound | 0.05 M (NH4)2SO4 | Wenzel et al.,2001 |
| II | Specifically bound | 0.05 M (NH4)H2PO4 | |
| III | Amorphous Fe-Al oxide bound | 0.2 M NH4-oxalate buffer (pH 3.25) | |
| IV | Crystalline Fe-Al oxide bound |
0.1 M ascorbic acid + 0.2 M NH4-oxalate buffer(pH 3.25) | |
| V | Residuals | Aqua regia (HCl:HNO3 = 3:1) | KMOE, 2022 |
결과 및 고찰
오염토양 실험 결과
오염토양 중농도(A), 고농도(B) 시료에 대해서 입도별 분석 결과를 Table 3에 정리하였다. 분석결과, 중농도(A) 시료의 경우 63.1 mg/kg으로 토양오염 1지역 우려기준(25 mg/kg)의 약 2.5배 초과하는 농도로 확인되었으며, 고농도(B) 시료는 209.8 mg/kg으로 토양오염 1지역 대책기준(75 mg/kg)을 초과하는 농도로 확인되었다. 국내 토양 내 비소 농도의 평균값(5.6 mg/kg)에 비해 각각 약 10배와 40배 정도 높은 값을 보였으며(Public Data Portal, 2025), 이는 2013년 조사된 국내 금속광산 지역의 비소 농도 평균값(47.4 mg/kg)에 비해 각각 약 1.5배와 4.5배 정도 높은 농도로 확인되었다(KMOE, 2013). 입도별 농도 값의 경우 입도가 작아질수록 비교적 높은 농도로 확인되었으며, 특히 0.5–0.075mm에서 가장 높은 농도로 나타났다.
Table 3.
Total concentrations of arsenic in different particle size fractions of the soil samples
| Sample ID | Particle Size | Concentration (mg/kg) |
| A1) | >0.15 mm | 63.1 |
| A-1 | 2–0.075 mm | 59.1 |
| A-2 | 2–0.15 mm | 60.9 |
| A-3 | 0.5–0.075 mm | 68.9 |
| B2) | >0.15 mm | 209.8 |
| B-1 | 2–0.075 mm | 194.6 |
| B-2 | 2–0.15 mm | 198.7 |
| B-3 | 0.5–0.075 mm | 292.6 |
실험용 시료들에 대한 연속 추출 결과를 Table 4에 정리하였다. 회수율 100%를 기준으로 확인한 결과 98–114%로 적절한 결과를 얻었으며, 두 시료 모두 Fraction 4(결정질 산화물)와 5(잔류상) 형태의 비소가 80% 이상의 높은 비율로 매우 강한 결합으로 존재하고 있었다.
Table 4.
Sequential extraction of the arsenic fractions from the soil samples (mg/kg)
See Table 3 for an explanation of the abbreviations
자력 선별 제거효율 규명
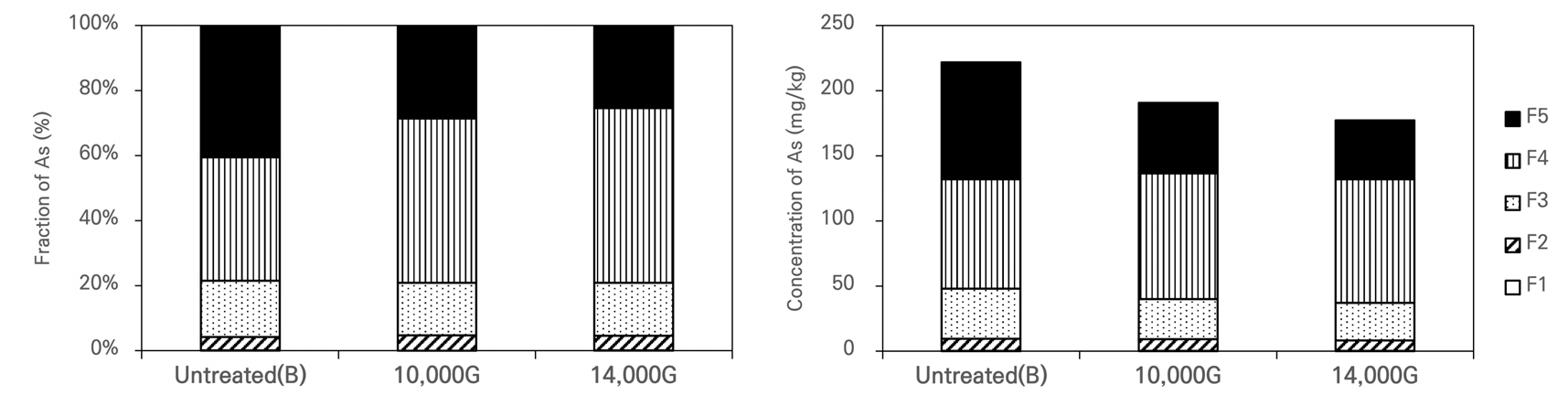
자성(10,000 G, 14,000 G)이 다른 2개의 자석막대를 사용하여 오염토양으로부터 금속물질을 제거한 후 중금속 농도를 분석한 결과는 Table 5에 나타내었다. 자력 선별 결과, 중농도(A-1) 시료에서는 초기 농도보다 다소 높은 값을 보여 선별 효율이 없는 것으로 확인되었다. 이는 자력 선별 과정에서 비소를 함유하지 않은 자성물질이 제거됨으로써, 잔류 시료의 단위 질량당 비소의 농도가 상대적으로 증가했을 가능성으로 해석된다. 반면, 고농도(B-1) 시료에서는 선별 전 초기 농도와 비교하여 10,000 Gauss 영구자석으로 선별 시 6.8%가 감소하였고, 14,000 Gauss 영구자석으로 선별하였을 때, 10.4%가 감소하였다. 이는 Kim(2018)과 Park(2015)의 연구에서 보고된 10% 내외 수준의 제거율과 유사한 결과이며, 또한, 고농도 시료에 대해 자력 선별 전·후 비소 연속추출 결과 10,000 Gauss 및 14,000 Gauss 영구자석 조건에서 모두 잔류상 형태(Fraction 5)에서 각각 39.5%, 50.0%로 제거율을 보이는 것으로 확인되었다(Fig. 2). 이는 일반적으로 잔류상 형태의 비소는 주로 황비철석과 같은 비자성 광물에 포함되어 있어 자력 선별만으로 제거되기 어렵다는 점에서 다소 비일관적으로 해석될 수 있다. 이에 따라 본 연구에서는 자성 물질 뿐만 아니라 이들과 결합되어 존재하거나 흡착된 형태의 비소 함유 입자들이 함께 제거되었을 가능성을 고려하고자하였다. 일부 비소는 자철석(Magnetite)이나 기타 약자성 광물에 흡착된 혼합 형태로 존재할 수 있는데, 이들이 자력 선별을 통해서 제거되면서 잔류상 형태의 비소가 함께 제거되었을 가능성이 있는 것으로 해석된다(Parviainen et al., 2012).
Table 5.
Soil arsenic concentrations after the magnetic separation process (mg/kg)
| 10,000 G | 14,000 G | |
| Initial concentration | 59.1(A-1)/194.6(B-1) | |
| After magnetic separation (A-1) | 90.1(‒)* | 70.8(‒) |
| After magnetic separation (B-1) | 181.3(6.8) | 174.4(10.4) |
See Table 3 for an explanation of the abbreviations
부유 선별 제거효율 규명
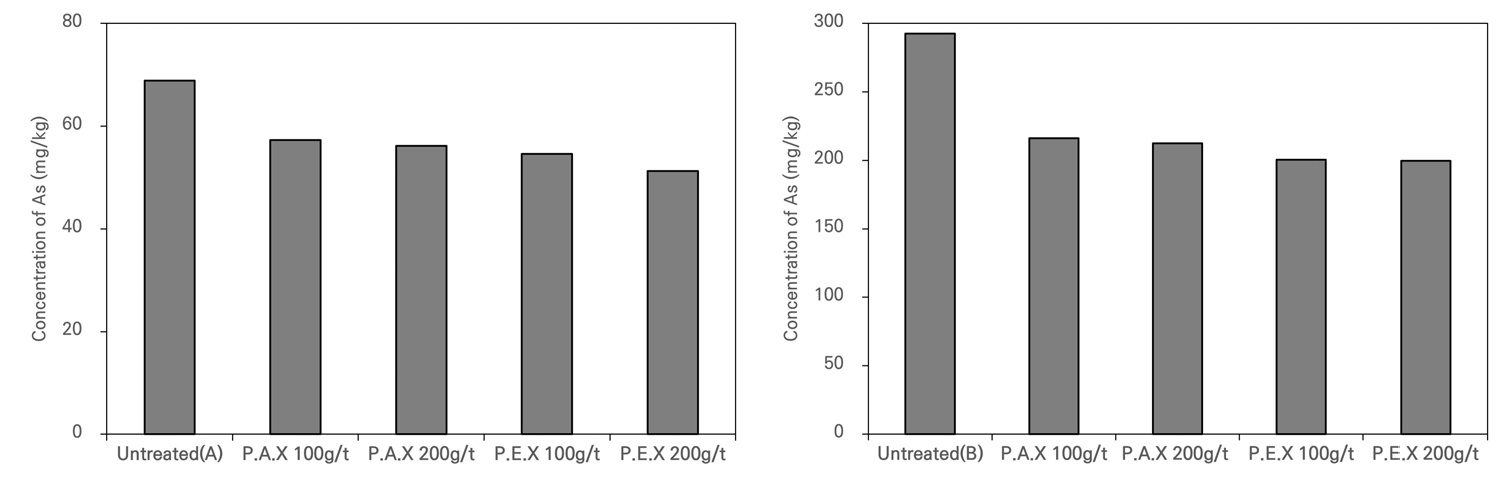
포수제 종류에 따른 영향을 확인하기 위해 Potassium Amyl Xanthate(P.A.X)와 Potassium Ethyl Xanthate(P.E.X)를 사용하였으며, 포수제는 부유 대상 광물의 표면에 흡착하여 표면을 소수성으로 변화시켜 부유성을 증가시키는 원리를 이용한다. 중농도(A-3) 부유 선별 결과 초기 농도 68.9 mg/kg와 비교하여 P.A.X 포수제 100 g/t을 투입하였을 때 16.7%의 제거율을 보였으며, 200 g/t을 적용 시 18.4%가 제거되었다(Fig. 3). P.E.X 포수제를 적용하였을 때에는 100 g/t에서 20.7%의 제거율을 보였으며, 200 g/t을 적용하였을 때, 25.6%가 제거되었다. 고농도(B-3) 시료의 경우 선별 전 초기 농도 292.6 mg/kg 대비, P.A.X 포수제 100 g/t 적용 시, 26.1%, 200 g/t을 적용하였을 때, 27.3%가 제거되었으며, P.E.X 포수제를 적용하였을 때에는 100 g/t에서 31.4%, 200 g/t로 포수제의 양을 증가시켰을 때에는 31.7% 제거되었다. 이러한 값은 Kim(2014)의 연구에서 보고된 35.0%의 제거율과 유사한 수준이며, Park(2015)의 연구(제거율 10.0%) 보다 상대적으로 높은 제거율을 나타냈다. 이러한 차이는 비교적 낮은 포수제의 농도와 상대적으로 큰 시료 입자 크기에 따른 부유 효율 감소에 기인하는 것으로 판단된다.
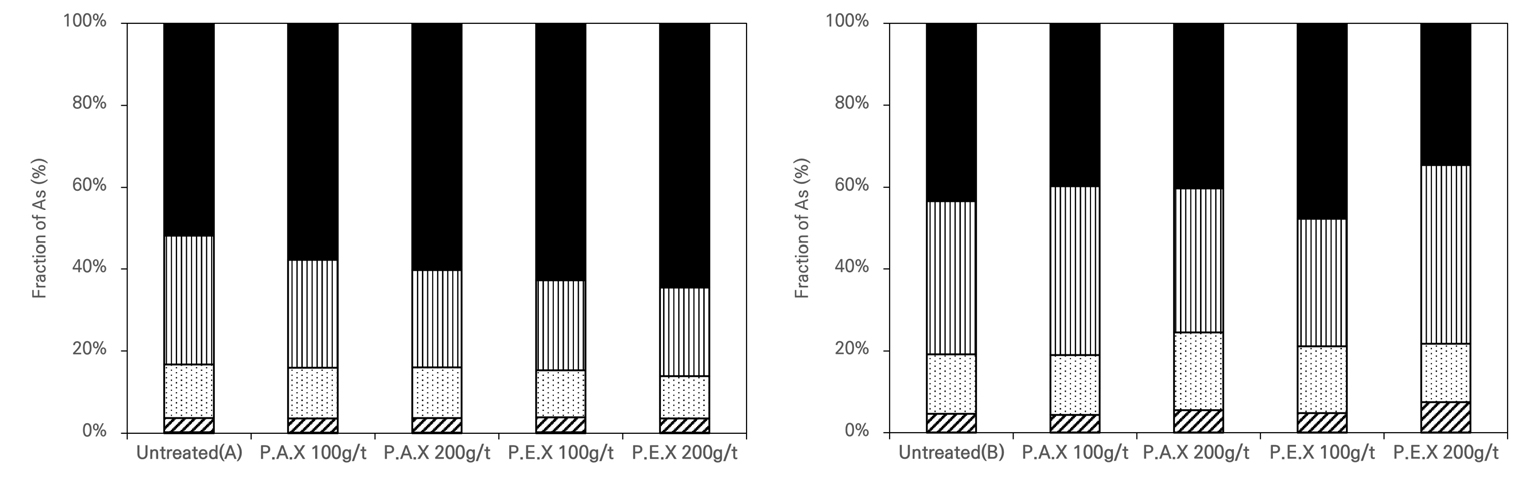
연속추출 결과 중농도 시료에서는 선별 전 초기 농도와 비교하여 P.A.X 포수제를 100 g/t 적용하였을 때, 연속추출 3단계와 4단계의 비율이 각각 23.1%, 31.6% 저감되었으며, 200 g/t을 적용 시 각각 30.7%, 44.7%의 제거율을 보였다. P.E.X 포수제를 사용하였을 때에는 연속추출 3, 4 단계가 100 g/t에서 각각 31.0%와 44.7%, 200 g/t을 투입하였을 때, 각각 40.5%와 48.2%의 제거율을 보였다. 고농도 시료의 선별 전 초기 농도와 비교하여 P.A.X 포수제를 100 g/t 적용하였을 때, 연속추출 3, 4 및 5단계의 비율이 각각 20.7%, 13.8% 및 28.3%가 저감되었으며, 200 g/t을 적용하였을 때, 3.1%, 30.9% 및 31.7%의 제거율을 보였다. P.E.X 포수제를 적용하였을 때에는 연속추출 3, 4 및 5단계의 비율이 100 g/t에서 각각 22.7%, 43.3%, 24.4%가 저감되었으며, 200 g/t을 적용하였을 때, 각각 32.7%, 20.8% 및 45.8%의 제거율이 확인되었다(Fig. 4).
토양세척 실험 결과
6가지 세척액(옥살산, 아스코빅산, 황산, 인산, 옥살산 + 디씨오나이트 및 물)을 사용하여 입도별, 농도별로 토양세척을 수행하였다(Table 6). 중농도 시료 2–0.075 mm 입도구간(A-1)에서는 황산 0.5 M을 사용하였을 때, 26.3%로 가장 높은 세척 효율을 보였으며, 아스코빅산 0.2 M을 사용하였을 때, 12.2%로 가장 낮은 제거율을 보였다. 2–0.15 mm 입도구간(A-2)에서는 옥살산 0.5 M과 디씨오나이트 0.1 M을 혼합하여 사용하였을 때, 36.7%로 가장 높은 제거율을 보였으며, 물세척에서 9.2%로 가장 낮은 제거율을 보였다.
Table 6.
Soil arsenic removal efficiencies of the washing reagents (mg/kg)
| Washing regents | A | B | ||
| 2–0.075 mm | 2–0.15 mm | 2–0.075 mm | 2–0.15 mm | |
| Soil sample | 59.1 | 60.9 | 194.6 | 198.7 |
| Deionized (DI) water | 51.0(13.6)* | 55.3(9.2) | 177.8(8.6) | 147.2(25.9) |
| 0.2 M Oxalic acid | 47.3(19.9) | 50.0(17.9) | 146.0(24.9) | 124.7(37.2) |
| 0.5 M Oxalic acid | 46.0(22.2) | 45.6(25.1) | 144.9(25.5) | 118.9(40.2) |
| 0.2 M Ascorbic acid | 51.9(12.2) | 54.6(10.4) | 175.5(9.8) | 146.9(26.1) |
| 0.5 M Ascorbic acid | 50.3(14.9) | 54.5(10.5) | 160.5(17.5) | 137.8(30.6) |
| 0.2 M Sulfuric acid | 46.0(22.1) | 44.7(26.6) | 166.8(14.3) | 133.7(32.7) |
| 0.5 M Sulfuric acid | 43.5(26.3) | 42.9(29.6) | 137.8(29.2) | 133.3(32.9) |
| 0.2 M Phosphoric acid | 48.6(17.8) | 45.8(24.9) | 149.6(23.1) | 135.9(31.6) |
| 0.5 M Phosphoric acid | 43.8(25.8) | 41.1(32.5) | 141.1(27.5) | 130.3(34.4) |
| 0.02 M Oxalic acid + 0.1 M Dithionite | 46.9(20.5) | 39.6(35.1) | 134.0(31.1) | 115.1(42.1) |
| 0.05 M Oxalic acid + 0.1 M Dithionite | 43.6(26.2) | 38.6(36.7) | 117.6(39.6) | 104.1(47.6) |
See Table 3 for an explanation of the abbreviations
고농도 시료의 경우 2–0.075 mm 입도구간(B-1)에서는 옥살산 0.5 M과 디씨오나이트 0.1 M을 혼합하여 사용하였을 때, 39.6%로 가장 높은 제거율을 보였으며, 물세척에서 8.6%로 가장 낮은 효율을 보였다. 2–0.15 mm 입도구간(B-2)에서는 2–0.075 mm에서와 마찬가지로 옥살산 0.5 M과 디씨오나이트 0.1 M을 혼합하여 사용하였을 때 47.6 %로 가장 높은 제거율을 보였으며, 물세척에서 25.9%로 가장 낮은 효율을 보였다.
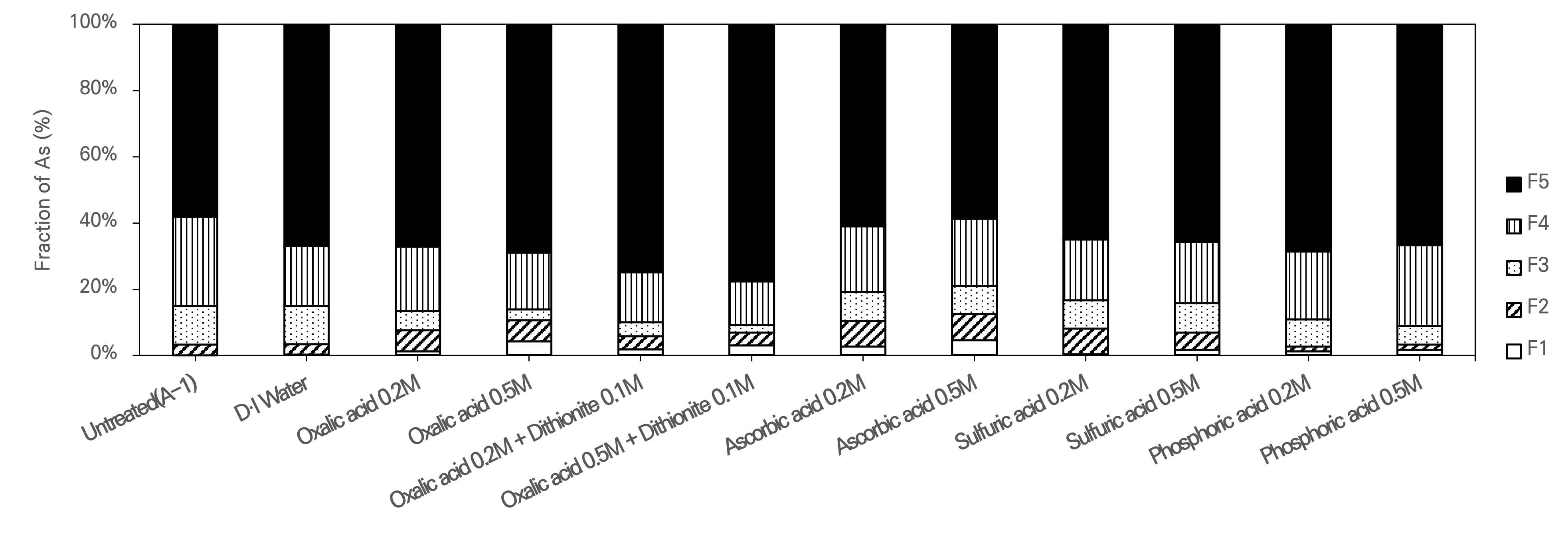
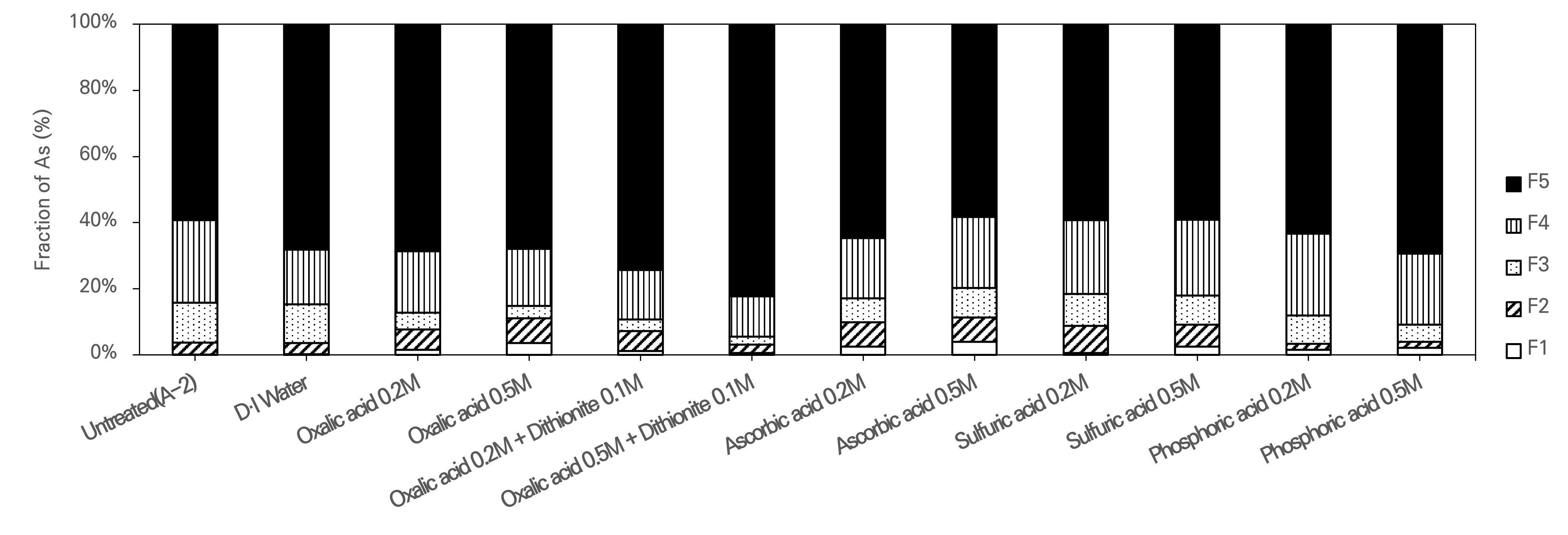
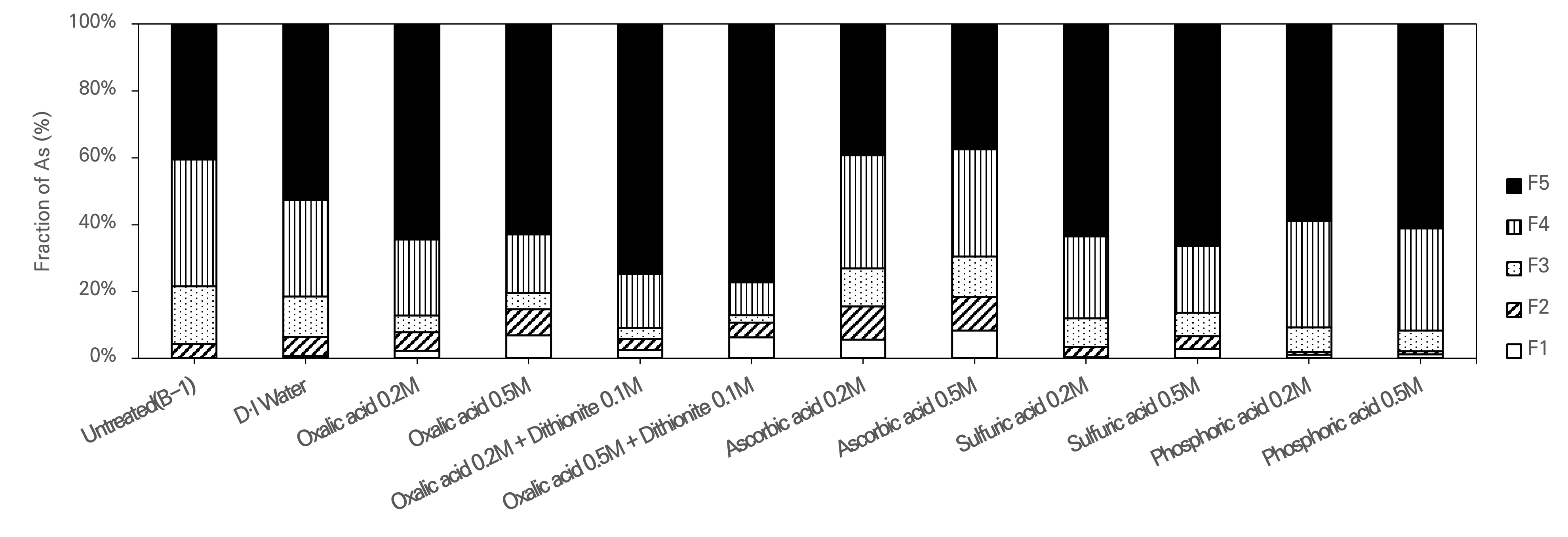
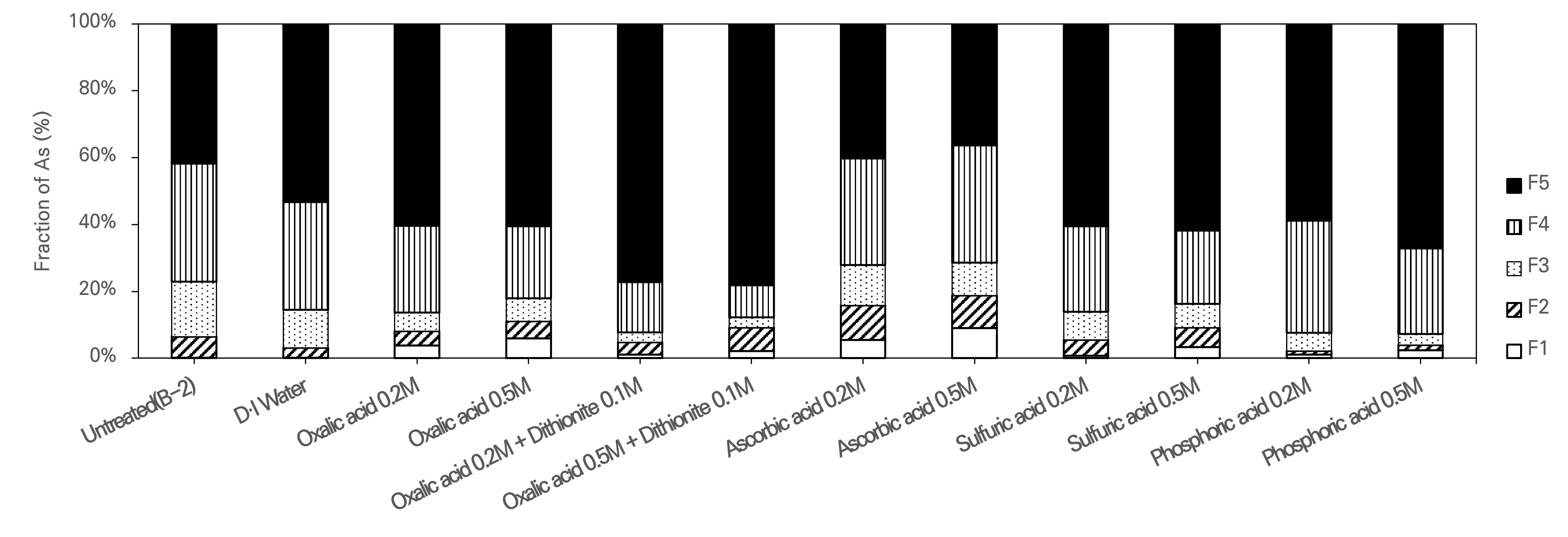
실험 결과, 세척액들 간의 효율을 비교한 결과는 Table 7에 정리하였으며 각 실험에 대한 결과는 Fig. 5, 6, 7, 8에 도시하였다. 토양세척 실험에서는 대체로 2–0.15 mm 입도구간에서 2–0.075 mm 입도구간에 비해 높은 세척 효율을 보였으며, 이는 Ko et al.(2004)의 연구에서 0.15 mm 이하의 토양을 분리할 경우 비소의 제거율이 상승한다는 결과와 유사한 경향을 나타냈다 또한, 옥살산과 디씨오나이트를 혼합하여 세척하였을 때, 최대 48.0%의 제거율을 보였으며, 이는 Baek(2021)의 연구에서 보고된 43.0%의 제거율과 비슷한 수준이다. 반면, KEITI(2016)에서 진행된 연구에서는 최대 70.0%까지 제거되었는데, 이는 해당 연구에서 사용한 고액비(1 : 25)가 본 연구(1 : 5)에서 보다 높아 비소 용출이 더 원활하게 진행되었기 때문으로 판단된다. 본 실험의 결과는 옥살산이 철(Fe) 및 알루미늄(Al) 산화물과 강한 킬레이트를 형성하고, 디씨오나이트가 철산화물 내 Fe(Ⅲ)를 Fe(Ⅱ)로 환원시켜 구조를 붕괴시킴으로써 비소의 용출을 유도한 것으로 해석된다(Huang and Wang, 2001). 한편, 아스코빅산의 경우 물세척을 제외하고 가장 낮은 제거 효율을 보였는데, 이는 황산이나 인산에 비해 산성도가 낮아 금속 산화물의 용해를 유도하는 능력이 제한적이며, 표준환원전위가 디씨오나이트 보다 높아 상대적으로 약한 환원제로 작용하는 것이 원인으로 판단된다.
Table 7.
Comparison of the arsenic removal efficiencies of the washing solutions
See Table 3 for an explanation of the abbreviations
연속추출 결과 중농도 시료에서는 입도와 상관없이 3, 4단계에서 많은 비율이 감소하는 결과를 보인 반면 5단계에서는 다소 낮은 제거율을 보였다. 고농도 시료에서도 3, 4단계에서 높은 제거율을 보였으며, 특히 아스코빅산을 사용했을 때 5단계에서도 40.0% 이상 제거율을 나타냈다. 이는 아스코빅산이 환원제로서 효과적으로 작용했기 때문으로 해석된다. 반면, 옥살산과 디씨오나이트의 혼합액이 전체적인 비소 농도는 가장 많이 감소하였지만 잔류상 형태의 비소가 아스코빅산에 비하여 적게 감소된 이유는 아스코빅산보다 환원전위는 낮지만, 반응이 빠르고, 수용액 내에서 불안정하기 때문에 용출된 비소가 일부 Fe2+ 침전물과 재결합되어 5단계의 제거 효율이 감소했을 가능성이 있는 것으로 판단된다(Jung et al., 2018).
단계별 토양세척 분석 결과
단계별 토양세척을 위한 세척제 선정은 연속추출 결과 3단계, 4단계 대상으로 가장 효율적인 옥살산 + 디씨오나이트 혼합액과 5단계에서 효율이 가장 좋은 아스코빅산을 이용하여 단계별 토양세척을 수행하였다. 실험은 고농도 시료(B) 시료의 2–0.075 mm 입도구간(B-1)을 사용하였으며, 세척액의 투입 순서를 달리하여 최종 농도를 비교하였다(Table 8). 분석 결과, (1) 옥살산 0.5 M + 디씨오나이트 0.1 M으로 세척 후 아스코빅산 0.2 M으로 세척한 시료의 경우, 초기 농도 194.6 mg/kg에 비하여 55.3%가 저감된 86.9 mg/kg의 농도를 보였으며, (2) 아스코빅산 0.2 M으로 세척 후 옥살산 0.5 M + 디씨오나이트 0.1 M으로 세척한 시료의 경우, 61.4%가 저감된 75.1 mg/kg의 농도를 보였다. 두 번째 방식이 더 높은 제거율을 보였기 때문에, (3) 아스코빅산 0.2 M으로 세척 후 옥살산과 디씨오나이트를 분리하여 순차적으로 투입하는 방법으로 세 번째 실험을 하여 그 농도를 비교하였다. 그 결과 60.5%의 농도가 저감되어 76.8 mg/kg의 농도로 확인되었으며, 두 번째 실험과 큰 차이를 보이지 않는 것으로 나타났다.
Table 8.
Details of the sequential soil washing process
본 실험에서 첫 번째 실험이 가장 낮은 효율을 보인 것은 1단계에서 옥살산이 투입되어 강산성 조건이 형성되었고, 이로 인해 이후 단계에서 아스코빅산의 환원 반응성이 저하된 것으로 해석된다(Chang et al., 2021). 반면, Set 2와 Set 3에서는 아스코빅산이 초기 단계에 적용되어 보다 적절한 pH 조건 하에서 반응하였으며, 두 조건 모두 유사한 제거 효율을 보인 것으로 보아, 옥살산과 디씨오나이트의 투입 순서가 제거 효율에 큰 영향을 미치지 않는 것으로 해석된다.
결 론
본 연구에서는 주로 결정질 산화물(Fraction 4)과 잔류상(Fraction 5) 형태로 존재하는 비소 오염 토양을 효과적으로 정화하기 위한 최적의 공법을 선정하고자 물리·화학적 선별 방법(자력 선별, 부유 선별 및 토양세척공법)의 적용 가능성을 평가하였다.
자력 선별 실험 결과, 중농도 시료에서는 제거 효율이 확인되지 않았으나, 고농도 시료에서는 10,000 Gauss에서 6.8%, 14,000 Gauss에서 10.4%의 제거율을 나타냈다. 실험 후 비소의 존재 형태를 분석한 결과, 잔류상 형태 비소의 경우 각각 39.5%와 50.0%의 높은 제거율을 보였는데, 이는 자력 선별이 철과 함께 결합된 광물형태의 비소를 효과적으로 제거할 수 있음을 의미한다.
부유 선별 실험에서는 Potassium Ethyl Xanthate(P.E.X) 포수제를 사용했을 때, Potassium Amyl Xanthate(P.A.X) 포수제 보다 제거율이 5–10% 증가하는 경향을 보였다. 다만 포수제 투입양의 경우 200 g/t을 사용하였을 때, 100 g/t에서 보다 제거율이 다소 높게 나타났으나, 큰 차이는 없어 현장 적용 시 경제성을 고려하여 적용하는 것이 적절할 것으로 판단된다. 선별 후 시료의 농도는 약 30.0%의 제거율을 보였다. 실험 후 비소의 존재 형태를 분석한 결과, 주로 연속추출 3단계와 4단계의 농도가 감소하는 경향을 보였으며, 특히 고농도 시료의 경우 연속추출 5단계의 농도도 저감되는 것이 확인되었다. 이는 고농도 비소 오염 토양에서의 부유 선별 공법이 광물형태 비소의 제거에도 효과적일 수 있음을 나타낸다.
토양세척 실험에서는 대체로 2–0.15 mm 입도구간에서 2–0.075 mm 입도구간에 비해 높은 세척 효율을 보였으며, 세척액들 간의 비교에서는 옥살산과 디씨오나이트를 혼합하여 세척했을 때 최대 48.0%로 가장 높은 제거율을 보였다. 세척 후 시료에 대한 연속추출 결과, 주로 연속추출 3, 4단계가 제거되는 것으로 나타났으며, 아스코빅산의 경우, 연속추출 5단계에서도 높은 제거율을 확인하였다. 따라서 이를 바탕으로 아스코빅산으로 1차 세척 후 옥살산과 디씨오나이트를 혼합하여 2차 세척하였을 때, 61.0%의 제거율을 얻을 수 있었다.
본 연구에서 평가한 물리·화학적 선별 방법은 비소 오염 토양의 정화에 효과적으로 적용될 수 있음을 확인하였으며, 향후 비소 오염 토양에서 최적의 정화공법을 설계하기 위한 기초자료로 활용될 수 있을 것으로 판단된다.