서론
중금속 토양오염은 사격장, 광산, 제련소 등 금속과 관련된 다양한 산업활동 지역에서 보고되고 있다. 유기물 오염은 유기물이 미생물 등에 의해 분해되어 자연정화될 가능성이 있으나 중금속은 미생물에 의해 분해되지 않기 때문에 자연적인 정화가 어렵다(Kirpichtchikova et al., 2006). 또한 우리나라의 토양오염공정시험법은 0.1 노르말 염산을 이용한 용출법에서 왕수를 이용하는 용출법으로 2010년 변경되어 고형화/안정화법을 적용하기 어려운 환경이다. 따라서 중금속 오염토양을 정화하기 위해서는 중금속 오염원을 토양으로부터 분리하여 제거하는 공정이 필요한 실정이다.
토양오염정화공정으로서 비중선별, 식물정화공정(phytoremediation), 열처리법, 동전기 정화법, 그리고 토양세척/세정법 등이 제안되어 왔다(Furukawa and Tokunaga, 2004; Park et al., 2013). 오염토양으로부터 중금속을 제거하기 위해 비중선별과 같은 광물처리(Mineral processing) 공정으로 오염토양 중 금속성분을 농축한 후 침출하는 공정이 효율적인 것으로 알려져 왔다. 그러나 75 µm이하의 입자는 비중선별이 곤란하기 때문에 매립처리되어 왔다. 미립자는 비표면적이 넓기 때문에 반응성이 우수하여 오히려 화학적 침출법이 미립자로 구성된 오염토양의 정화에 유용할 수 있다. 염산과 질산과 같은 무기산은 토양오염 중 금속 오염원 제거에 효과적인 것으로 알려졌으나(Isoyama and Wada, 2007; Meunier et al., 2009; Tokunaga et al., 2005), 오염토양 정화 후 토양을 산성화시키기 때문에 토양의 재이용을 위해서는 별도의 중화공정이 필요해 처리비용 상승이 불가피한 단점이 있다(Han and Lee, 2015).
상기의 무기산을 대체하기 위해 다양한 유기산을 이용한 오염토양 정화 연구가 수행되었다. 유기산으로서 아세트산(acetic acid) (Mercier et al., 2002), 타르타르산(tartaric acid) (Gao et al., 2003; Tokunaga et al., 2005), S,S-ethylenediaminedisuccinic acid(EDDS) (Kirpichtchikova et al., 2006), ethylenediaminetetraacetic acid(EDTA) (Jean-Soro et al., 2012; Kirpichtchikova et al., 2006; Labanowski et al., 2008; Wasay et al., 1998; Wen et al., 2009), diethylenetriaminepentaacetic acid(DTPA) (Wasay et al., 1998), 옥살산(oxalic acid) (Renella et al., 2004), 그리고 구연산(citric acid) (Bassi et al., 2000; Gao et al., 2003; Jean-Soro et al., 2012; Kirpichtchikova et al., 2006; Labanowski et al., 2008; Renella et al., 2004; Tokunaga et al., 2005; Wasay et al., 1998; Wen et al., 2009)이 침출제로 연구되었다. 구연산은 금속이온과 착이온 형성능력이 우수한 것으로 알려져 있으나 EDTA 등에 비하여 오염토양 중 중금속의 제거율이 낮은 것으로 보고되었다(Furukawa and Tokunaga, 2004; Tokunaga et al., 2005).
제거율이 낮은 이유로서 구연산은 탄산염 또는 산화물과 같이 풍화된 형태의 금속 성분을 용출시키는 것으로 보고되었다(Park et al., 2013). 구연산만을 이용한 침출실험에서 토양 중 납, 구리, 아연의 침출율(제거율)은 60-90%로 나타났으나, 토양오염 우려기준은 초과하는 것으로 확인되었다(Park et al., 2013). 이 연구에서는 오염토양 중 납, 구리, 아연의 침출율을 향상 시키기 위해서 구연산 용액에 과산화수소를 첨가하여 중금속 제거 개선 효과를 검토하였다.
실험방법
본 연구에서 사용된 오염토양시료는 소화기 사격훈련장(시료 A), 클레이 사격장(시료 B), 항만퇴적토(시료 C)로부터 채취된 것을 이용하였다. 미립자 시료를 처리하기 위해 200 mesh(75 µm)로 습식체질하여 80oC에서 12시간 건조한 후 침출실험에 사용하였다. 체질 후 얻어진 시료의 중금속 함량은 시료 A에서 구리와 아연이 각각 1256 mg·kg-1과 897 mg·kg-1, 시료 B에서 납이 4635 mg·kg-1 그리고 시료 C에서 아연이 4221 mg·kg-1이었다. 침출 및 추출 실험에 사용된 모든 시약은 시약급을 사용하였다.
Tessier et al.(1979)이 제안하고 Li et al.(1995)이 수정한 연속추출법(sequential extraction method)을 사용하여 오염토양 중 중금속의 화학적 형태를 조사하였다. 상기의 체질에서 얻어진 75 µm 이하의 1 g 시료를 연속추출법 실험에 사용하였고, 각 연속추출법 단계에 사용된 시약과 조건은 아래와 같다. 1) pH 7로 조절된 1 mol·l-1 MgCl2용액 8 ml에 시료를 넣고 1시간 동안 교반하며 상온에서 용출 2) pH 5로 조절된 1 mol·l-1 CH3COONa 용액 8 ml에 1단계 용출실험의 잔사를 넣고 5시간 동안 교반하며 상온에서 용출 3) 0.4 mol·l-1 NH2OH·HCl(in 25% CH3COOH)용액 20 ml에 2단계 용출실험의 잔사를 투입하고 6시간 동안 히팅블록을 사용하여 96oC에서 용출, 4) 먼저 0.02 mol·l-1 HNO3 용액 3 ml와 pH 2로 조절된 30% H2O2 용액 5 ml에 3단계 용출실험의 잔사를 투입하고 2시간 동안 히팅블록을 사용하여 85oC에서 용출한 후, pH 2로 조절된 30% H2O2 용액 3 ml를 추가하고 3시간 동안 히팅블록을 이용하여 85oC에서 용출하며 마지막으로 3.2 mol·l-1 CH3COONH4(in 20% HNO3) 용액 5 ml와 전체 용액의 부피가 20 ml가 되도록 초순수를 추가하여 상온에서 30분간 용출, 5) 남은 잔사의 성분이 모두 용출되도록 하며, 당 연구에서는 왕수를 사용하여 고온에서 용출시켰다. 모든 용출용액은 원심분리기를 이용하여 10,000 rpm에서 30분간 분리 후 상등액을 5% 질산으로 희석한 후 분석하였으며, 침전물은 세척하고 다음 단계의 용출실험에 사용하였다.
침출용액은 구연산나트륨(trisodium citrate)과 구연산(citric acid)을 8:2의 비율로 섞어 제조하였으며, 침출액의 pH는 5.1이었다. 과산화수소를 첨가한 후 50 ml 침출액을 100 ml 플라스크에 넣었으며, 구연산과 과산화수소의 농도는 각각 1 mol·l-1과 0 mol·l-1 - 2 mol·l-1이었다. 항온수조(BS-31, Jeio Tech, Co, Ltd.)의 온도와 교반속도가 50oC와 80 rpm이 되면 5 g의 시료를 침출액에 투입하였다. 120분의 침출실험이 종료되면 모든 용액을 0.45 µm 멤브레인 필터로 여과한 후 초순수로 두 번 세척하고 105oC에서 8시간 동안 건조하였다. 건조된 시료는 왕수로 분해하여 잔류 금속 함량을 분석하였고, 여과액은 pH를 측정한 후, 질산으로 희석하여 납, 구리, 아연의 농도를 원자흡광광도계(AA- 7000, Shimadzu Scientific Instrument, Ltd., Japan)로 측정하였다. 침출율은 침출액과 잔사 중 금속의 함량을 고려하여 계산하였다.
실험결과 및 고찰
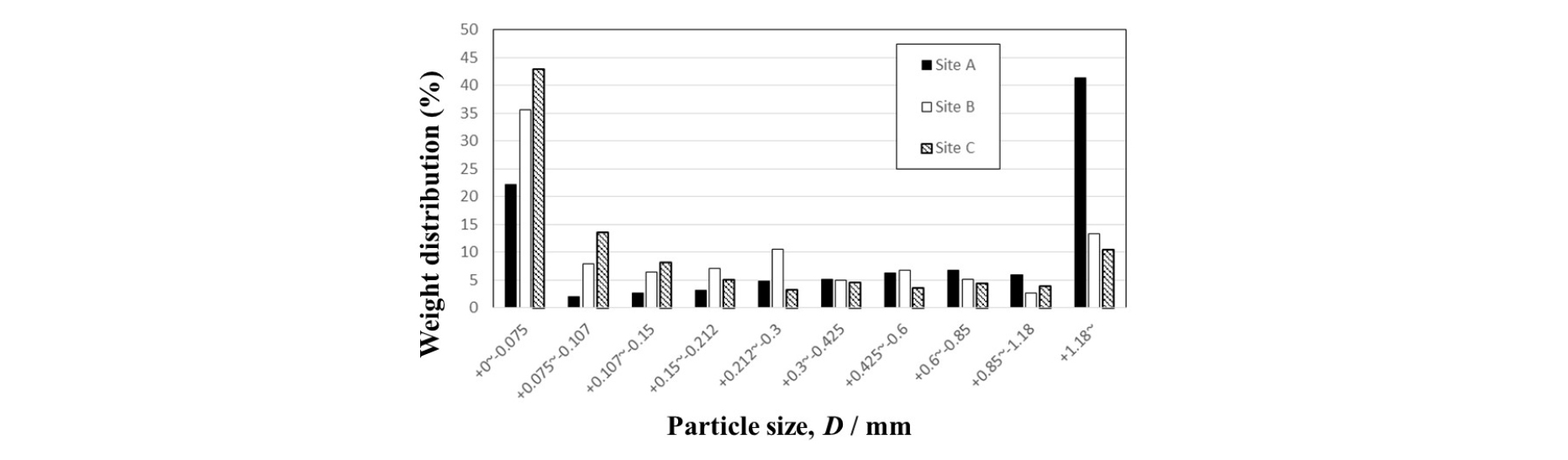
소화기 사격훈련장(시료 A)은 30년 이상 군부대 사격훈련에 사용된 장소로서 주로 구리, 아연, 납으로 오염되어 있으나 납의 경우 토양 중 함유량이 200 mg·kg-1이하로 환경기준에 미치지 못하기 때문에 당 연구에서는 시료 A의 경우 구리와 아연의 침출거동만을 조사하였다. 클레이사격장(시료 B)은 레저용 프로그램으로 사용되는 사격장으로 오염원은 주로 납탄이므로 납의 침출거동이 조사되었다. 마지막으로 항만퇴적토(시료 C)는 국내 항구에서 채취된 시료로 아연이 주 오염성분이었다. 이상의 시료에서 75 µm이하 입자의 비율은 Fig. 1에 나타낸 바와 같이 22%에서 43%를 차지하고 있으나 이와 같은 미립자는 현재까지 적절한 처리 없이 매립되는 경우가 많았다.
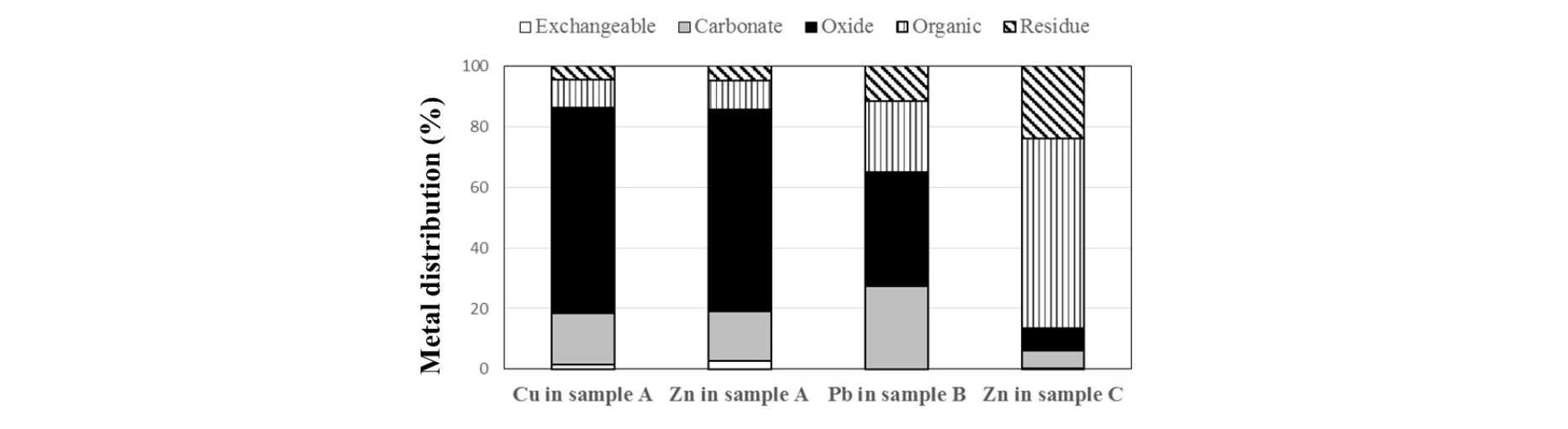
화합물의 동정은 X선 회절법(X-ray diffractometer, XRD) 사용이 일반적이나, 미량 금속의 경우 분석이 곤란하다. 연속추출법은 특정한 추출 시약을 이용하여 특정한 화학 형태의 성분만을 추출하는 방법으로 토양이나 퇴적토 중 미량으로 존재하는 금속의 화학적 형태 분석에 유효하다. Tessier의 연속추출법은 이온교환태, 탄산염결합태, 산화물결합태, 유기물(황화물)결합태, 잔류물의 다섯 단계로 구성되어 있다(Li et al., 1995; Tessier et al. 1979). Fig. 2는 Tessier 법에 의한 각 시료 중 금속 성분형태의 분포를 나타내고 있다. 소화기 훈련장의 오염토양(시료 A)에서 구리와 아연은 비슷한 분포를 나타내고 있는데 이는 두 금속이 총탄의 합금성분이기 때문이다. 구리와 아연의 67.8%와 66.4%가 각각 산화물결합태에 분포하고 있으며, 풍화된 형태인 이온교환태, 탄산염결합태, 산화물결합태의 합계는 구리와 아연이 각각 86.2%와 85.6%로 나타났다. 클레이사격장의 오염토양 중 납은 탄산염결합태와 산화물결합태에 각각 27.4%와 37.6%가 분포하고 있는 반면, 유기물(황화물)결합태와 잔류물에 23.5%와 11.5%가 각각 분포하고 있다. 마지막으로 항만퇴적토(시료 C) 중 아연의 대부분은 유기물(황화물) 결합태에 분포하고 있는데 이는 아연오염원이 섬아연광(ZnS)이기 때문이다. 풍화된 형태인 이온교환태, 탄산염결합태, 산화물결합태의 합계는 시료 B와 시료 C에서 각각 65.0%와 13.6%인 것을 알 수 있다.
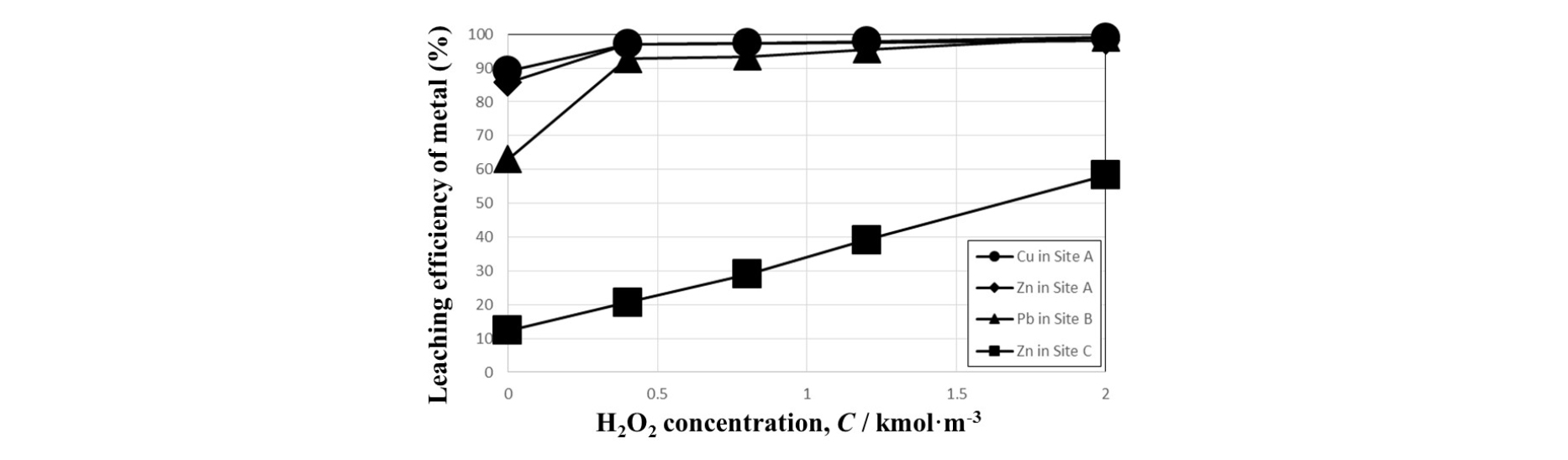
Fig. 3은 납, 구리, 아연의 구연산 침출에 대한 과산화수소 첨가의 영향을 나타내고 있다. 과산화수소 첨가 없이 구연산으로 침출한 경우, 시료 A의 구리와 아연, 시료 B의 납, 시료 C의 아연 침출율은 각각 89.2%, 85.8%, 63.1%, 그리고 12.3%이었다. 종래의 연구에서 구연산은 풍화된 형태인 이온교환태, 탄산염결합태, 산화물결합태를 침출할 수 있다고 보고되었다(Park et al., 2013). Fig. 3에서 침출된 금속의 양은 Fig. 2에 나타난 풍화된 형태의 양과 유사하여 종래의 연구결과와 일치하고 있다.
Fig. 3에 나타난 시료 A와 B의 침출결과에서 과산화수소 첨가량이 2 mol·l-1까지 증가한 경우 금속침출율은 98%까지 증가하였다. 즉, 시료 A에서 구리와 아연의 시료 중 잔존량과 시료 B에서 납의 잔존량은 각각 150 mg·kg-1, 300 mg·kg-1, 200 mg·kg-1이하로 감소하여 환경기준을 만족하였다. 시료 C의 아연은 과산화수소 첨가량이 증가함에 따라 침출율이 점차적으로 증가하여 58.3%에 이르렀다. 시료 C를 강열감량법으로 조사한 결과 11.3%의 유기물이 존재하는 것으로 분석되었으며 투입된 과산화수소가 금속의 침출이 아닌 유기물 분해에 사용되었을 가능성이 높은 것으로 생각된다. 상기의 침출결과는 구연산은 오염토양 중 풍화된 형태의 금속성분을 용해시키며 과산화수소는 금속 또는 황화물로 존재하는 금속을 산화시켜 침출율을 향상시키는 것을 나타낸다.
초기 구연산 침출액의 pH는 Table 1과 같이 구연산나트륨(trisodium citrate)과 구연산(citric acid)의 혼합비율을 조정하여 조절되었다. 침출액의 pH는 구연산의 비율이 증가함에 따라 감소하였다. 구연산나트륨(trisodium citrate)과 구연산(citric acid)의 혼합비율을 8:2로 하였을 때 별도의 산이나 염기의 첨가 없이도 pH는 5.1로 조절가능하였다. 과산화수소에 의한 침출반응은 다음과 같이 정리할 수 있다.
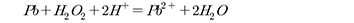 (1)
(1)
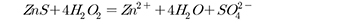 (2)
(2)
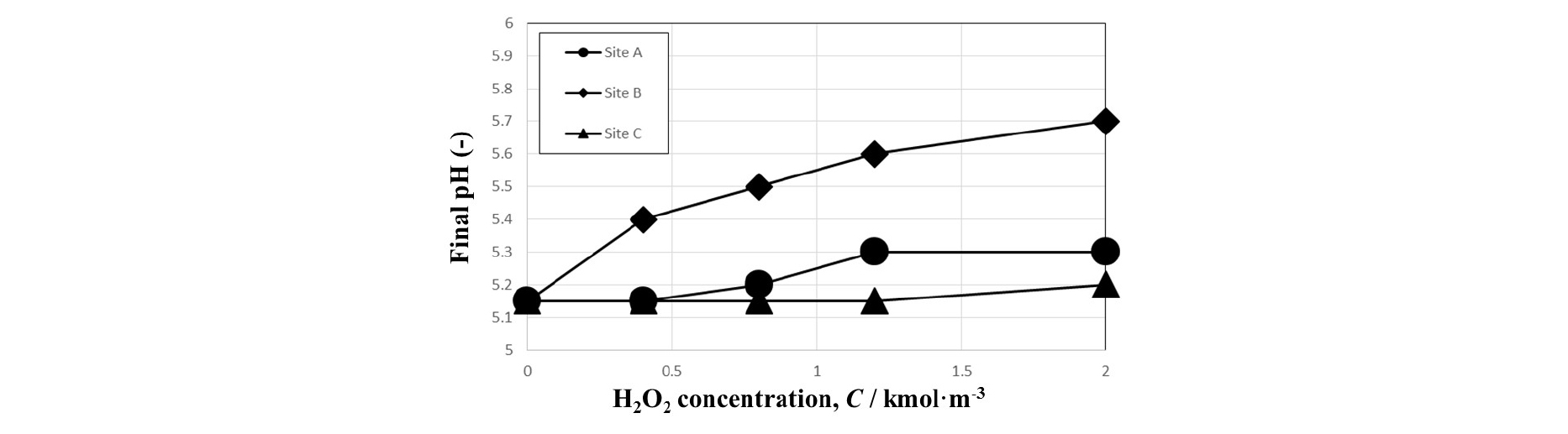
식 (1)에서 알 수 있듯이 과산화수소(H2O2)가 금속을 산화시키는 과정에서 수소이온을 소비하기 때문에 반응 후 pH는 상승한다. 식 (2)와 같이 황화물을 산화시키는 경우 수소이온이 소비되는 반응이 존재하지 않기 때문에 pH의 변화는 나타나지 않는다. Fig. 4는 침출 반응 후 pH에 미치는 과산화수소 첨가의 영향을 나타내었다. 시료 A와 B는 납, 구리, 아연이 금속으로 존재하기 때문에 pH의 증가가 나타났으며, 금속 존재량이 시료 B의 경우 시료 A보다 많기 때문에 시료 B에서 pH 증가가 더 크게 나타난다. 그러나 금속이 황화물로 존재하는 시료 C의 경우 아연이 황화물로 존재하기 때문에 pH의 변화는 거의 나타나지 않았다.
오염토양 중 존재하는 금속의 풍화된 형태는 구연산에 의해 성공적으로 용해될 수 있으나, 종래의 연구에서는 침출 후 토양 중 금속의 잔존량이 환경기준을 초과하는 경우도 보고되었다(Park et al., 2013). 이 연구에서는 1 mol·l-1의 구연산염 용액만을 사용한 경우 환경기준치 이하로 제거하는 것이 불가능하였던 시료에 대해 2 mol·l-1 과산화수소를 추가로 첨가하여 환경기준치 이하로 납을 제거하는 것이 가능한 것을 나타내었다. 또한 침출 반응 후 pH는 5.7까지 상승하여 납을 환경기준 이하로 제거할 뿐 아니라 중성 영역에 가까운 pH로 배출하는 것이 가능한 것을 알 수 있다. 미립자를 침출하는 경우, 고액분리가 어려운 것으로 알려져 있으나 구연산은 과일 등에 함유되어 있는 물질로 토양 중 잔존하고 있어도 주변 환경에 영향이 없기 때문에 상기와 같이 미립자를 구연산을 이용해 침출하여도 추가적인 처리공정은 불필요할 것으로 기대된다.
결론
과산화수소를 첨가한 구연산 침출을 수행하여 오염토양 중 납, 구리, 아연의 침출거동을 조사하였으며, Tessier의 연속추출법을 이용하여 조사한 오염토양 중 금속의 존재형태와 구연산 침출결과를 비교하여 분석하였다.
이온교환태, 탄산염결합태, 산화물결합태 등의 풍화된 금속형태는 1 mol·l-1의 구연산염 용액만을 사용하여도 침출되는 것이 확인되었으며, 과산화수소 첨가량이 증가함에 따라 금속의 침출율은 추가적으로 증가하였다. 사격장 시료에 비해 항만퇴적토 시료 중금속 침출율이 더 낮은 것은 퇴적토 중 함유된 11.3%의 유기물을 분해하는 것에 첨가된 과산화수소가 사용된 것이 이유로 판단되었다. 반응 후 pH는 사격장 시료를 처리한 경우 과산화수소 첨가량이 증가함에 따라 금속산화반응에서 수소이온을 소비하여 증가하였으나 항만퇴적토 시료의 경우 황화물 산화반응에서 수소이온농도의 변화가 없어 과산화수소 첨가량에 따른 pH 변화가 나타나지 않았다.