서 론
비소는 유기비소와 무기비소로 분류되는데 자연환경 지하수에서는 유기비소 형태인 Monomethylarsonate(MMA), Dimethylarsinate(DMA) 뿐 아니라 As(III), As(V)의 무기비소가 공존할 수 있으며, 대부분은 As(III), As(V)와 같은 무기비소로 이루어져 있다(Cullen and Reimer, 1989; Xu et al., 1991; Jackson and Miller, 2000).
무기비소인 As(III), As(V)의 형태는 pH와 산화환원 조건(Eh)에 따라 댜양하게 존재한다. 산화조건일때는 As(V)가 안정하여 H3AsO4, H2AsO4‒, HAsO42‒ 형태로 존재하며, 반면 환원조건일 경우 As(III)가 안정하여 H3AsO30, H2AsO3‒, HAsO32‒, AsO33‒ 형태로 존재한다(Smedley and Kinniburgh, 2002; Kim, 2005).
pH 7 이하에서 비소 형태별 이동성 순위는 As(III) > MMA > DMA > As(V)이며, pH 7 이상에서는 MMA = DMA > As(III) > As(V) 이다(Bowell, 1994). As(III)는 pH 2~pH 9 범위에서는 H3AsO30의 중성분자형이기 때문에 이동성이 크고 즉, 흡착제와의 정전기적 인력이 약하다. 유기비소인 MMA, DMA의 경우는 대부분 전하를 띠지 않거나 약한 음이온 형태로 존재하여 이동성이 크다. 반면 As(V)는 pH 2이상에서는 음이온 형태로 존재하여, 양전하를 띠는 흡착제 표면과 강한 정전기적 상호작용에 의해 잘 흡착되므로 이동성이 낮다. 물 속에서의 As는 음이온으로 존재하며, 다른 음이온들과 착화합물을 형성하지 않고, 호기성인 지표수 등에서는 As(V)로, 지하수와 같은 혐기성인 조건이 우세한 곳에서는 As(III)로 주로 존재한다(Kim, 2005). 그러나 양이온인 금속성 물질(Ca, Na, Mn, Fe, Al 등)과 결합, 흡착하여 침전물을 형성하고 이동성에 영향을 준다. As의 이동성은 Fe/As비가 증가할수록 감소한다(Krause and Ettel, 1989).
As 오염수를 처리하는 방법으로는 물리·화학적 처리기술인 응집·침전, 이온교환법, 멤브레인처리법, 흡착 등의 기술이 있으며(Mondal et al., 2006; Singh et al., 2015; Sarkar and Paul, 2016), 수질의 pH, 산화환원 조건, 비소의 형태 및 농도 등에 따라 다르게 적용할 수 있다. 그러나 응집·침전, 막분리, 이온교환방법 등 기존의 화학적 처리기술은 높은 운전 비용, 2차 폐기물 발생, 복잡한 운전 조건 등의 단점을 가지고 있어 장기적인 지속가능성에는 한계가 존재한다.
반면에, 흡착은 높은 선택성, 친환경성, 효율성, 가역성, 경제성, 그리고 단순성 때문에 효과적인 방법으로 여겨진다(Yao et al., 2024). 최근에는 금속산화물, 점토광물, 바이오차, 탄소나노튜브, 그래핀 산화물 등 다양한 흡착제가 중금속 제거를 위해 활발히 연구되고 있다(Samyuktha et al., 2021; Park and Kim, 2024; Lorenzo et al., 2025). Iwuozor et al.(2022)에 따르면 최적의 흡착 결과를 얻는데 있어 흡작제의 표면 화학, 친수성, 물리화학적 특성, 형태, 구조, 질감 특성(기공크기, 기공부피, 표면적, 기공면적)등이 영향을 미친다고 하였다. 또한 흡착제는 지속 가능한 개발을 위해서는 다공성이 높은 산화물 금속과 같은 친환경 흡착제가 선호된다는 기존의 연구결과가 있다(Yao et al., 2024).
이에 따라 본 연구에서는 다공성과 높은 농도의 철산화물을 포함한 T-폐석탄광산배수 처리시설의 산업부산물인 T-sludge를 흡착제로 활용하여 As 제거 효율을 평가하고자 하였다. 이를 위해 Langmuir, Freundlich 및 Dubinin-Radushkevich(D-R) 등 세가지 등온흡착모델을 적용하여 As농도 및 접촉시간에 따른 흡착 특성을 분석하였으며, 최대흡착용량(qmax)을 기준으로 기존 철 수산화물 기반 흡착제와 성능 비교를 수행하였다. 아울러 pH변화에 따른 동적흡착실험을 통해 유사 1차 반응속도모델과 유사 2차 반응속도모델을 적용함으로써 흡착 속도 특성을 정량적으로 평가하였다.
연구재료 및 방법
실험재료
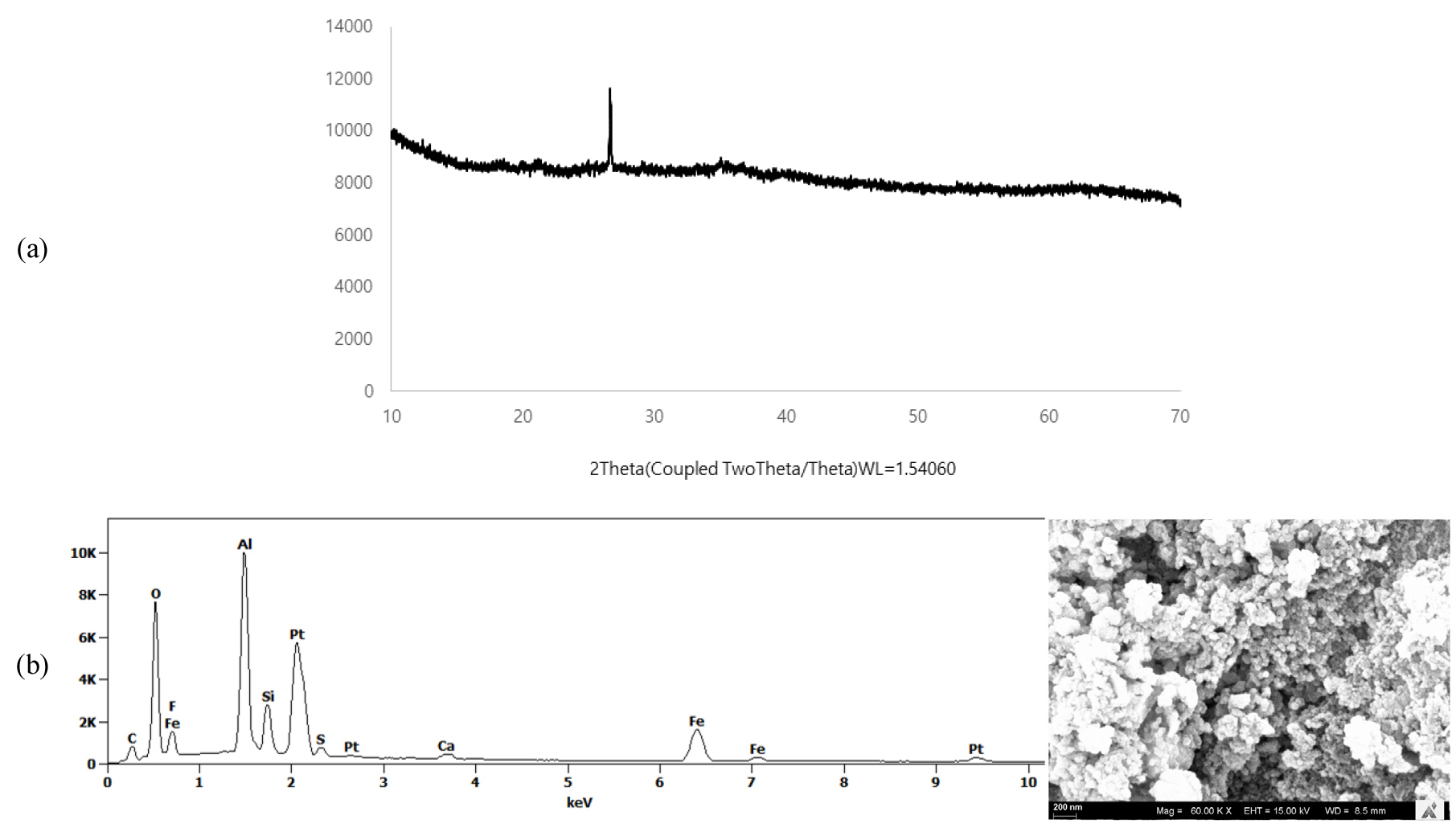
흡착제로 사용할 폐석탄광산배수슬러지는 수질정화시 고분자 무기 응집제인 PAC(Poly aluminium chloride) polymer를 사용하여 처리하는 T-수질정화시설에서 발생한 것으로 탈수된 슬러지(T-Sludge)를 채취하였다. 채취된 시료는 균일화 작업을 거친후 자연건조하여 흡착실험에 사용하였다. T-Sludge의 영전하점(pHzpc)은 9.59로 확인되었으며, BET분석결과 295.85 m2/g의 넓은 비표면적과 메조기공의 다공성 크기로 이루어진 입자로 나타났다. BET 분석은 질소를 흡탈착하는 방법으로 비표면적 기공 분석기(3Flex, micromericitics)를 사용하여 수행되었으며, XRD 분석은 XRD(X-ray diffiractometer, X'Pert PRO, Malvern Panalytical)장비를 사용하여 2Ɵ 범위 10°‒70°에서 수행되었으며, 그 결과 높은 농도의 알루미늄과 철을 함유하고 있는 석영광물임이 확인되었다. 이와 같은 결과는 Table 1과 Fig. 1에 나타내었으며(Kim and Ji, 2023), 기존에 발표된 철수산화물의 비표면적, 기공크기, 영전하점도 Table 1에 함께 나타내었다.
Table 1.
Comparison of the BET surface area, pore size, and pHzpc of T-sludge and iron-based coagulants
| BET (m2/g) | Pore size (Å) | pHzpc | Reference | |
| T-Sludge | 295.85 | 47.41 | 9.59 | This study |
| ZVI | 1.03 | 101.3 | - | Kim et al. (2011a) |
| GFO | 54.7 | 125.4 | - | |
| GFH | 222.00 | 5.12 | 5.2 | Kumar et al. (2020) |
| Akaganeite | - | - | 7.8 | Kim et al. (2011b) |
| Ferrihydrite | - | - | 8.5 |
흡착질로 사용된 비소오염수는 시판되는 98% 이상의 Sodium arsenite(NaAsO2)와 Sodium arsenate dibasic heptahydrate(Na2HAsO4·7H2O) 시약을 사용하여 각각 As(III), As(V) 용액을 조제하여 사용하였으며, 흡착실험시 초기 농도는 ICP-OES(model 8300, Perkin-Elmer Inc.)로 측정하였다.
등온흡착모델
흡착성능평가를 위해 Langmuir, Freundlich 등온흡착모델을 사용하였으며, 흡착메커니즘을 평가하기 위해 Dubinin-Radushkevich(D-R) 등온흡착모델을 사용하였다.
등온흡착실험을 위한 흡착질은 As(III)와 As(V) 용액를 1, 5, 10, 30, 50, 110, 230 mg/L의 농도로 조제하였고, 이때 용액의 pH는 0.1N NaOH용액을 사용하여 6.9~7.1로 조절하였다. 흡착제와 흡착질의 고액비는 1:500이고, 수평진탕기에서 20℃에서 200 rpm으로 60 시간 동안 교반하여 흡착실험을 진행하였다. 시료는 12, 24, 36, 48, 60시간의 간격으로 채취하였으며, 원심분리 후 상등액을 0.45 ㎛ 필터로 여과한 뒤 여액을 ICP-OES로 As농도를 측정하였다. 이와 같은 실험은 3회 반복으로 수행하였다.
Langmuir 등온흡착
Langmuir 등온흡착모델은 저농도 흡착에 더 적합한 특징을 갖고 있으며, 4개의 전제조건을 가진다. (1) 흡착은 고정된 단일 흡착층에서 일어나고, 하나의 분자만 흡착할 수 있는 모두 동일한 성질을 가지고 있다. (2) 흡착에너지는 모든 지점에서 동일하고 흡착된 물질간의 상호작용은 없다. (3) 흡착은 가역적이다. (4) 표면에 흡착된 분자는 옆으로 이동하지 않는다(Ata et al., 2023).
Langmuir 등온흡착식은 다음 (식 1)과 같다(Otgonjargal et al., 2012). KL은 흡착제와 흡착질 사이의 친화도를 나타내는 상수로, 흡착제의 적절한 면적 및 다공성의 변화와 상관관계를 갖는다(Snoeyink, 1990).
여기서, Ce : 흡착질의 평형농도(mg/L)
qe : 평형상태에서 흡착제 단위질량당 흡착된 흡착질의 양(mg/g)
qmax : 이론 최대흡착용량(mg/g)
KL : Langmuir 상수
Langmuir 등온흡착식의 분리계수 RL은 흡착공정의 적합성을 판단할 수 있는 무차원 상수로, RL > 1 일 경우 흡착이 불리함을 나타내며, RL = 1 일 경우 선형을 나타내고, 0 < RL < 1 일 경우 흡착이 유리함을, RL = 0일 경우 비가역적임을 나타낸다(Ayawei et al., 2017). RL 값이 작을수록 흡착이 더 유리함을 뜻한다.
Freundlich 등온흡착
Freundlich 등온흡착모델은 에너지 분포가 불균일한 흡착제 표면에서 단분자층 외에 다분자층 흡착에도 적용 가능하다(Lee, 2019)는 것을 전제로 하는 모델로 다음 (식 3)과 같다.
여기서, KF : Freundlich 상수
n : 불균일도(heterogeneity)
KF 값은 흡착제가 흡착질을 흡착할 수 있는 잠재적인 에너지를 나타낸 것으로, 값이 클수록 흡착이 양호함을 의미한다. 데이터의 선형화를 위해 Freundlich 등온흡착식 (식 3)을 log 형식으로 작성하면 (식 4)와 같다. 기울기인 1/n 의 값은 흡착강도 또는 표면 불균일성을 나타내는데 0에 가까울수록 불균일성이 높다는 것을 의미하며(Kumar et al., 2020), 0.1 < 1/n < 0.5 일 때 흡착처리가 효과적이라고 판단한다(Srihari and Das, 2008). 다시 말해 n은 흡착동력의 크기를 나타낸 것으로 n > 2 이상이면 흡착이 용이한 반면 n < 1 이하인 경우 난흡착성 물질로 평가된다(Na et al., 2011).
Dubinin Radushkevich(D-R) 등온흡착
D-R 등온흡착모델은 흡착제의 불균일한 표면에 가우스 분포를 가지는 흡착기구를 설명하며, 다분자층 흡착 특성을 나타낸다(Lee, 2021). D-R 등온흡착식은 다음 (식 5)와 같다.
여기서, qmax : 최대흡착량(mol/g)
β : 흡착질 1몰당 평균 흡착 자유에너지(mol2/J2)
ε : Potential 에너지
R : 기체상수(8.314 J/mol·K)
T : 절대온도(K)
흡착에너지(E, kJ/mol)는 다음 (식 6)과 같다.
흡착에너지(E)값을 통해 흡착메커니즘을 판단할 수 있으며, E 값이 8 kJ/mol보다 작으면 물리적 흡착을 나타내고, 8 kJ/mol~16 kJ/mol이면 이온교환흡착, 16 kJ/mol보다 크면 화학적 흡착으로 설명할 수 있다(Namasivayam and Sangeetha, 2006).
동적흡착모델
흡착 과정에 필요한 시간을 설명하는데 있어서 동적흡착모델을 사용한다. 본 연구에서는 시간에 따른 흡착 특성과 비소 흡착을 위한 최적의 pH를 선택하기 위해 유사 1차 반응모델(pseudo first order)과 유사 2차 반응모델(pseudo second order)을 사용하여 평가하였다. 동적흡착실험에 사용된 흡착질인 As(III)와 As(V) 용액의 초기 농도는 10 mg/L, 이때 pH는 3, 5, 7, 9, 11로 설정하여 설정 pH값과 ± 0.15범위안으로 조절하여 조제하였다. 고액비는 1: 500, 수평진탕기에서 20℃에서 200 rpm으로 48시간 동안 교반하고 일정시간 간격으로 시료채취 후 As를 분석하였다.
유사 1차 반응모델(pseudo first order)은 (식 7)과 같으며(Lee, 2015), 유사 2차 반응모델(pseudo second order)은 (식 8)과 같다(Ho and Mckay, 1999). (식 9)의 h는 흡착이 시작되는 초기 단계에서 흡착제가 흡착질을 얼마나 빠르게 흡착하는지를 설명하는 초기 흡착 속도를 의미한다.
여기서, qt : 반응시간 t에서 흡착제 단위질량당 흡착된 흡착질의 양(mg/g)
t : 반응시간(h)
k1 : 유사 1차 반응속도상수(1/hr)
k2 : 유사 2차 반응속도상수(g/mg·h)
h : 초기 흡착속도(mg/g·min)
또한 (식 10)을 사용하여 유사 1차 반응모델과 유사 2차 반응모델에 의해 계산한 흡착용량 값(qe,cal)과 실제 실험에 의해 구한 값(qe,exp)의 오차율(%)을 비교하였다.
연구결과
등온흡착실험 결과
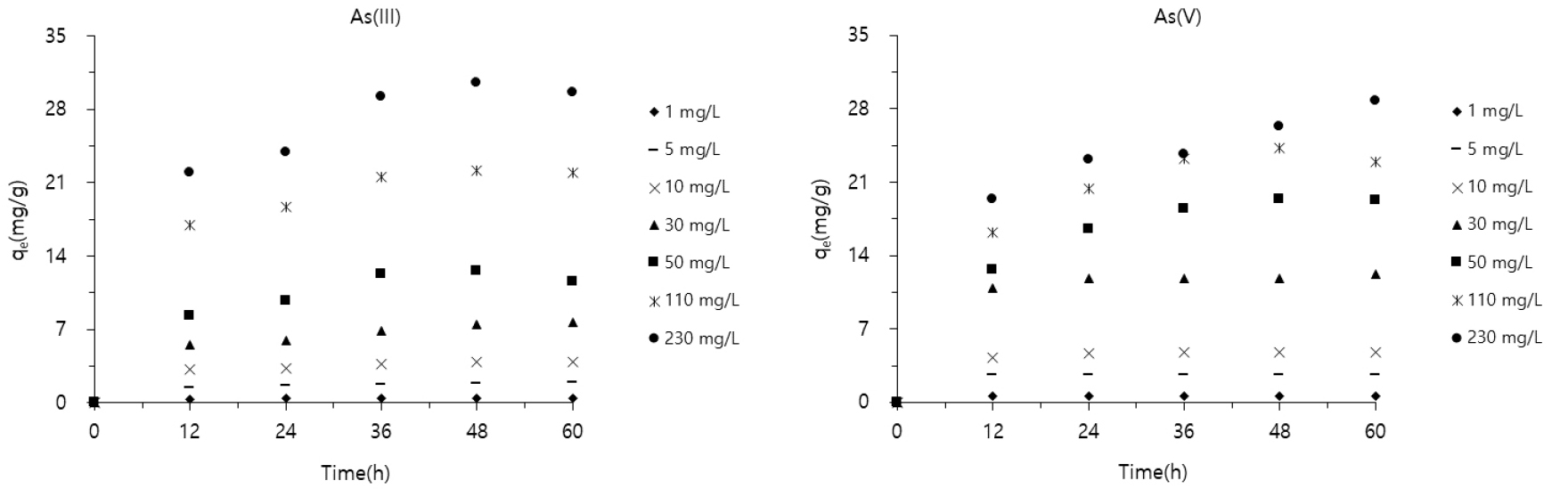
As(III)의 경우 초기 농도 30 mg/L 이하의 경우 48시간 지난 후에 흡착이 평형상태에 도달했으며, 50 mg/L 이상의 경우에는 36시간 지난 후에 평형상태에 도달하는 것을 확인 할 수 있었다. As(V)의 경우에는 초기 농도 30 mg/L 이하의 경우 12시간 지난 후에 흡착이 평형상태에 도달했으며, 50 mg/L 이상의 경우(230 mg/L 제외)에는 36시간 지난 후에 평형상태에 도달하는 것을 확인하였다(Fig. 2). 또한 초기 농도가 1 mg/L~50 mg/L인 경우에는 As(V)의 평형 흡착량(qe)값이 As(III)보다 더 많았으며, 그 밖의 110 mg/L, 230 mg/L 농도에서는 As(III)와 As(V)의 평형 흡착량(qe)이 비슷한 수준을 보였음을 확인하였다.
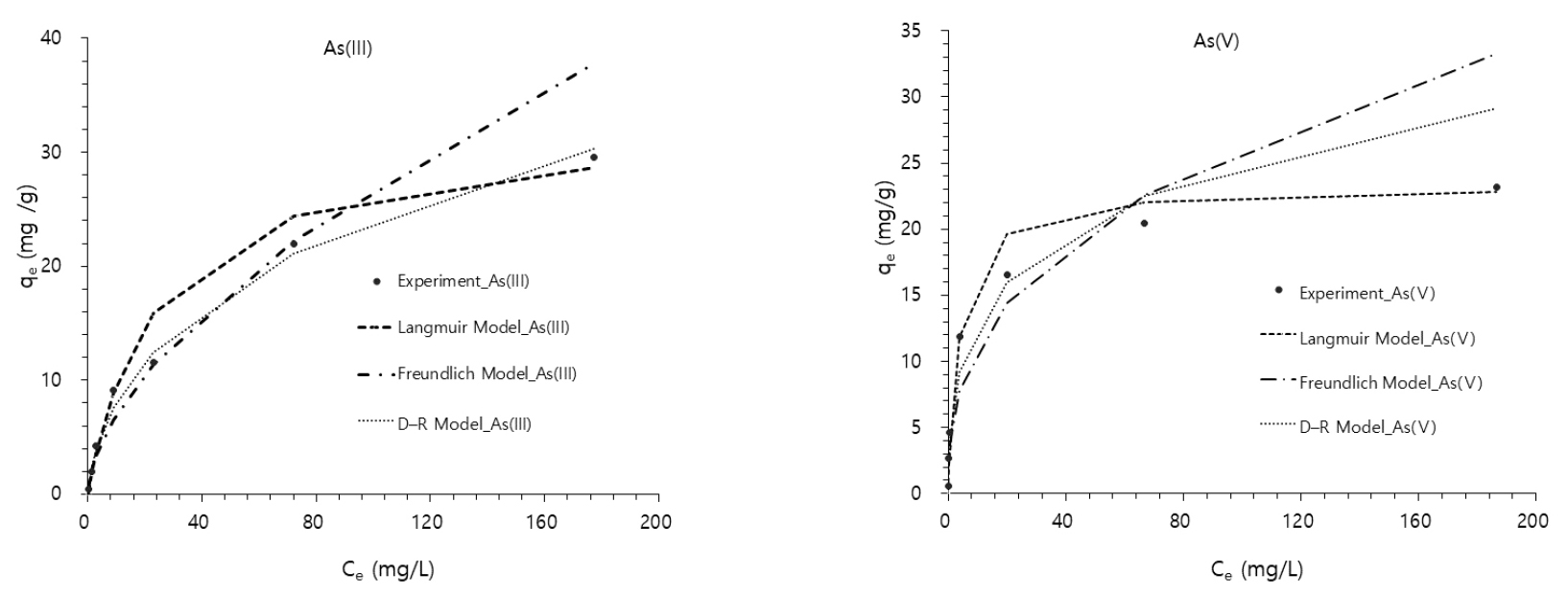
Fig. 3은 다양한 농도에서의 평형 흡착용량(qe)을 나타내며, 이는 실험값(qe,exp)과 다양한 등온흡착모델을 이용해 계산된 값(qe,cal)을 비교한 것이다. 초기 농도가 높을수록 실험적 흡착량이 유의미하게 증가하는 경향을 보였으며, 이는 선행 연구(Ahmed et al., 2024)와도 일치하는 결과이다. 이러한 경향은, 비소의 초기 농도가 흡착과정에서 더 강력한 추진력을 나타냄을 유추할 수 있다.
Table 2는 Langmuir, Freundlich 그리고 D-R 등온흡착실험으로부터 얻어진 결과를 흡착 매개변수값에 대하여 나타내었다. 각 모델의 상관계수(r2)를 비교한 결과, As(III)에서 각각 0.972, 0.980, 0.908을 보였으며, As(V)에서는 각각 0.997, 0.868, 0.991로 나타났다.
Table 2.
Comparison of isotherm model parameters for As(III) and As(V) adsorption onto T-sludge using Langmuir, Freundlich, and D–R models
최대흡착량(qmax)은 As(III)와 As(V)에 대하여 Langmuir 모델에서 각각 32.573 mg/g, 23.310 mg/g으로 계산되었으며, D-R 모델에서 각각 105.162 mg/g, 62.741 mg/g으로 Langmuir 값보다 2~3배 높게 나타났다. 실제 평형실험값(Ce)으로부터 얻은 최대 qe,exp 값은 29.600 mg/g, 23.168 mg/g 나타나 Langmuir 모델의 값과 더 일치하여 적합성을 보였으며, D-R 모델의 경우 신뢰성을 얻기 어려웠다. 이러한 결과는 다른 연구에서도 보편적으로 나타났던 결과와 유사하다(Na et al., 2012).
Langmuir 모델에서 흡착제의 친화도를 나타내는 KL값과 흡착공정의 유리함을 나타내는 RL 값을 확인한 결과, As(V)가 As(III) 비해 더 높은 흡착 성능을 나타내는 것을 확인할 수 있었다. D-R model로부터 구한 흡착에너지(E)값은 각각 10.136 kJ/mol, 13.021 kJ/mol 로 나타나 As(III)와 As(V)는 흡착제로 사용된 T-Sludge에 대해 이온교환에 의한 흡착으로 판단된다.
흡착 성능은 실험 조건 및 흡착제 종류마다 특성이 다르므로 직접적으로 비교하는 것은 어려우나, 본 연구재료인 슬러지의 흡착능력을 평가하기 위해 실험으로부터 얻은 최대흡착용량(qmax)을 선행 연구에서 보고된 철 기반 흡착제의 최대흡착용량(qmax)과 비교하였다(Table 3). 선행 연구에서 보고된 철 기반 흡착제의 최대흡착용량은 As(III)에서 0.66 mg/g~66.9 mg/g, As(V)에서는 0.05 mg/g~41.2 mg/g으로 다양하게 보고되었다. 본 연구에서 도출된 최대흡착용량(qmax)은 각각 32.57 mg/g, 23.31 mg/g으로, 이는 선행 연구에서 보고된 범위와 유사한 수준이다. 따라서 T-sludge는 흡착제로 활용이 가능할 것으로 판단된다.
Table 3.
Comparison of maximum adsorption capacities of T-sludge and previously reported iron-based adsorbents for As(III) and As(V) removal
| Adsorbent | Maximum adsorption capacity | Reference | |
| As(III) | As(V) | ||
| T-sludge | 32.57 mg/g | 23.31 mg/g | This study |
| Akaganeite | 29.2 mg/g | 36.7 mg/g | Kim et al. (2011b) |
| Ferrihydrite | 43.5 mg/g | 41.2 mg/g | |
| Iron-rich sludge | 66.9 mg/g | 21.5 mg/g | Yang et al. (2014) |
| Iron-coated manganese sand | 2.20 mg/g | 5.4 mg/g | Wu et al. (2011) |
| Red mud | 0.66 mg/g | 0.05 mg/g | Altundoğan et al. (2000) |
| Amorphous iron oxide | 28 mg/g | 7 mg/g | Lenoble et al. (2002) |
| Goethite | 22 mg/g | 7 mg/g | |
| GFH (commercial) | 1.75 mg/g | 1.17 mg/g | Lekic et al. (2013) |
| GFHa) | - | 24.36 mg/g | Kumar et al. (2020) |
| CMDS-PUb) | - | 7.26 mg/g | |
등적흡착실험 결과
pH변화에 따른 흡착반응속도를 평가하기위해 흡착질인 As(III)와 As(V) 용액은 농도 10 mg/L, 이때 용액의 pH는 pH 3, pH 5, pH 7, pH 9, pH 11로 조제하여 흡착실험을 진행하였으며, 시료는 1, 3, 6, 12, 24, 48시간 일 때 채취하여 As농도를 분석하였다.
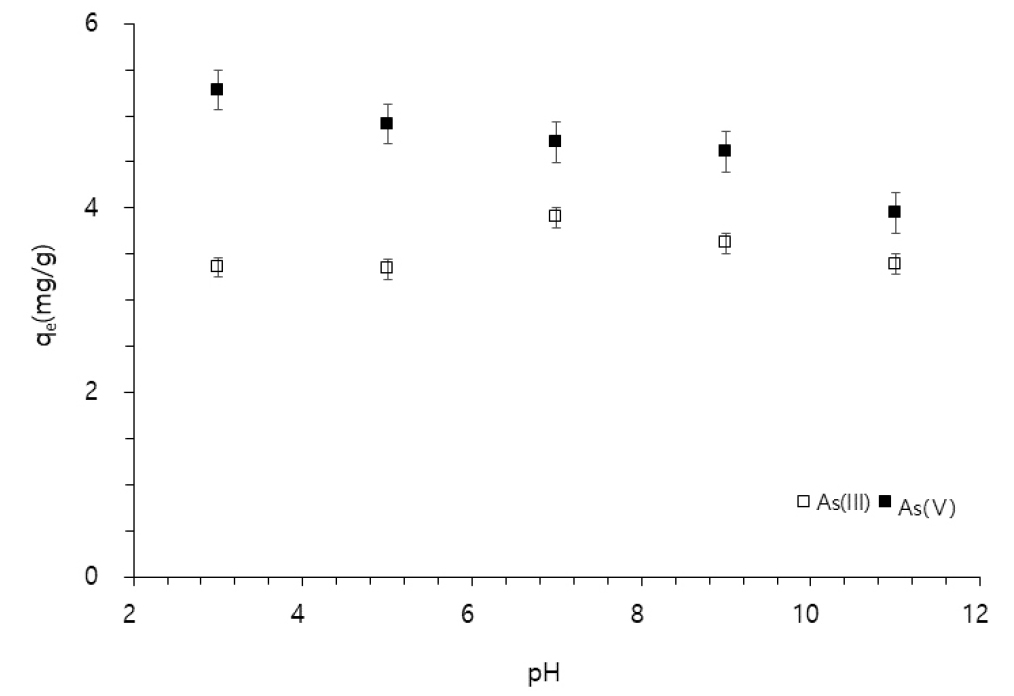
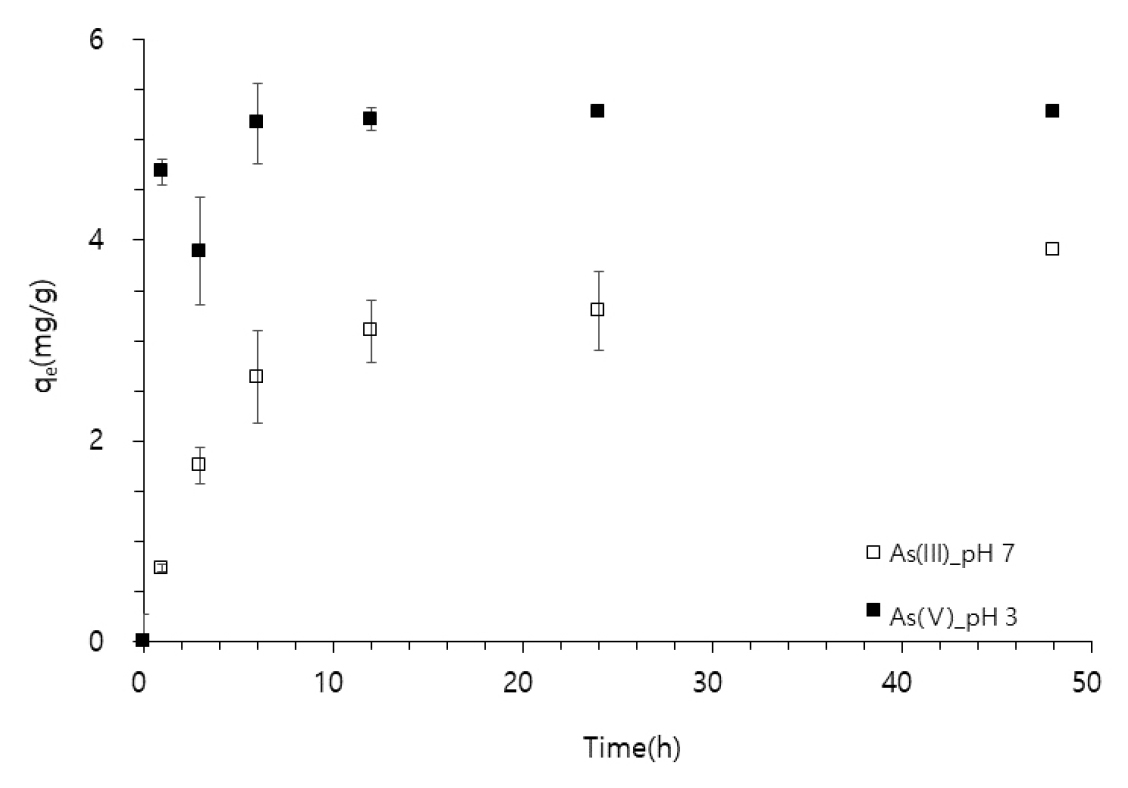
Fig. 4는 pH변화에 따른 흡착용량값(qe)을 나타낸 것으로 As(III)의 경우 pH 7까지는 증가하다 pH 9 이후로 감소하는 경향을 보였으며, As(V)의 경우 pH 증가에 따라 흡착용량값이 감소하는 경향을 보였다.
이와 같은 이유는 흡착제로 사용된 T-sludge의 영전하점(pHzpc)은 9.59로 pH가 영전하점보다 낮을 때 흡착제 표면은 양전하를 띠게 된다. 따라서 음전하를 띠고 있는 As와 정전기적 인력이 작용하여 흡착이 더 잘 일어난 것으로 판단된다. 다시 말해 As(III)는 pH 7 이하에서는 비전하(H3AsO30)상태로 주로 존재하여 흡착제와 전기적 반발력이 작으므로 낮은 pH에서 흡착량이 증가한 반면, As(V)는 pH 2.2 이상에서는 대부분 음이온 종(H2AsO4‒, HAsO42‒, AsO43‒ )으로 존재하기 때문에 흡착제 표면과 정전기적 반발력이 작용하여 pH상승에 따라 흡착량이 감소한 것으로 보인다. 또한 낮은 pH에서 흡착량이 높은 이유는 교반을 통한 응집 및 흡착에 따른 결과라고 판단된다. 이것은 낮은 pH 조건일 경우 As는 산화철 광물인 Ferrihydrite와 공침되어 더 효율적으로 제거할 수 있다는 결과와도 유사하다(Jeon et al., 2008).
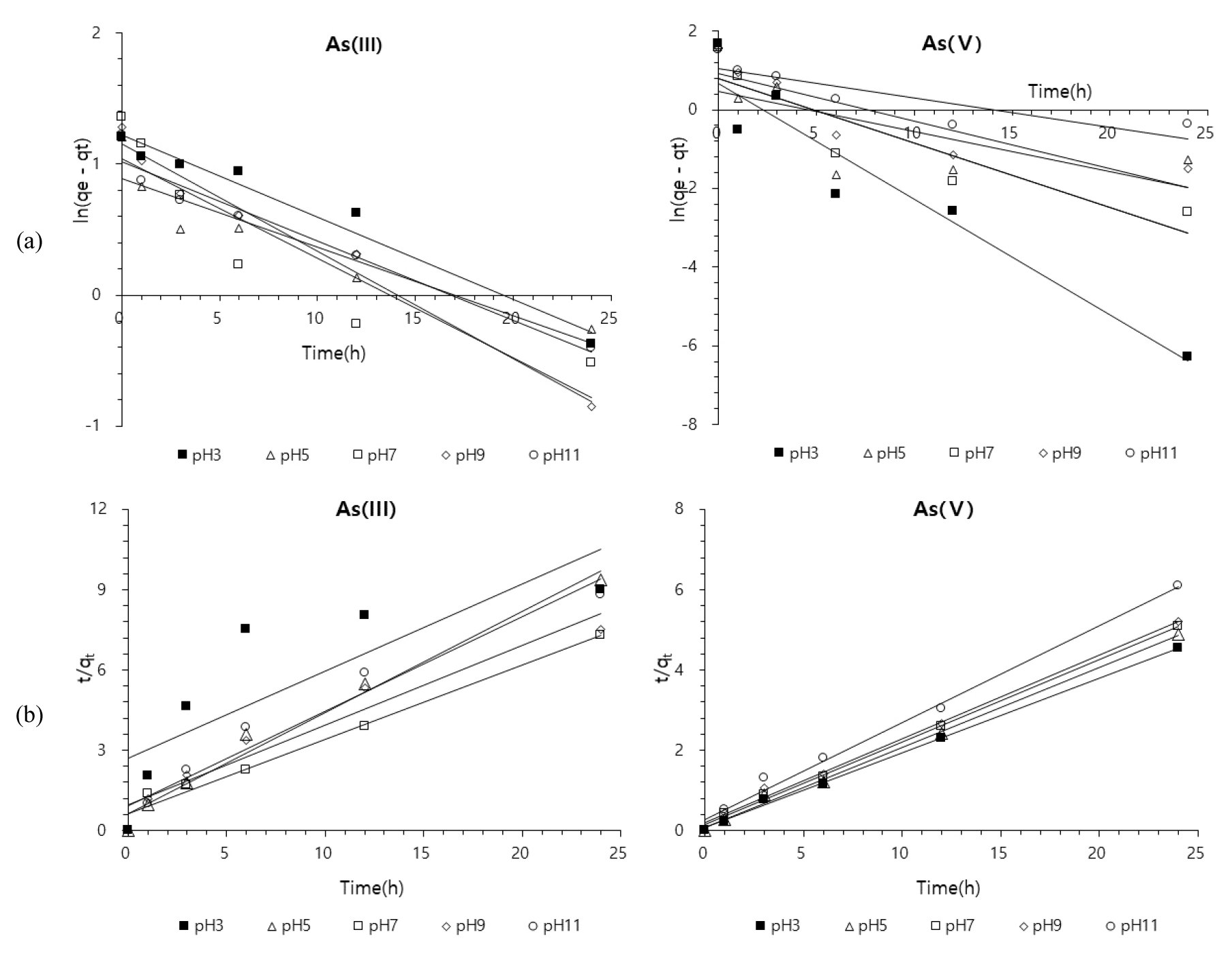
유사 1차 반응 모델과 유사 2차 반응 모델에 적용한 결과를 매개변수값에 대하여 Table 4에 나타내었다. As(III)에 대해 유사 1차 반응 모델의 평균상관계수 값은 0.920 이고 유사 2차 반응 모델의 평균상관계수는 0.904로 나타났다. 그러나 유사 2차 반응 모델에서 As(III)의 pH 3 일 경우를 살펴보면 12, 24시간일 때 흡착속도가 초기에 비해 떨어져서 비선형적으로 나타나 상관계수가 낮은 것을 확인할 수 있었다(Fig. 5). 이러한 이유는 흡착제가 양전하를 띠는 낮은 pH에서 As(III)가 비전하를 띠기 때문에 흡착제와 인력이 약해져 흡착속도가 감소한 것으로 판단된다. 실제 As(III), pH 3에서의 12, 24시간를 제외한 실험결과에서 유사 2차 반응 모델에 따라 계산하면 상관계수는 0.967, 초기흡착속도(h)는 2.004로 나타나는 것으로 확인되었다.
Table 4.
Kinetic model parameters of the pseudo-first-order and pseudo-second-order adsorption for As(III) and As(V) onto T-sludge at different pH levels
As(V)의 경우 유사 1차 반응 모델의 평균상관계수는 0.745, 유사 2차 반응 모델의 평균상관계수는 0.996으로 나타났다. Table 5는 실험으로부터 구한 평형흡착량(qe,exp)과 유사 1차 반응 모델과 유사 2차 반응 모델에 의해 계산된 평형흡착량(qe,cal)를 비교하여 나타냈으며, 이에 따른 오차율도 나타내었다. 그 결과 유사 1차 반응 모델에 의해 계산된 값은 실제 실험으로부터 구한 흡착량과 1.14%~69.55%의 오차율을 보였으며, 유사 2차 반응 모델은 1.01%~20.60 %의 오차율 보였다. 이와 같은 결과에 의하면 흡착반응속도를 잘 표현하는 모델은 유사 2차 반응 모델로 판단된다.
Table 5.
Comparison of experimental and model-predicted equilibrium adsorption capacities (qe) and their relative errors for As(III) and As(V) using dynamic adsorption models
가장 흡착용량값(qe)이 많았던 As(III)의 pH 7일 때와 As(V)의 pH 3일때의 반응속도상수(k2) 및 초기흡착속도(h)를 비교시, As(V)에서의 k2, h 값이 As(III)보다 각각 4.26배, 9.41배 더 높은 것으로 나타났다. 또한 As(V)의 경우는 흡착제 접촉 6시간 이후의 시료에서 흡착량 값에 큰 변화가 없는 것으로 나타난 반면, As(III)의 경우에는 24시간까지 계속 흡착량이 증가하는 양상을 보여 흡착속도가 느리다는 것을 알 수 있었다(Fig. 6).
결 론
본 연구에서는 산업부산물인 폐석탄슬러지(T-Sludge)의 비소 흡착 가능성을 평가하여, 이를 수처리용 흡착제로 재활용 할 수 있는지를 검토하는데 목적이 있다. 이를 위해 T-Sludge를 흡착제로 이용한 등온흡착실험과 동적흡착실험을 수행하였으며, As(III)와 As(V)에 대한 흡착량, 흡착 속도 및 메커니즘에 대한 분석을 통해 다음과 같은 결론을 도출하였다.
1. 초기농도 50 mg/L 이하에서는 As(V)가 As(III)보다 빠르게 평형에 도달하며, 많은 흡착량(qe)을 나타냈고, 고농도인 230 mg/L에서는 As(III)와 As(V)의 흡착량(qe)이 유사한 수준을 보였다. 이러한 결과는 As(III)가 상대적으로 느린 흡착속도를 가지지만, 고농도 조건에서는 더 많은 흡착이 가능한 잠재력을 지난다는 것을 시사한다. 반면 As(V)는 저농도에서는 빠르게 흡착되며, 고농도에서는 충분한 접촉시간이 확보될 경우 더 높은 흡착량에 도달할 수 있음을 시사한다.
2. 등온흡착실험결과 As(III)에 대해서는 Langmuir, Freundlich 모델의 상관계수값이 비슷하였으나, As(V)에서는 Langmuir 모델이 더 적합성을 보였다. Langmuir 모델 적용 결과, As(III)는 더 높은 이론적 최대 흡수량(qmax)을 나타냈으나, 흡착 친화도(kL)는 As(V)보다 낮게 나타났다. 반면 As(V)는 낮은 최대 흡수량(qmax)에도 불구하고 높은 흡착 친화도를 보여 낮은 농도에서의 흡착 효율이 우수함을 확인하였다.
3. D-R 모델 결과, As(III)와 As(V) 모두 이온교환 기반의 화학적 흡착 메커니즘에 의해 제거됨을 확인하였다.
4. 동적흡착실험에서는 유사 2차 반응 모델이 흡착 속도를 잘 설명하였으며, As(V)의 반응속도상수(k2) 및 초기흡착속도(h)가 As(III)보다 각각 4.26배, 9.41배 더 높아 빠른 흡착 특성을 보였다.
이러한 결과는 T-sludge의 비소 제거 가능성을 입증하며, 향후 수처리 공정에 적용하기 위한 기초자료로 활용될 수 있다.