서 론
토양은 수자원과 함께 매우 중요한 자연자원으로서 토양이 유실되거나 오염되면 식물, 동물, 인간에게 미치는 영향은 매우 치명적이다. 적절한 복원시설이 설치되지 않은 채 방치된 폐광산에서 발생한 폐기물 내 중금속은 다양한 물리적·화학적 반응을 통해 토양을 비롯한 주변 환경으로 이동, 확산한다(Jung et al., 2004; Kim et al., 2018; Choo and Lee, 2019). 특히 농경지 토양은 인간과 동물에게 중요한 식량을 제공한다는 측면에서 독성물질에 의한 오염 발생은 더욱 심각한 결과를 초래할 수 있다. 독성 물질 가운데 중금속과 같은 무기 오염물질은 유기 오염물질과는 달리 생물학적 또는 화학적 분해가 되지 않은 채 농경지에서 재배되는 작물을 통해 먹이사슬에 진입하여 생체농축을 통해 점차 축적된다. 이는 궁극적으로 인체에 직접적이고 유해한 영향을 미치게 되므로 인간의 보건 및 생명에 큰 위협이 된다.
중금속 오염토를 정화하기 위하여 다양한 기술이 개발되었으나 이를 농경지에 적용하기에는 많은 제한요소가 존재한다. 특히 토지를 집약적으로 사용하여야 하는 국내 실정상 농업활동이 지속적으로 수행되어야 하며, 토양을 보유하고 있는 농민의 재산권을 보호하는 측면에서도 작물생산 기능을 파괴하지 않는 선에서 농경지의 기능과 생태적 건강성을 유지할 수 있는 복원 공법을 수행해야 한다. 이에 시공이 간단하고, 비용과 시간 소모가 적으며, 토양 생태계를 크게 저해하지 않고, 효율적 결과를 기대할 수 있는 중금속 안정화(stabilization) 기술이 오염 농경지 복원에 적절한 방법으로서 현장에 널리 적용되고 있다(Yang et al., 2008; Ok et al., 2011). 안정화 기술은 오염토에 다양한 안정화제를 투입하여 중금속을 안정한 형태로 변환시킨다. 이는 오염물질의 이동성(mobility) 저감과 생물학적 이용가능성(bioavailability) 감소의 효과를 거둘 수 있을 뿐만 아니라 시공이 비교적 빠르고 운영이 간단하다는 장점이 있어 특히 중금속으로 오염된 대면적 농경지에 적합하다.
그러나 안정화제 처리 심도보다 더 하부의 토양이 중금속으로 오염된 경우, 시간이 경과하며 하부 중금속이 상부로 이동하여 근권 오염 현상이 재발하는 경우가 발생할 수 있다. 광산 주변의 중금속으로 오염된 농경지 토양 개량 및 정화사업 수행 시 표토는 객토, 환토, 복토 등의 작업을 수행하고 중간층에 석회석 및 제강슬래그 등을 이용한 안정화층을 배치하는 공법이 주로 적용되는데, 복원 완료 후 수 년이 경과하면 복원된 필지에서 재배한 작물의 중금속이 허용기준을 초과하는 경우도 있다. 이는 안정화제의 기능이 소진되고 토양 하부의 중금속이 모세관압에 의해 오염된 심토에서 근권으로 상향 이동한데 기인한다(Aloud, 2012; Boduroglu and Bashir, 2022; Zhao et al., 2023). 이를 방지하기 위하여 심부토양 층위까지 안정화 공법을 적용하는 방안을 생각할 수 있으나 이는 토양 굴착비 등 막대한 비용이 발생해 실행이 곤란할 것이다. 이러한 경우, 높은 시공비가 요구되지 않는 방법인 혐기성 심토에 적절한 황산염환원균(SRB, sulfate-reducing bacteria)을 적용하는 방법을 통하여 중금속을 원위치에 안정화시키는 효과를 기대할 수 있다.
SRB는 편성혐기성세균(obligate anaerobe)으로 황산이온(SO42-)을 전자수용체, 유기물을 전자공여체로 이용하며 혐기성 호흡을 하는 세균이다(McMohan and Daugulis, 2008; Eqs. 1, 2).
그 결과 생성된 S2-, HS-, H2S 등은 용존 금속과 매우 강하게 결합하여 불용성의 화합물을 형성한다(Sheoran et al., 2010; Eq. 3).
이러한 SRB의 지구미생물학적 특징은 중금속으로 오염된 광산배수의 자연정화처리에 적합하여 유망기술로 주목받고 있으나(Lens et al., 2002; Jong and Parry, 2004; Yoo et al., 2006; Le Pape et al., 2017), 토양에 이를 적용하여 중금속을 원위치 안정화하려는 예는 드문 형편이다. Papassiopi et al.(2009)은 S0 환원균인 Desulfuromonas palmitatis를 이용하여 토양 내 Cr을 안정화하였을 경우 Cr이 용이하게 용출되지 않는 형태로 변화하는 것을 밝혔으며, Hu et al. (2007)은 SO42-를 처리한 토양에서 철황화물 형성으로 인해 벼에 의한 As 흡수가 감소함을 밝힌 바 있다. Peng et al. (2018)은 대표적 SRB인 Desulfobacteraceae 및 Desulfobulbaceae를 이용한 166일 간의 처리를 통해 퇴적물 내의 Cd를 안정화하였으며, SRB와 polyvinyl alcohol을 같이 사용하여 Pb, Zn, Cu, Cd를 안정화한 연구 결과도 보고된 바 있다(Li et al., 2017). 국내에서도 SRB에 의한 비소 및 중금속 고정화에 관한 보고가 발표된 바 있다(Ha et al., 2006; Lee et al., 2006; Song et al., 2007; Ko et al., 2009; Jang et al., 2009; Kim et al., 2011).
이 연구에서는 SRB가 SO42-를 전자수용체로 이용하는 혐기성 호흡을 통해 접근이 어려운 심부 토양 내 용존 중금속을 안정화하는 실험을 통해 다양한 중금속으로 오염된 농경지에 대한 경제적이고 효율적인 처리 방안 수립 과정에 유용한 정보를 제공하고자 하였다. 또한 SRB를 이용한 기존의 중금속 안정화 연구에서는 주로 토양수 또는 상등액을 채취하여 용존 중금속의 농도 변화를 측정하였으나(Ko et al., 2009; Jang et al., 2009; Kim et al., 2011), 이 연구에서는 용존 함량뿐만 아니라 0.1 N HCl 및 Mehlich3(이하 Mehlich)를 이용한 단일용출법을 적용함으로써 토양 내 중금속의 안정화 효율을 확인하고자 하였다. 현재 토양 단일용출법을 이용하여 안정화 효율을 추정하는 연구가 널리 수행되고 있음을 감안할 때(Han et al., 2020a, 2020b; Jo et al., 2022), 이는 SRB를 이용한 안정화 공법 적용 후 토양을 채취하여 단일용출법을 적용함으로써 중금속의 생물학적 이용도 정도를 파악하는데 유용한 자료를 제공할 수 있을 것이다.
연구방법
토양 시료의 물리화학적 특성
중금속으로 오염되었을 가능성이 큰 폐광산 주변 2 km 이내의 농경지를 대상으로 토양시료를 채취하여 안정화 실험을 수행하였다. 시료는 전남 광양시 옥룡면 석동광산 인근 밭토양에서 2개(시료명 B1, B2), 전남 보성군 복내면 계산리 산양광산 인근 논토양에서 1개(시료명 E25)를 채취하였다. 채취한 토양은 암편과 불순물을 육안으로 선별, 제거한 후 실내(20°C)에서 자연건조하였다. 그 후 토양 물성 조사와 안정화 배치 실험을 위해 10 mesh(<2 mm) 및 80 mesh (<0.18 mm)로 체거름하였다. 체거름한 토양은 지퍼백(zipper bag)에 담아 밀봉한 후 실온에서 보관하였다.
2 mm 이하 시료는 토양 pH, 작열감량(LOI, loss-on-ignition) 양이온교환능력(CEC, cation exchange capacity) 분석 및 미생물을 접종한 안정화 배치 실험에 사용하였다. 0.18 mm 이하의 토양은 왕수를 이용한 중금속 전함량분석 수행에 사용하였다. 토양 pH는 토양오염공정시험법을 기준으로 토양을 탈이온수로 1 시간 진탕한 후 60초 이내에 pH meter(Hanna Instruments, USA)를 이용해 측정하였다. 토양 CEC를 측정하기 위하여 1 M sodium acetate 용액과 토양 0.5 g을 반응시켜 토양 내 치환성 양이온과 Na를 치환하였다. 토양 내 Na를 1 M ammonium acetate 용액으로 치환한 뒤 치환되어 나온 Na 농도를 ICP-OES(Spectro, Germany)로 측정하였다(Busenberg and Clemency, 1973). 유기물 함량은 105°C와 550°C 조건에서 각각 1시간 및 4시간 가열한 LOI 측정을 통해 계산하였다.
토양 내 중금속의 전함량을 측정하기 위하여 토양을 왕수로 분해한 후 Fe, Mn, Pb, Zn, Cu, Cd, Ni, 총 Cr, As, Sb를 ICP-OES로 정량하였다. 동시에 상대적으로 약한 추출제를 이용해 용출함으로써 식물체 전이가 가능한 중금속의 함량을 추정할 수 있는 단일용출법을 수행하였으며, 단일용출제로는 0.1 N HCl 및 Mehlich를 사용하였다. Mehlich 용액은 아래와 같이 제조하였다.
i) Stock solution M-3
:55.56 g NH4F + 29.23 g EDTA(F.W. 292.24) in 1 L deionized water(DIW)
ii) Mehlich solution
:200.1 g NH4NO3 + 100 mL stock solution M-3 + 115 mL CH3COOH + 82 mL 10% HNO3 in 10 L DIW
Mehlich 용출은 체거름한 토양시료 0.5 g을 15 mL 코니칼 튜브에 정량한 후, Mehlich 용출액 5 mL을 주입하고 120 rpm으로 5분간 교반하여 중금속을 용출하였다. 0.1 N HCl 용출법은 토양시료 1 g에 5 mL의 0.1 N HCl을 주입하여 1시간 동안 100 rpm에서 교반하였다. 용출 후 원심분리(4000 rpm, 5분)하여 상등액을 0.45 µm 필터로 여과하였다. 단일용출법을 통한 중금속 함량은 ICP-MS(Agilent, USA)를 이용하여 측정하였다.
미생물 배양
실험에 사용한 SRB는 Desulfovibrio desulfuricans로서 한국생명공학연구원 생물자원센터(KCTC)에서 분양받았으며 동결 건조 상태의 균을 액체배지에 접종 및 활성화시켜 사용하였다. SRB 배양액은 다음 조성을 갖는 Solution A, B, C를 혼합하여 제조하였다. ① Solution A: K2HPO4 0.5 g, NH4Cl 1.0 g, Na2SO4 1.0 g, CaCl2·2H2O 0.1 g, MgSO4·7H2O 2.0 g, CH3CH(OH)COONa solution 50%, 4.0 mL, 효모추출물(yeast extract), 1.0 g, resazurin 1.0 mg, DIW 980.0 mL, ② Solution B: FeSO4·7H2O 0.5 g, DIW 10.0 mL, ③ Solution C: Na-thioglycolate 0.1 g, ascorbic acid 0.1 g, DIW 10.0 mL. 제조한 배지는 배양병(serum bottle)에 넣어 121°C에서 15분간 멸균하여 사용하였으며, 1 M HCl과 1 M NaOH를 이용하여 최종 pH를 7로 맞춘 후 질소 가스로 2시간 배기(purging)하여 용존산소를 제거한 후 혐기조건에서 SRB를 접종하여 37°C에서 배양하였다. 이 과정을 3번 반복하여 순수한 균체를 얻었으며 계대배양이 반복될수록 용액 내 검은색 침전물이 발생하여 SRB가 활성화된 것을 확인하였다(de Matos et al., 2018).
안정화 배치 실험
실험은 첨가된 SRB와 SO42-의 농도 그리고 토착미생물(indigenous bacteria)의 영향 인자에 따른 중금속의 미생물학적 안정화 효율을 평가하기 위해 다음과 같이 구성하였다. ① 토착미생물의 SO42- 환원 정도를 알기 위하여 SO42-만 주입한 시료(시료명 SO4), ② SRB가 토양 내 자연적으로 존재하는 SO42-를 이용하는지 여부를 관찰하기 위하여 멸균 토양에 SRB만 주입한 시료(시료명 SRBo), ③ 토착미생물이 살아 있는 상태에서 SO42-와 SRB를 모두 주입한 시료(시료명 SS).
실험에 사용한 토양 시료는 실험 전 충분히 교반하여 최대한 균질성을 유지하려 하였다. 무생물 비교시료(control)는 고압멸균한 토양 시료 10 g에 위 SRB 배양액 50 mL을 주입하였다. SO4 시료는 멸균하지 않은 토양 10 g에 배양액 50 mL을 주입하였으며 이 때 SO42-를 추가로 첨가해 최종 SO42- 농도 1,400 mg/L이 되게 하였다. SRBo 시료는 고압멸균한 토양 시료 10 g에 안정기(stationary phase)의 D. desulfuricans 접종액 5 mL을 포함한 배양액 50 mL을 주입하였다. 이 때 배양액은 SO42- 대신 Cl-로 대체하여 제조하였다. SS 시료는 멸균하지 않은 토양 10 g에 D. desulfuricans 접종액 5 mL을 포함한 배양액 50 mL을 주입하였으며 배양액 내 SO42-농도는 1,400 mg/L로 조정하였다. 모든 실험은 혐기 조건에서 이중시료(duplicate)를 이용하여 중복으로 수행하였으며, 항온 진탕배양기(37°C) 내에서 9주간 배양하였다.
세 종류의 토양시료에 대하여 비교시료, SO4 시료, SRBo 시료, SS 시료별로 1주, 4주, 7주, 9주에 배양병을 하나씩 개봉하여 토양을 회수하였으며, 0.1 N HCl과 Mehlich 단일용출법을 적용한 후 ICP-MS를 이용하여 Pb, Zn, Cu, Cd, Ni, 총 Cr, As, Sb를 분석하였다.
한편, 1주, 4주, 7주, 9주에 토양 이외에 상등액도 채취하여 pH를 측정(1주, 4주, 7주)하였으며 용존 중금속 함량을 측정하기 위해 0.2 µm로 필터링한 후 ICP-MS를 이용하여 정량하였다.
결과 및 해석
토양 시료의 물리화학적 특성
연구 대상인 토양시료(밭토양 B1, B2, 논토양 E25)의 pH, CEC, 유기물 함량 및 왕수분해 후의 As, Sb 및 각종 중금속 함량을 Table 1에 나타내었다. pH의 경우 5.9~6.6으로서 대체로 약산성을 띄며, CEC의 경우 우리나라 농경지 토양(평균 10 cmolc/kg; Song et al., 2019)과 비교하여 다소 높은 값(11.8~12.9 cmolc/kg)을 가진 것으로 나타났다. 유기물 함량은 6.8~8.3%로서 대체로 CEC와 비례하는 경향을 보였다. 왕수를 이용한 토양의 전함량 분석 결과, E25 토양 내 As가 82 mg/kg으로서 1지역 토양오염우려기준(25 mg/kg) 및 대책기준(75 mg/kg)을 크게 초과하였다. 이 외 Pb, Zn, Cu, Cd, Ni 등은 모두 우려기준보다 낮은 함량을 보였다.
Table 1.
pH, CEC, organic matter content, and total heavy metal content (mean ± standard deviation) of the investigated soil samples following aqua regia extraction (nd: not determined)
한편, 0.1 N HCl 및 Mehlich를 이용하여 토양 시료를 단일용출한 결과를 Table 2에 수록하였다. Pb, Zn, Cu, Cd 등 일반 비금속(base metal)의 경우 0.1 N HCl로 용출한 함량이 Mehlich로 용출한 함량에 비해 높게 나타났으나, As와 Sb 등 준금속은 Mehlich 용출량이 높게 나타났다.
토양 단일용출을 통한 안정화 효율 평가
안정화 효율은 Eq. 4와 같이 정의하였다.
이 때, Cc: 비교시료의 농도, Cs: 안정화제 처리 시료의 농도.
실험 결과, 각 토양, 중금속, 단일용출제에 대하여 안정화 효율의 시간에 따른 일관된 감소 또는 증가는 거의 관찰되지 않았다. 이는 아마도 토양 시료의 불균질성, 미생물 군집의 변화, 0.1 N HCl 및 Mehlich의 중금속에 대한 제한적 용출, 원래 토양 내 중금속의 낮은 함량 등에 기인한 것으로 보인다. 따라서 이 실험에서는 임의적으로 각 원소별로 시료채취 시기에 관계없이 전체 분석 횟수의 70% 이상에서 양의 안정화 효율을 나타낸 경우, 비교시료에 비하여 높은 안정화 효율이 나타난 것으로 감안하였다.
Table 2.
Concentrations of extracted heavy metals (mean ± standard deviation) of the investigated soil samples following 0.1 N HCl and Mehlich extraction (nd: not determined)
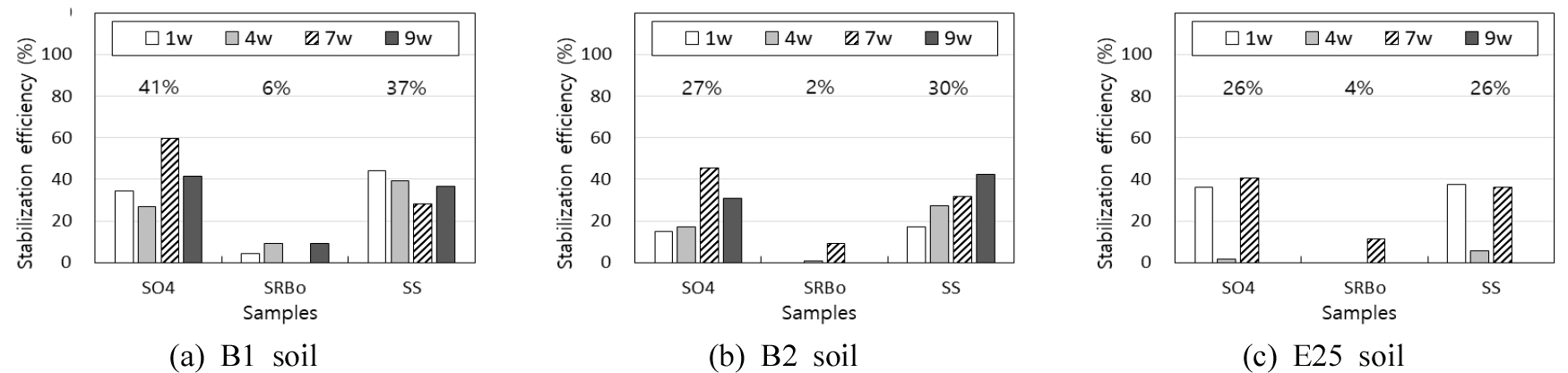
0.1 N HCl을 이용한 단일용출 결과를 바탕으로 세 토양 시료의 안정화 효율을 구한 결과 중금속 중 Pb만 비교시료에 비하여 안정화 효율이 높게 나타났다(Fig. 1). Pb의 안정화 효율은 SO4, SRBo, SS 시료에서 각각 26~41%, 2~6%, 26~37%를 보여, 토양에 인위적으로 SO42-를 주입하여 토착 SRB를 활성화하거나(SO4 시료) SO42-와 SRB를 모두 주입한 경우(SS 시료)에는 일정 정도 안정화가 이루어졌으나, 멸균 토양에 SRB를 인위적으로 접종한 경우(SRBo 시료) 황화물 형성을 통한 안정화 효율은 낮은 것으로 나타났다. SPSS(IBM SPSS Statistics 26)를 이용하여 일원분산분석(ANOVA)을 수행한 결과, 95% 신뢰구간에서 SRBo의 안정화 효율은 SO4 및 SS에 비하여 통계적으로 유의하게 낮은 것으로 나타났다. 이는 아마도 토양 자체에 존재하는 SO42- 함량이 낮아 SRB가 이를 효과적으로 전자수용체로 이용할 수 있는 용량이 부족하기 때문으로 보인다. 한편 Pb의 경우, 토양에 주입한 SO42-가 Pb2+와 결합하여 용해도가 매우 낮은 PbSO4(s)를 화학적으로 형성, 침전함으로 인해 낮은 안정화 효율을 보였을 가능성이 있다(Han et al., 2009). 이 연구에서는 둘 중 어느 메커니즘이 우세하게 작용하였는지의 실험은 따로 수행하지 않았다.
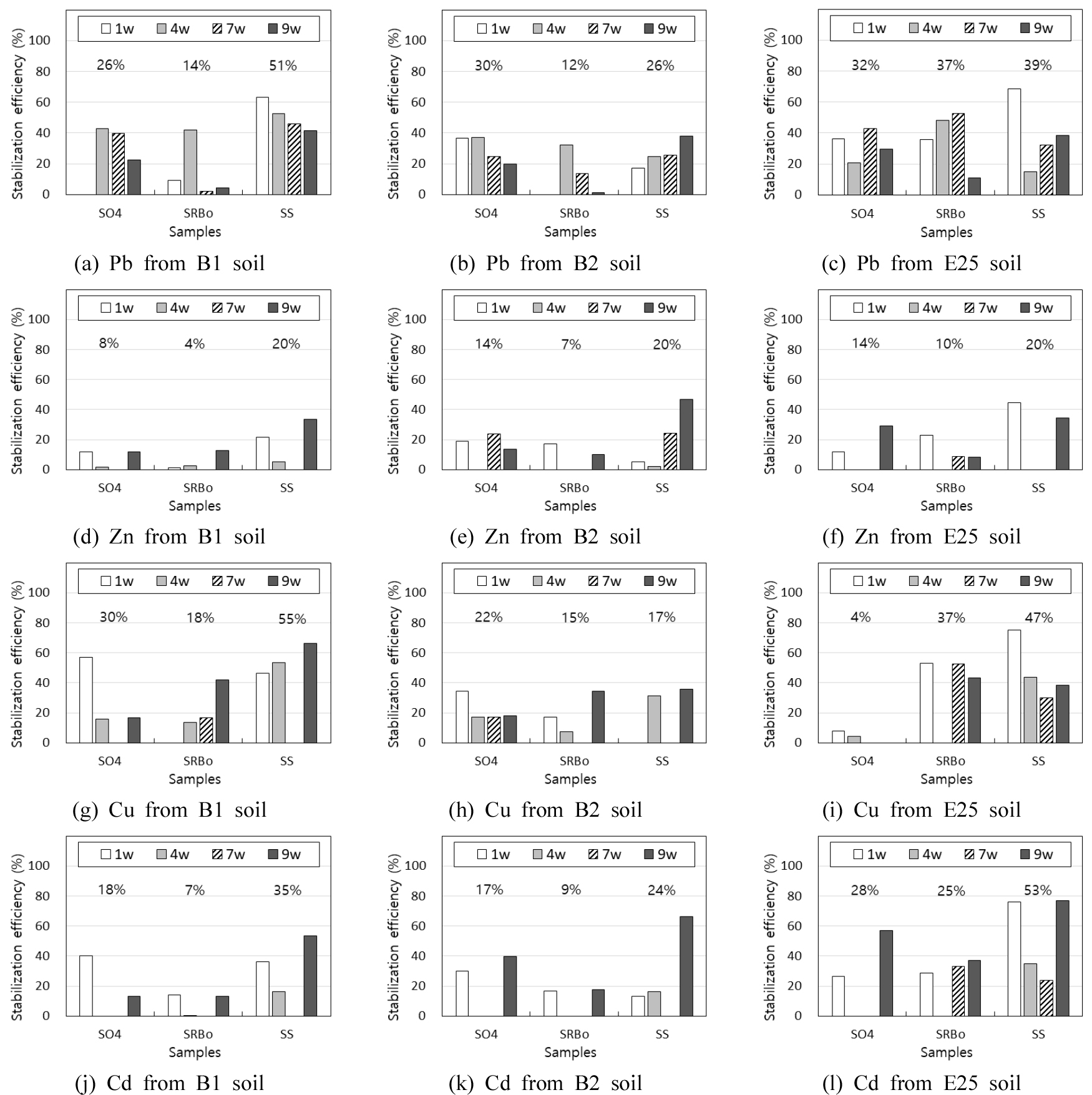
Mehlich를 이용한 단일용출 결과 나타난 세 토양 시료의 안정화 효율을 Fig. 2에 도시하였다. Mehlich로 토양을 용출한 결과, Pb, Zn, Cu, Cd의 안정화 효율이 비교시료에 비하여 높은 것으로 나타났다. Pb의 안정화 효율은 SO4, SRBo, SS 시료에서 각각 26~32%, 12~37%, 26~51%, Zn의 경우 8~14%, 4~10%, 20%, Cu의 경우 4~30%, 15~37%, 17~55%, Cd는 17~28%, 7~25%, 24~53%의 안정화 효율을 보였다. 일원분산분석 수행 결과, SS의 안정화 효율이 SO4와 SRBo에 비하여 통계적으로 높은 것으로 나타났으며, 또한 Pb의 안정화 효율이 Zn에 비하여 높게 나타났다. Ni, 총 Cr, As Sb의 경우에는 비교시료에 비하여 높은 안정화 효율이 나타나지 않았다.
0.1 N HCl과 Mehlich의 용출 결과를 고려할 때, 세 시료 중 SO4와 SS 시료에서 좋은 안정화 효율을 보였으며, 특히 SS, 즉, SO42-와 SRB를 모두 주입한 시료에서 가장 높은 안정화 효율을 보였다. 이 결과를 통해 볼 때, Mehlich 용출의 경우, SO42-만 주입한 시료인 SO4에 대해서도 안정화 효율이 높게 나타난 것은 토착미생물 중 SRB가 존재하여 공급한 SO42-를 이용하여 중금속을 황화물 형태로 침전시켰기 때문으로 생각된다. SRB와 SO42-를 동시에 주입한 SS 시료의 경우 다른 시료에 비하여 상대적으로 높은 안정화 효율을 보였는데 이는 미생물과 전자수용체를 동시에 공급할 때 심부 토양에서 SRB에 의한 중금속 안정화가 효과적으로 발생할 수 있음을 나타내는 것이다. 그리고 SO4와 SS 시료에 비하여 SRBo 시료에서 낮은 효율을 보인 결과는 토착미생물 군집 내에 존재하는 SRB를 활성화하기 위해서는 별도의 SO42-를 주입해야 한다는 것을 지시한다. Joo et al.(2014)은 SRB에 SO42-를 제공한 경우, Cu의 경우 약 2배, Zn은 약 10% 제거율이 증가하는 결과를 보인 바 있다.
준금속인 As의 경우, 모든 용출법에서 명확한 안정화 효과를 보이지 않았다. 시간에 따라 토양 상등액의 pH를 측정한 결과, B1 토양의 경우 평균 pH는 1주차 5.8, 4주차 8.2, 7주차 7.3, B2 토양의 경우 1주차 6.1, 4주차 8.5, 7주차 7.2, E25 토양의 경우 1주차 6.8, 4주차 8.5, 7주차 7.5로 나타나, 시간이 경과하며 pH가 크게 상승함을 보였고 특히 4주차 시료에서 가장 높은 pH를 나타내었다. pH의 증가는 SRB의 대사작용 결과 생성되는 HCO3-에 의한 알칼리도 증가와 연관이 있다(Kim et al., 2008). 용존 As는 pH 증가에 의해 흡착 능력이 감소하여 함량이 증가하므로, 관찰된 As의 낮은 안정화 효율은 pH 상승 및 그에 따른 이동도 증가에 기인한 것으로 보인다. pH 변화에 따른 As 거동에 관한 SRB의 역할에 관한 후속 연구가 진행될 필요성이 있다.
한편, 0.1 N HCl은 Pb만 비교시료에 비하여 높은 안정화 효율을 보인 것으로 나타난 반면, Mehlich는 Pb, Zn, Cu, Cd에 대한 안정화 효과를 지시할 수 있는 것으로 나타났다. 이는 Table 2에서 볼 수 있듯이 일반 비금속(base metal)의 경우 0.1 N HCl이 Mehlich에 비하여 용출능이 높았으므로, SRB에 의해 생성된 침전물의 안정도가 두 용출제의 용출능 사이에 존재하기 때문으로 보인다. SRB를 이용한 토양 내 중금속의 안정화를 추정하기 위하여 토양에 단일용출제를 적용할 경우 0.1 N HCl 보다는 Mehlich가 더욱 많은 중금속의 안정화 효과를 지시할 수 있는 것으로 나타났다. 한국광해광업공단에서는 안정화 기술의 유효성을 평가하기 위해 다양한 단일용출법을 평가한 결과, Mehlich 용출법이 가장 적합한 용출법이라고 보고한 바 있다(Han et al., 2020b). 즉 심부 토양에서의 중금속 안정화를 도모하기 위하여 SRB를 투입하였을 때, 침전된 중금속 이차 광물의 안정성을 지시하는 데에는 Mehlich 용출법이 더욱 적절할 것으로 보인다.
상등액 분석 결과
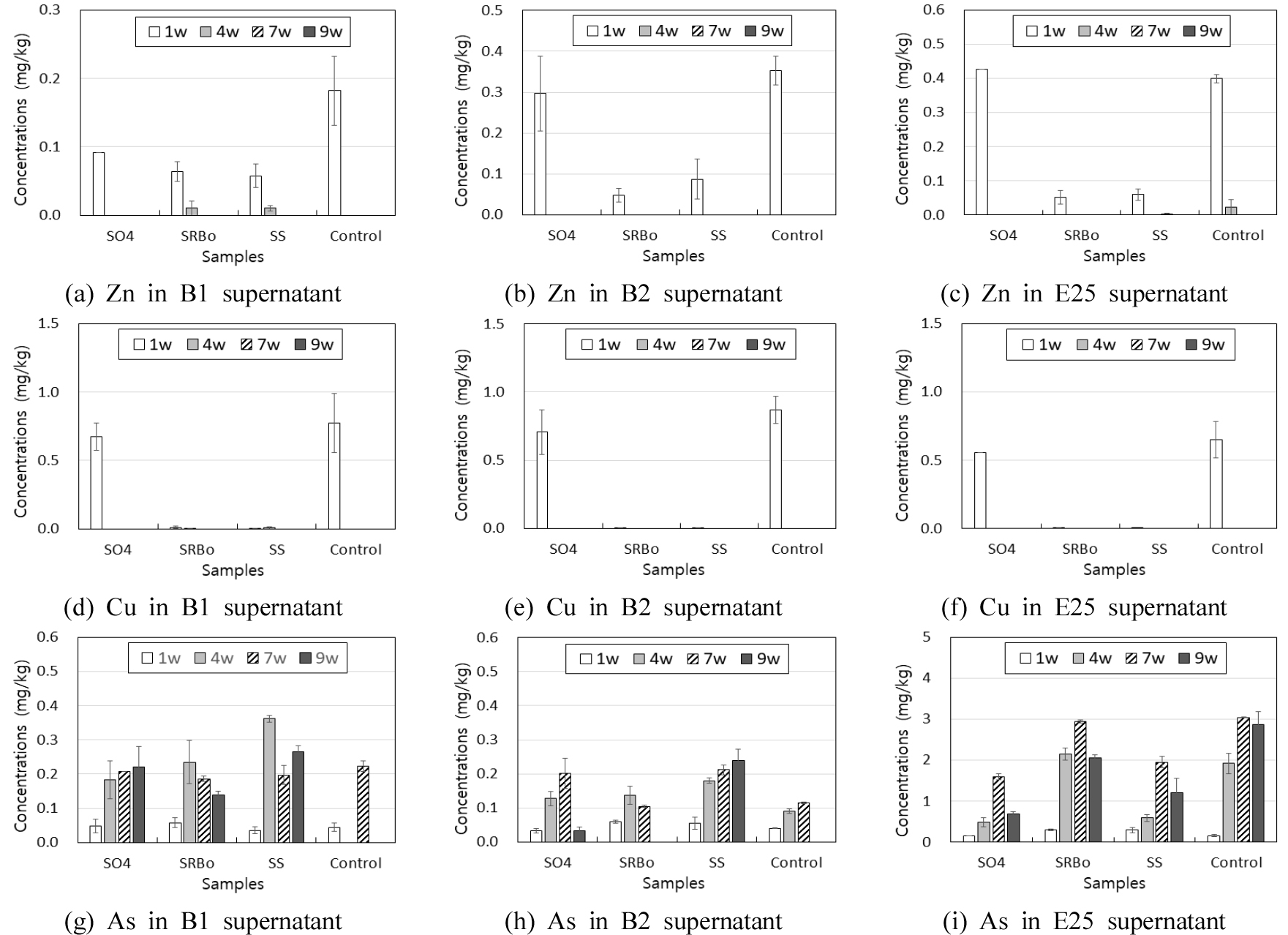
토양을 채취하여 단일용출법을 적용한 것과 별도로 토양 상등액을 채취하여 중금속 함량을 분석하였다(Fig. 3). Zn과 Cu는 1주 경과 시에만 용출되었으며 대체적으로 SS 및 SO4 시료에서 비교시료에 비하여 확연히 용출량이 감소하였다. 이후 시간이 경과한 후에는 비교시료에서도 거의 용출되지 않았으며 이는 중금속이 토양 입자 표면에 흡착된 상태로 존재하기 때문으로 보인다. Pb와 Cd의 경우, Zn과 Cu와 매우 유사한 결과가 나타났다.
한편, As의 경우, 토양 내 함량이 낮은 B1, B2 토양(12~14 mg/kg)에서는 특기할만한 차이를 보이지 않았으나 As 함량이 높은 E25 토양(82 mg/kg)은 토양 단일용출 결과와 유사하게 SS 및 SO4에서 용출량이 감소하였다(Fig. 3(i)). Ko et al.(2017)에 의한 현장 연구 결과에 의하면, 현장 토양수를 채취하여 분석한 결과 As 안정화 결과를 얻은 바 있으며 SRB에 의해 금은광산 주변 오염 토양 내 용이하게 용출되는 형태의 As 중 75% 정도가 감소되었다고 보고한 바 있다. 이러한 결과는 심부 토양에 SRB 및 적절한 SO42-를 공급하면 오염 토양으로부터 용출되는 As의 이동도를 효과적으로 감소시킬 가능성이 있음을 나타낸다.
결 론
폐광산 주변 중금속으로 오염된 농경지 3곳을 대상으로 하여 심부 토양 내 용존 중금속을 SRB를 이용하여 불용성 금속 황화물로 안정화시키는 실험을 수행하였다. SRB를 이용하여 안정화 처리한 토양을 대상으로 0.1 N HCl 및 Mehlich 단일용출법을 동시 적용한 결과, 토착미생물에 SO42-와 SRB를 동시에 적용하거나 또는 SO42- 만을 공급한 경우에서 상대적으로 높은 안정화 효율을 보여 심부 토양에서 중금속의 이동도를 감소시킬 수 있음을 나타내었다. 반면, 멸균 토양에 SRB를 접종한 경우에는 낮은 효율을 보였으며 이는 효과적인 황산염환원을 유도하기 위해서는 별도의 SO42-를 주입해야 함을 나타낸다.
또한 0.1 N HCl과 비교하였을 때 Mehlich 용출 결과에서 다수의 중금속이 비교시료에 비하여 높은 안정화 효율을 보인 것은 SRB에 의해 환원된 침전물의 안정성이 두 용출제의 용출능 사이에 존재하는 것을 나타낸다.
한편, 토양의 단일용출 결과 As의 안정화는 관찰되지 않았으나 토양 상등액을 채취하여 분석한 결과 As 용출량이 감소하였으므로 심부 토양에 SRB 및 적절한 SO42-를 공급하면 오염 토양으로부터 용출되는 As의 이동도를 감소시킬 수 있을 것으로 보인다.
SRB를 이용한 중금속 안정화 기술이 실용화되면 그간 굴착 등을 통한 접근이 어려웠던 심부 농경지 토양 환경에 대한 중금속 처리가 가능해지게 될 것이다. 작물 근권 부근의 얕은 심도는 현재 수행되고 있는 공정처럼 안정화층을 설치하고 복토 및 환토 등을 통해 중금속 안정화를 도모하고, 하부 심도에는 SO42- 및 필요한 경우 SRB를 부지 내 넓은 범위에 걸쳐 소구경 천공을 통해 인위적으로 주입함으로써 중금속을 안정화하여 상부로 이동하는 현상을 방지할 수 있을 것이다.
이 연구에서는 황산염환원을 수행하는 SRB 단일 기능에만 초점을 맞춰 진행하였으나 향후 미생물군 유전체 분석을 통해 토착미생물의 미생물 군집을 함께 파악함으로써 접종한 SRB의 기능을 촉진 또는 저해하는 메커니즘을 규명하는 연구가 필요할 것으로 생각한다. 이러한 연구를 통해서 연구에 따라 나타나는 부지특이적(site-specific)인 다소 상이한 결과에 대한 원인 규명이 가능할 것으로 보인다.