서론
침강성탄산칼슘(Precipitated Calcium Carbonate, PCC)은 불순물 함량이 낮고, 백색도가 높으며, 균일한 입도 및 입형 제어가 가능한 합성 탄산칼슘으로 알려져 있다. 이러한 이유로 침강성탄산칼슘은 부가가치가 높은 석회석 제품으로 고급 제지 초지용 필러나 제지 코팅용 제품, 고기능성 고무나 플라스틱의 충전제로 사용되고 있다.
침강성탄산칼슘은 화학조성, 즉 CaCO3은 같으나 여러 형태의 결정구조를 갖는 대표적 동질이상(Polymorphism) 물질이다. 대표적인 동질이상의 침강성탄산칼슘으로 육방밀집구조를 갖는 방해석(Calcite)과 침상의 사방정계(orthor-hombic)구조를 갖는 아라고나이트를 들 수 있다. 이러한 동질이상의 침강성탄산칼슘은 석회석 원석을 700°C 이상의 온도에서 탈탄산하여 생석회(Lime, CaO)화하는 하소(Calcination) 공정과 생석회를 물과 반응하여 소석회(Slaked lime, Ca(OH)2)를 합성하는 수화(Hydration) 공정, 소석회를 이산화탄소와 반응시켜 침강성탄산칼슘을 생성시키는 탄산화(Carbonation) 공정을 통해 합성된다. 이때 사용된 석회석 원석의 광물학적 특성과 각 공정의 조건은 침강성탄산칼슘의 결정구조를 결정하는 매우 중요한 변수가 된다. 특히 석회석 원석의 산지에 따른 영향이 매우 큰 것으로 알려져 있다(Yang et al., 2014a, 2014b). 이는 석회석의 불순물의 종류와 함량과 같은 화학 조성과 석회석의 결정성 등에 따른 반응성(또는 활성도)에 기인한다.
침강성탄산칼슘의 원료가 되는 석회석은 국내에는 강원도와 충청북도에만도 약 60억 톤이 매장되어 있는 것으로 추정되고 있다. 이렇게 풍부한 매장량 때문에 국내 석회석을 주(부)원료로 하는 시멘트, 철강/제철, 제지(중탄용) 산업 등에서의 자급율은 100%에 이른다. 그러나 이와는 대조적으로 고품질 고기능성 침강성탄산칼슘의 경우 국내의 수요가 지속적으로 증가되고 있는 추세에도 불구하고 많은 양이 수입 제품에 의존하고 있다. 현재 일부 국내 기업에서도 침강성탄산칼슘을 생산하고 있으나 국내 석회석 광산에서 채광된 원석을 이용하여 다양한 침강성탄산칼슘을 생산하기 위해서는 아직도 많은 기술적 노하우 축적이 필요하다. 이러한 이유로 석회석 원석으로부터 침강성탄산칼슘 합성 공정에 대한 다양한 검토가 선행되어야 한다. 이는 석회석 원석의 하소 특성과 이에 따른 수화, 탄산화 거동에 대한 고찰이 매우 중요하다는 것을 의미한다. 이에 본 연구에서는 각기 다른 화학성분을 갖는 석회석을 이용하여 석회석 하소반응과 이에 따른 수화 활성도, 침성탄산칼슘의 생성에 미치는 상관성에 대해 논하였다.
연구 방법
본 실험에는 채광 지역과 화학조성이 다른 5종의 석회석이 사용되었다. 5종의 석회석을 죠크러셔(Jaw crusher)를 사용하여 파쇄한 후 체(sieve)를 이용해 입자 크기 20∼35 mm 범위의 시료 500 g을 취하여 실험에 사용하였다. 선별된 석회석을 전기로에서 하소하였는데, 하소 온도는 1,000°C, 하소 시간은 2시간으로 하였다. 이때 승온 속도는 분당 10°C로 하였다. 이론상 석회석의 탈탄산 반응은 848°C에서 일어난다(식 (1)). 본 실험에서는 완전한 탈탄산 반응을 위해 이론 온도 보다 높은 1,000°C에서 하소하였다.
CaCO3(S) → CaO(S) + CO2(g), △Go = 0 at 848°C (1)
하소반응을 통해 얻어진 생석회를 대상으로 분말 X-선 회절 분석을 실시하였다. 이를 통해 각기 다른 석회석 원석에 따라 하소 조건인 1,000°C에서 생성된 생석회 결정학적 특성에 대해 고찰하였다.
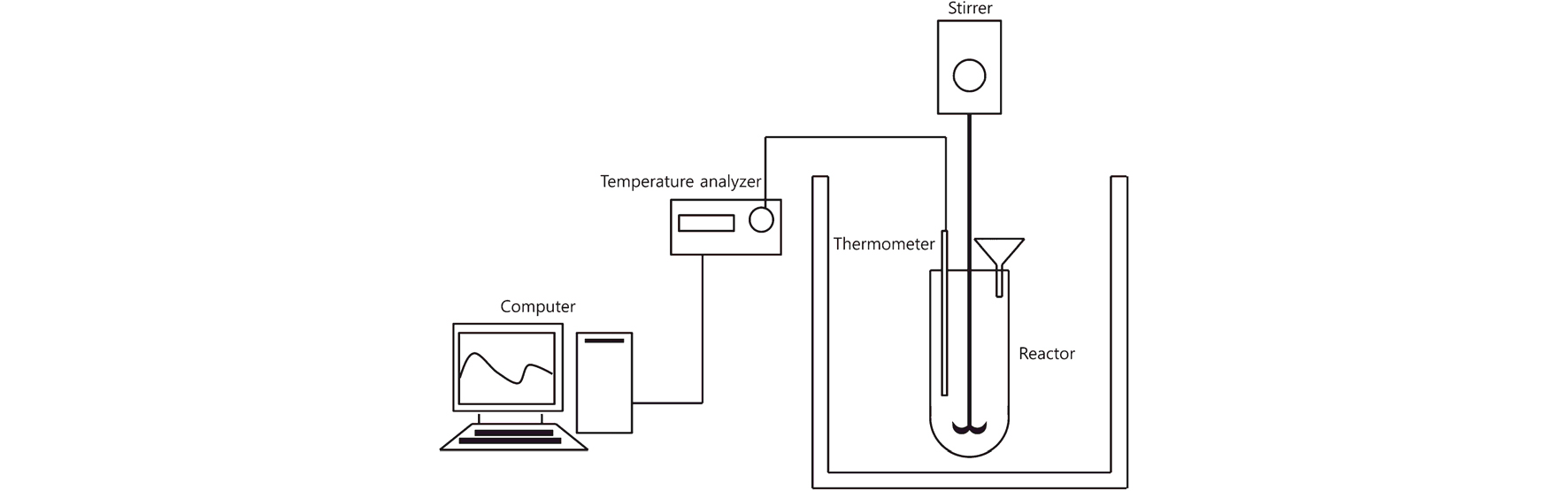
하소 공정을 통해 얻어진 5종의 생석회를 30g씩 마노 유발에서 분쇄한 후 수화 반응기(Fig. 1)에 수화반응을 실시하였다. 수화 반응에 사용된 수용액은 증류수이며, 그 양은 120 ml, 수화 개시와 동시에 400 rpm으로 교반하여 수화 반응 온도를 측정하였다.
수화 반응은 생석회가 물 분자와 반응하여 수산화칼슘인 소석회(Slaked lime, Ca(OH)2)가 생성되는 반응으로 발열 반응이다(식 (2)).
CaO(S) + H2O(L) → Ca(OH)2(S), △H = -64kJ (2)
수화 반응은 총 30분 동안 실시하였으며, 수화 반응 후 생성된 소석회는 여과지를 이용하여 반응하지 않은 물과 분리시키고 이어서 소석회 표면에 부착되어 있는 부착수를 제거하기 위해 에탄올로 3∼4회 추가 세척하여 여과하였다. 회수된 소석회는 결정수가 분해되지 않도록 40°C의 온도가 유지되고 있는 전기 오븐에서 건조하였다. 건조된 소석회는 공기 중의 이산화탄소와 반응하지 않게 진공 팩을 사용하여 진공 상태로 보관하였다. 이렇게 얻어진 소석회는 생석회와 같이 분말 X-선 회절 분석을 통해 소석회의 결정학적 특성 분석을 실시하였다. 이와 함께 생석회의 수화반응 과정에서 발생되는 수화열 측정하기 위해 KS E 3077의 ‘침강성탄산칼슘용 석회석의 활성도 측정 방법’에 따라 측정하였다. KS E 3077에 따르면 수화 개시 전 온도와 수화 반응 개시 30초 후의 수화 온도 값의 차를 활성도로 정의하고 있다(식 (3)).
A = T30 – T0 (3)
where
A : Hydration activity (°C)
T30 : Hydration temperature at 30 seconds (°C)
T0 : Initial hydration temperature (°C)
생석회의 수화 반응 후 잔존하는 수용액 내 칼슘 이온 농도는 원자흡수분광기(Atomic Absorption Spectroscopy)를 이용하여 측정하였다.
침강성탄산칼슘 합성을 위해 수화 반응에서 얻어진 소석회를 사용하여 탄산화 반응을 실시하였다. 실험 조건은 Kim (2004)이 아라고나이트 합성의 최적 조건으로 제시한 CaCO3-NaOH-Na2CO3계 수용액 합성 방법에 따라 실시하였다(식 (4)). 침강성탄산칼슘 합성에는 0.5M Na2CO3를 사용하였으며 합성 시간 210분, 반응기의 온도는 75°C로 하였다.
Ca(OH)2(S) + Na2CO3(S) + Heat → CaCO3(S) + 2NaOH(L) (4)
반응 후 합성된 침강성탄산칼슘으로부터 미 반응 이온 성분들을 제거하기 위해 에탄올로 3∼4회 세척하며 여과하였다. 회수된 침강성탄산칼슘은 분석 전 공기와의 접촉을 최소화하기 위해 진공 팩에 보관하였다. 합성된 침강성탄산칼슘의 정량/정성 분석을 위해 알루미나를 내부 표준 분석 시료로 한 분말 X-선 회절 분석을 실시하였다.
결과 및 고찰
시료
본 실험에 사용된 석회석의 생성 연대는 중생대(시료 A) 1종, 고생대 전기(시료 B, C, D) 3종, 고생대 후기(시료 E) 1종으로 총 5종이 사용되었다. Table 1은 본 실험에 사용된 석회석의 화학 조성과 생성 시기를 나타내고 있다.
Table 1. Chemical compositions of limestone ores (unit: wt.%)
하소 반응과 수화 반응
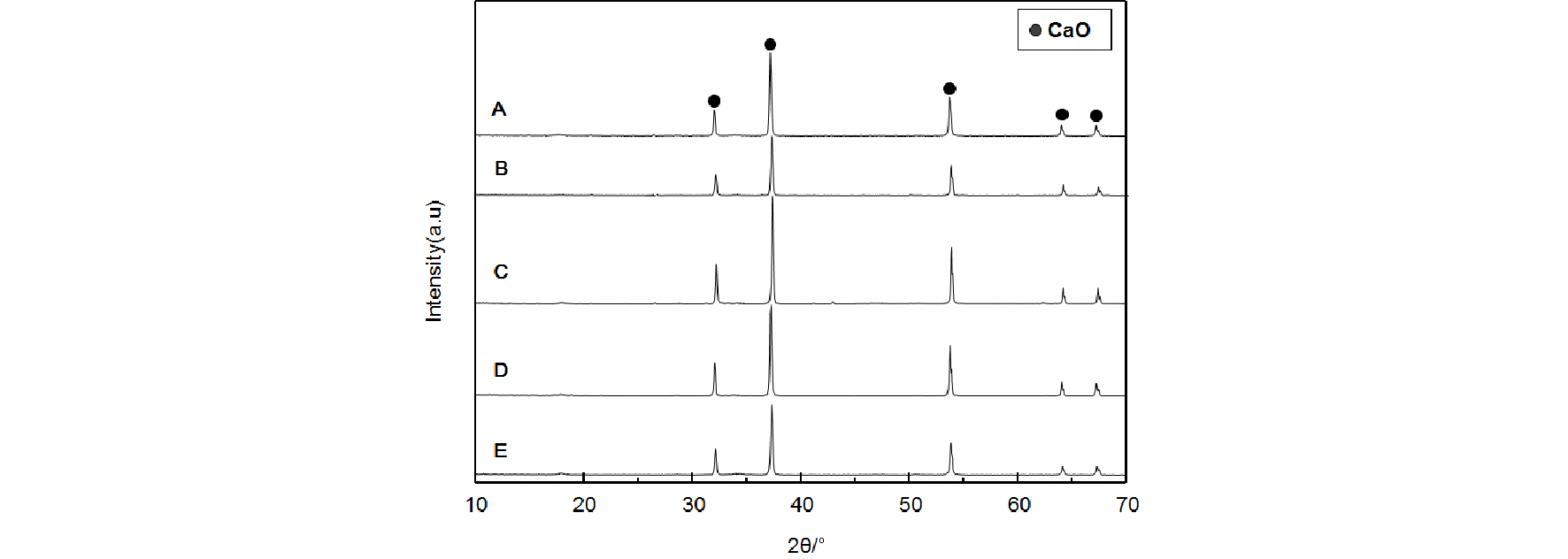
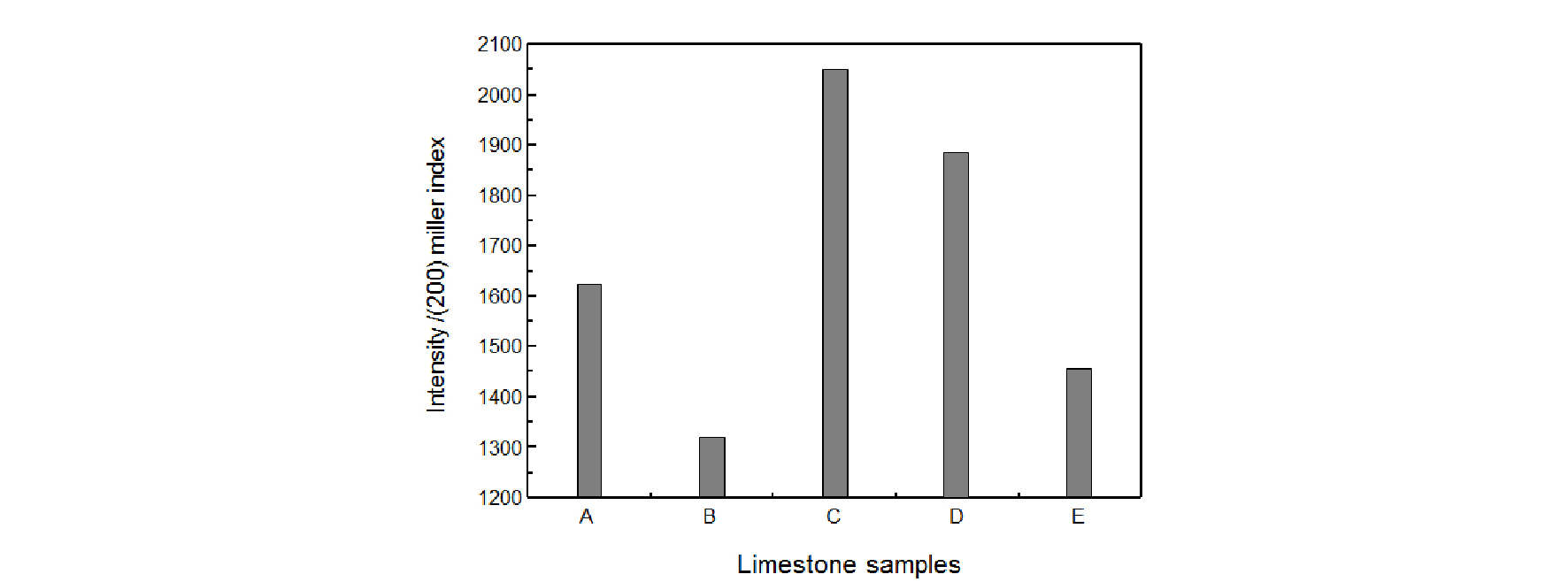
Fig. 2는 5종의 석회석을 1,000°C에서 2시간 동안 하소를 통해 얻어진 생석회의 X-선 회절 곡선을 나타내고 있다. 분석 결과 5종의 석회석 모두 탈탄산화 반응에 의해 순수한 생석회(CaO)가 생성된 것으로 나타났다. Fig. 3은 생석회의 주 결정면의 면 지수 (200)에서의 X-ray선 회절 강도를 나타내고 있다. 분석 결과 석회석 C의 생석회 결정화가 가장 높았으며, 반대로 석회석 B가 가장 낮게 나타났다. 이를 기준으로 강소(强燒, Hard burning) 정도를 C>D>A>E>B의 순으로 나타낼 수 있다.
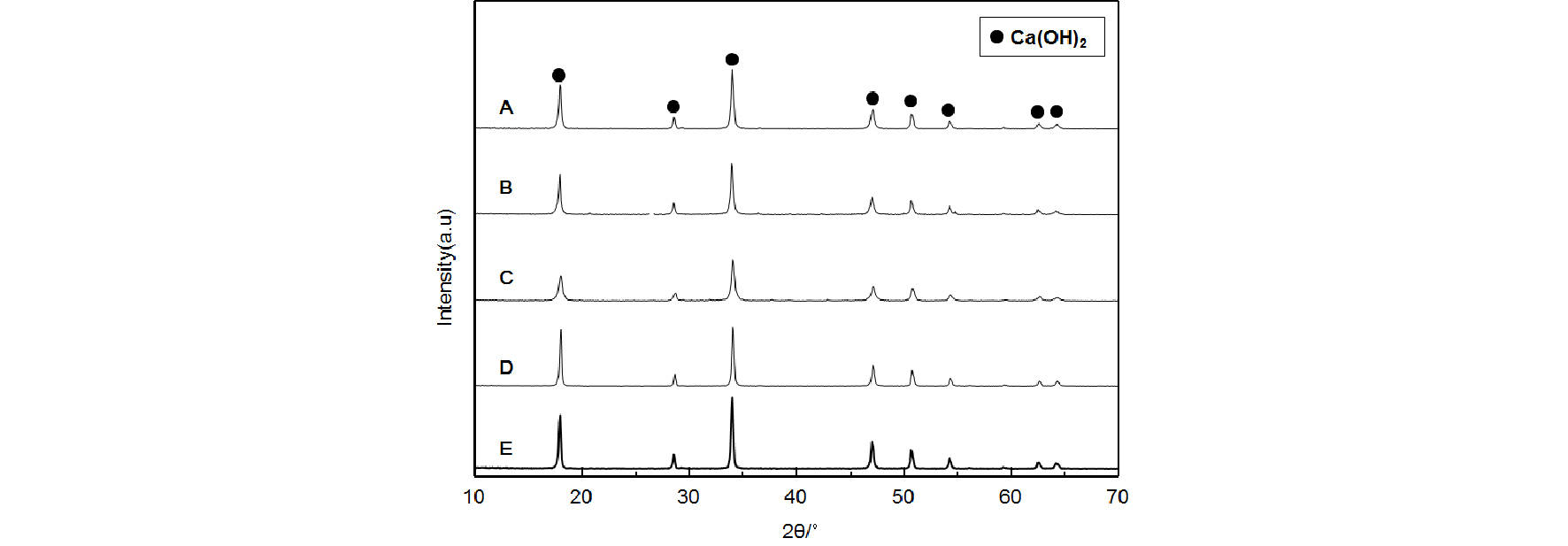
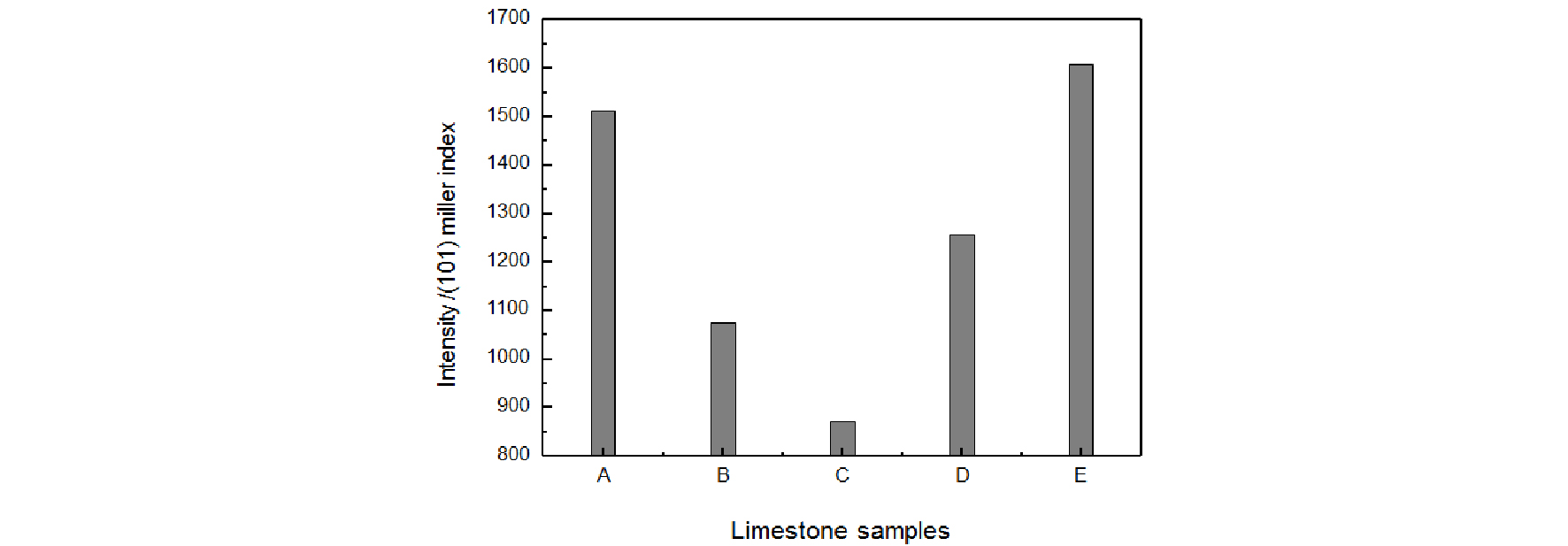
Fig. 4는 5종의 석회석으로부터 얻어진 생석회의 수화 반응에 의해 생성된 소석회의 X-ray 선의 회절 피크를 나타내고 있다. 5종의 생석회 모두 수화 반응을 통해 소석회로 상전이가 일어났다. Fig. 5는 수화 반응으로 생성된 소석회의 주 결정면의 면 지수(101)에서의 X-ray선 회절 강도를 나타내고 있다. 같은 수화 반응 조건에서의 높은 결정성을 보인 소석회는 석회석 E와 A의 생석회로 나타났고, 결정성이 가장 낮은 소석회는 석회석 C의 생석회로 나타났다. 소석회의 결정성이 높은 순서는 E>A>D>B>C로 나타났다. 이는 석회석 B를 제외하고 생석회의 결정성과 역전 현상이 일어났음을 확인할 수 있다. 특히, 석회석 C의 경우 가장 높은 결정성의 생석회를 나타냈으나, 소석회의 결정성은 가장 낮게 나타났다. 이는 하소 단계에서 석회석의 종류에 따라 같은 하소 조건에서 탈탄산화 반응 이후, 강소(Hard burning) 정도에 따라 생석회의 결정화도 및 치밀도를 증가시키는 소성 반응이 일어나고, 이러한 결과는 생석회의 수화 반응 단계에서 수화 반응성이 저하되는 결과와 상관성이 존재하는 것을 알 수 있다.
이와는 반대로 같은 하소 조건에서 석회석 E와 A는 탈탄산 반응만 일어나고, 생석회의 결정 성장이나 치밀화는 일어나지 않아 상대적으로 높은 수화 반응성을 보인 것으로 판단된다.
석회석 B의 경우에 대해서는 추후 실험을 통해 수화 반응 저하 원인에 대해 규명하고자 한다.
위의 결과에 따라서 석회석의 종류에 따라 하소 단계에서의 강소(Hard burning) 정도에 따르며, 하소 단계에서 생석회의 결정 성장이나 치밀화가 일어날 경우 생석회의 수화 반응성의 저하 원인으로 작용할 수 있다는 것을 확인할 수 있었다.
수화 활성도
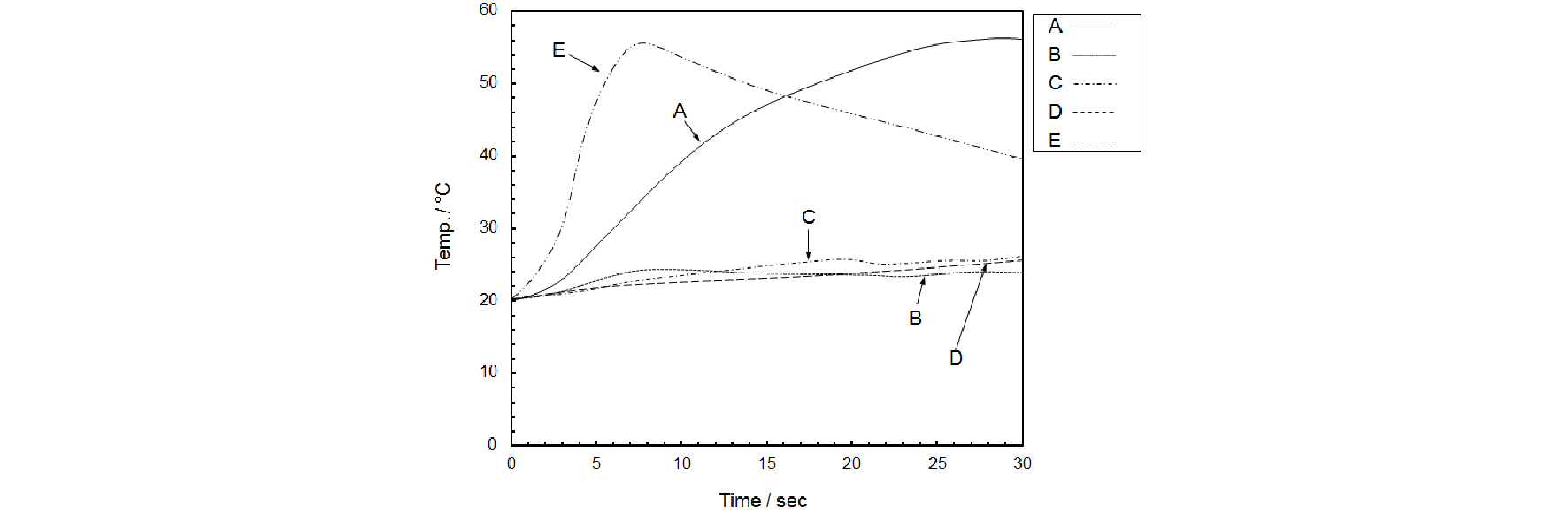
Fig. 6은 생석회의 수화 반응 시간에 따른 수화 온도 변화를 나타내고 있다. 생석회의 수화 반응은 발열 반응으로 반응 시간에 따른 발열량의 추이는 생석회의 수화 반응 속도를 예측할 수 있는 주요 척도이다. 수화 반응 개시 후 초기 수화 활성도는 석회석 E의 생석회가 가장 높게 나타났으며 다음으로 석회석 A의 생석회로 나타났다. 상대적으로 석회석 B, C, D의 수화 반응 속도는 매우 낮게 나타났다.
Table 2는 5종의 석회석의 생석회의 수화 활성도를 나타내고 있다. 석회석 A가 34.5°C로 가장 큰 값을 보였다. 다음으로 반응 초기 수화 활성도가 가장 높았던 석회석 E가 18.1°C로 나타났다.
Table 2. Hydration activity of different limestones (Unit: °C)
| Hydration activity | |
| A | 34.5 |
| B | 3.3 |
| C | 5.6 |
| D | 5.1 |
| E | 18.1 |
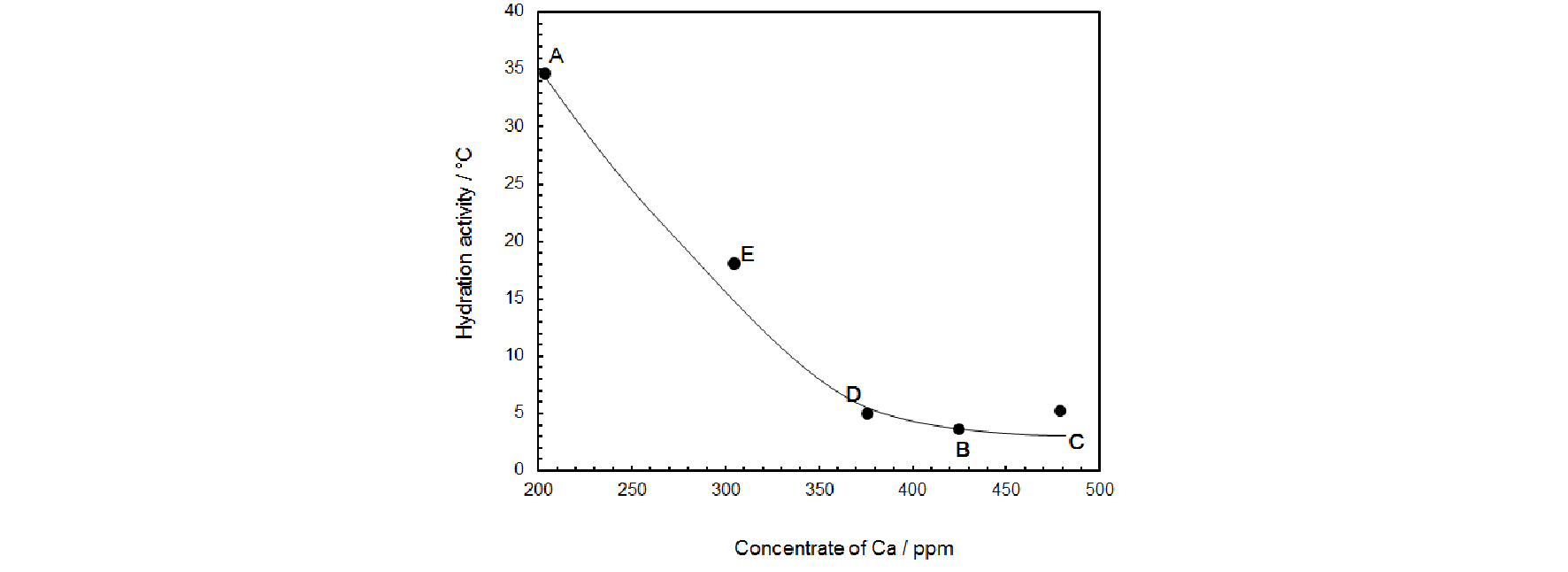
Fig. 7은 석회석 5종의 생석회의 수화 시간 30분 시점에서의 수화 용액 내 Ca2+ 이온 농도와 수화 활성도의 상관관계를 나타내고 있다. 결과에서 알 수 있듯이 수화 용액의 Ca2+ 이온의 농도와 수화 활성도의 관계는 반비례인 것을 알 수 있다. 수화 반응 시간 30분 내 용액의 Ca2+ 이온의 농도의 감소는 소석회를 생성에 의한 것으로 해석 할 수 있다. 수화 반응 개시 후 높은 Ca2+ 이온 농도의 과포화 상태에서 소석회의 결정핵이 생성되면 결정 성장에 의해 급격히 Ca2+ 이온 농도가 감소하고 Ca2+ 이온 농도의 평형 상태에 도달하게 된다. 문헌에 따르면 Ca2+ 이온의 농도가 낮은 환경에서는 소석회 결정 핵생성보다는 소석회의 결정 성장이 일어나며 이로 인해 결정성이 높은 소석회가 생성된다고 보고하고 있다(Kim et al 2007). 이러한 이유로 본 실험에서도 석회석 A와 E에서 결정성이 높은 소석회가 관찰될 수 있었다.
탄산화 반응
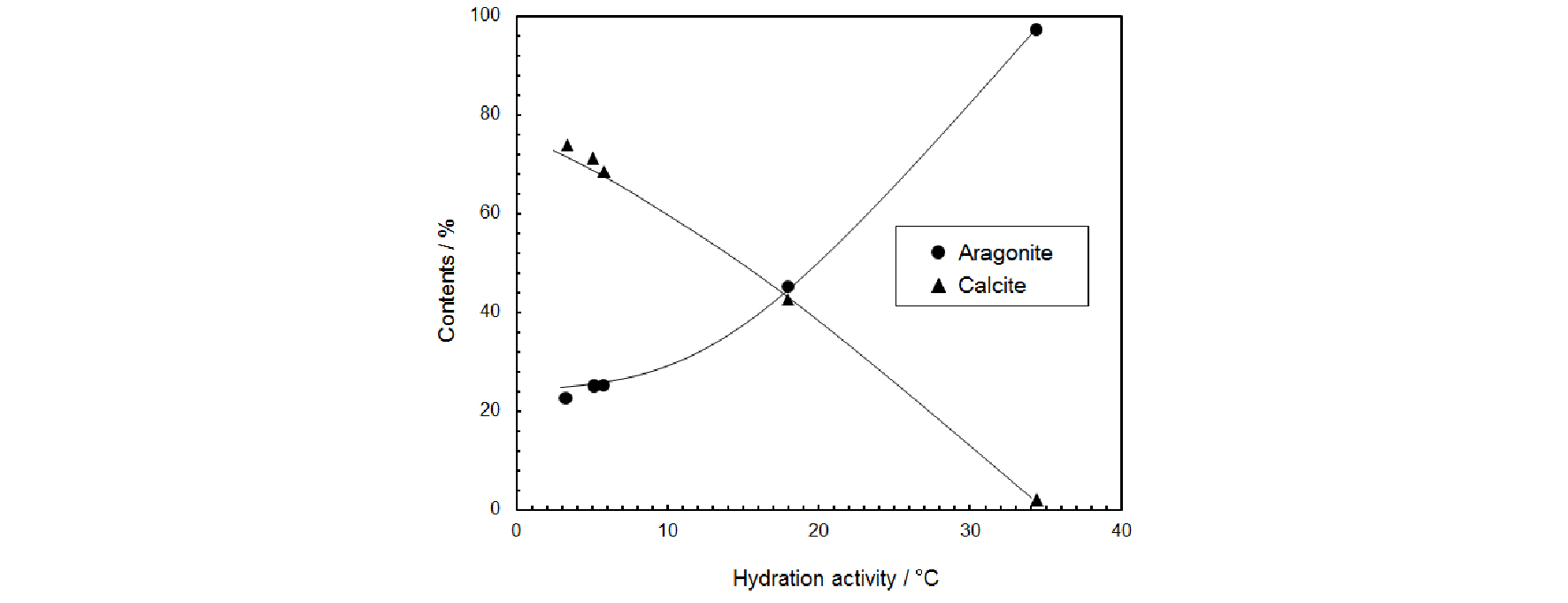
Fig. 8은 생석회의 수화 활성도와 탄산화 반응에 따른 생성되는 침강성탄산칼슘의 생성량의 상관관계를 나타내고 있다(Ahn et al., 2007). 생석회의 수화 활성도가 클수록 준 안정상인 아라고나이트(Aragonite)형 침강성탄산칼슘의 생성량이 높게 나타났다. 준 안정상인 아라고나이트형 침강성탄산칼슘의 생성량은 소석회의 결정이 클수록, 초기 수화반응 발열량이 클수록 증가하는 것으로 보고되고 있다(Kim et al., 2007; Ko et al., 2007). 본 논문에서 제시된 조건에서는 생석회의 수화 활성도(수화 속도, 누적 발열량)가 높은 석회석 A와 E에서 아라고나타이트형 침강성탄산칼슘이 생성되는 결과와 잘 일치하고 있다.
Fig. 9는 5종의 석회석 원석의 CaO와 MgO 함량에 따른 생성된 침강성탄산칼슘의 XRD 정량 분석을 실시한 결과를 나타내고 있다. 그러나 본 연구 결과에서는 CaO와 MgO의 함량과 침강성탄산칼슘의 생성 량 사이에는 뚜렷한 연관성을 살펴볼 수 없었다. 많은 연구들에서 침강성탄산칼슘의 합성 과정에 Mg2+ 이온을 소량 첨가할 경우 아라고나이트 침강성탄산칼슘의 생성 량을 증가시키는 것으로 보고되고 있다. 그러나 원석 내에 포함된 Mg의 경우는 소성과 수화 과정을 거치며 최종 산물에까지는 영향을 미치지 못하는 것으로 본 실험에서는 타났다. 이에 대한 고찰은 추후 실험을 통해 규명할 예정이다.
결론
본 연구에서는 화학 조성이 각기 다른 석회석을 이용하여 석회석 하소반응과 이에 따른 수화 활성도 및 동질이상의 침강성탄산칼슘의 합성 거동에 대해 고찰하였다.
1.석회석의 종류에 따라 1,000°C, 2시간의 하소 단계에서의 각기 다른 결정성의 생석회가 생성되었으며, 이를 통해 생석회의 결정 성장이나 치밀화가 생석회의 수화 활성도의 저하 원인으로 작용하는 것을 확인하였다.
2.수화 반응 후 수화 용액 내 잔류 Ca2+ 이온의 농도와 생석회의 수화 활성도의 관계는 반비례이며, 생석회의 수화 활성도가 높을수록 상대적으로 결정성이 높은 소석회가 생성되었다.
3.생석회의 수화 활성도가 높을수록, 소석회의 결정성이 높을수록 준안정상인 아라고나이트(Aragonite)형 침강성탄산칼슘의 생성 수율이 높게 나타났다.